Clear Sky Science · de
Datenbank für Lipid-Nanopartikel zur Struktur-Funktions-Modellierung und datengestützten Gestaltung für Nukleinsäure-Delivery
Warum winzige Fettbläschen für künftige Medikamente wichtig sind
Lipid-Nanopartikel sind mikroskopische, fettbasierte Bläschen, die genetische Anweisungen — etwa mRNA-Impfstoffe — sicher in unsere Zellen transportieren. Sie trugen wesentlich zum Erfolg der COVID-19-Impfstoffe bei, doch Forscher verstehen noch nicht vollständig, wie ihre detaillierte chemische Zusammensetzung ihre Wirksamkeit steuert. Dieser Artikel beschreibt eine neue Online-Ressource, die Lipid Nanoparticle Database (LNPDB), die verstreute Daten an einem Ort zusammenführt, damit Wissenschaftler systematisch bessere und sicherere Gen-Liefermedikamente entwerfen können.
Verstreute Ergebnisse an einem Ort bündeln
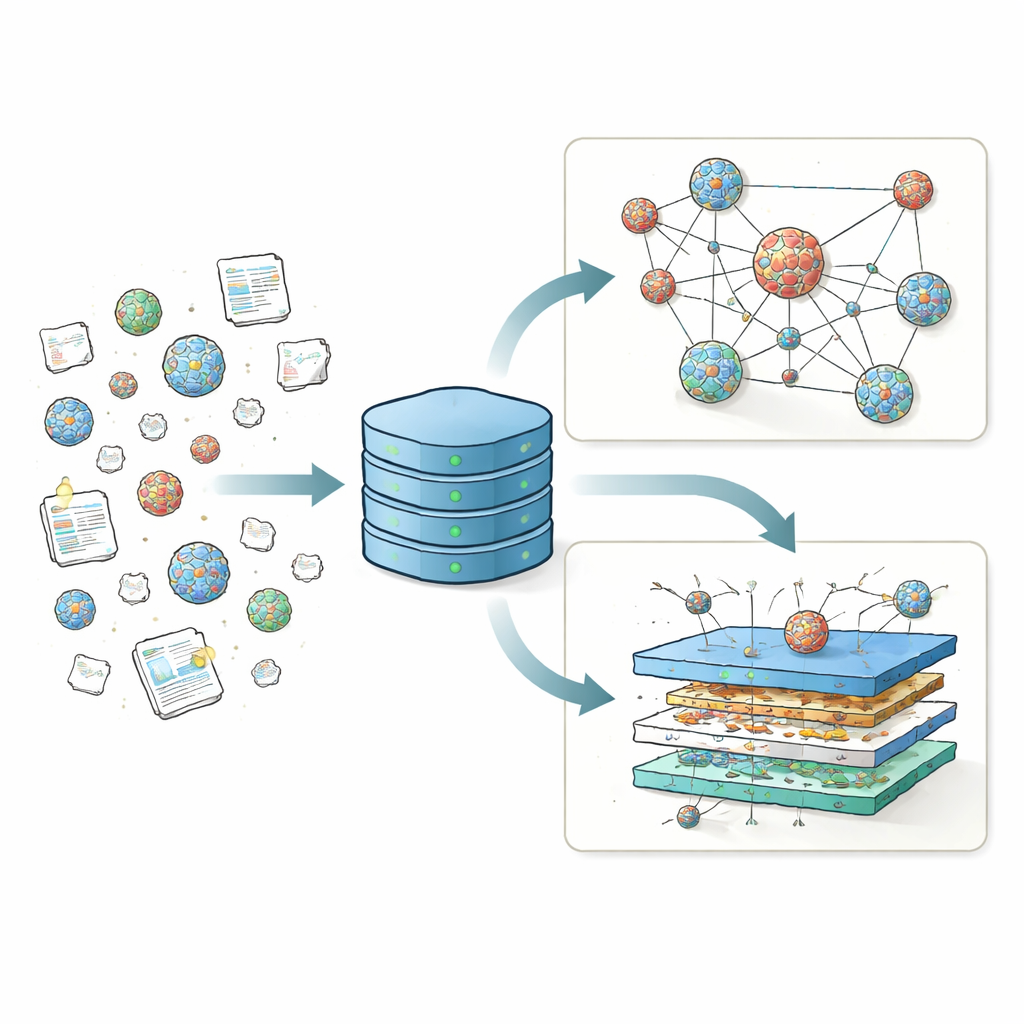
Jahrelang haben verschiedene Labore Tausende von Rezepturen für Lipid-Nanopartikel (LNP) getestet und dabei die Hauptladungsträgerlipide, Hilfslipide, Cholesterin und schützende Beschichtungslipide variiert, um zu sehen, welche Kombinationen genetisches Material am effektivsten liefern. Diese Ergebnisse wurden jedoch in vielen Formaten über Dutzende von Publikationen verteilt veröffentlicht, was Vergleiche und das Erkennen übergreifender Trends erschwerte. Anders als die Proteinforschung, die durch das zentrale Protein Data Bank gestützt wird und Werkzeuge wie AlphaFold beflügelt hat, hatte das LNP-Feld keine einheitliche Datenbank für Struktur- und Leistungsdaten. LNPDB schließt diese Lücke, indem sie detaillierte Informationen zu 19.528 LNP-Formulierungen aus 42 Studien und einem kommerziellen Anbieter sammelt und standardisiert, wie die Bestandteile, Versuchsbedingungen und Ergebnisse jedes Partikels codiert werden.
Was die neue Datenbank enthält
Jeder LNP-Eintrag in der LNPDB ist entlang dreier Hauptachsen beschrieben: Zusammensetzung, Experiment und Simulation. Die Zusammensetzungsfelder dokumentieren, welche Lipide verwendet wurden, wie viele Stickstoffatome das hauptsächliche geladene Lipid enthält und die genauen Mischungsverhältnisse zwischen den vier Kernkomponenten: ionisierbares Lipid, Hilfslipid, Cholesterin und ein Polyethylenglykol(PEG)-Lipid. Experimentfelder erfassen, welche Art genetischer Fracht geliefert wurde — meist mRNA, die für ein Reporterprotein kodiert —, wohin sie gesendet wurde (z. B. Zellen in einer Schale, Leber, Lunge oder Muskel), wie die Partikel hergestellt wurden und wie der Erfolg gemessen wurde. Schließlich liefern die Simulationsfelder gebrauchsfertige Dateien, die das physikalische Verhalten jedes Lipidmoleküls in ausreichendem Detail beschreiben, um atomare Computersimulationen von Lipidmembranen durchzuführen. Zusammen verwandeln diese standardisierten Beschreiber ein Flickwerk einzelner Screens in eine kohärente Landschaft, die von der Gemeinschaft durchsucht, gefiltert und erweitert werden kann.
Computern beibringen, bessere Formulierungen zu erkennen
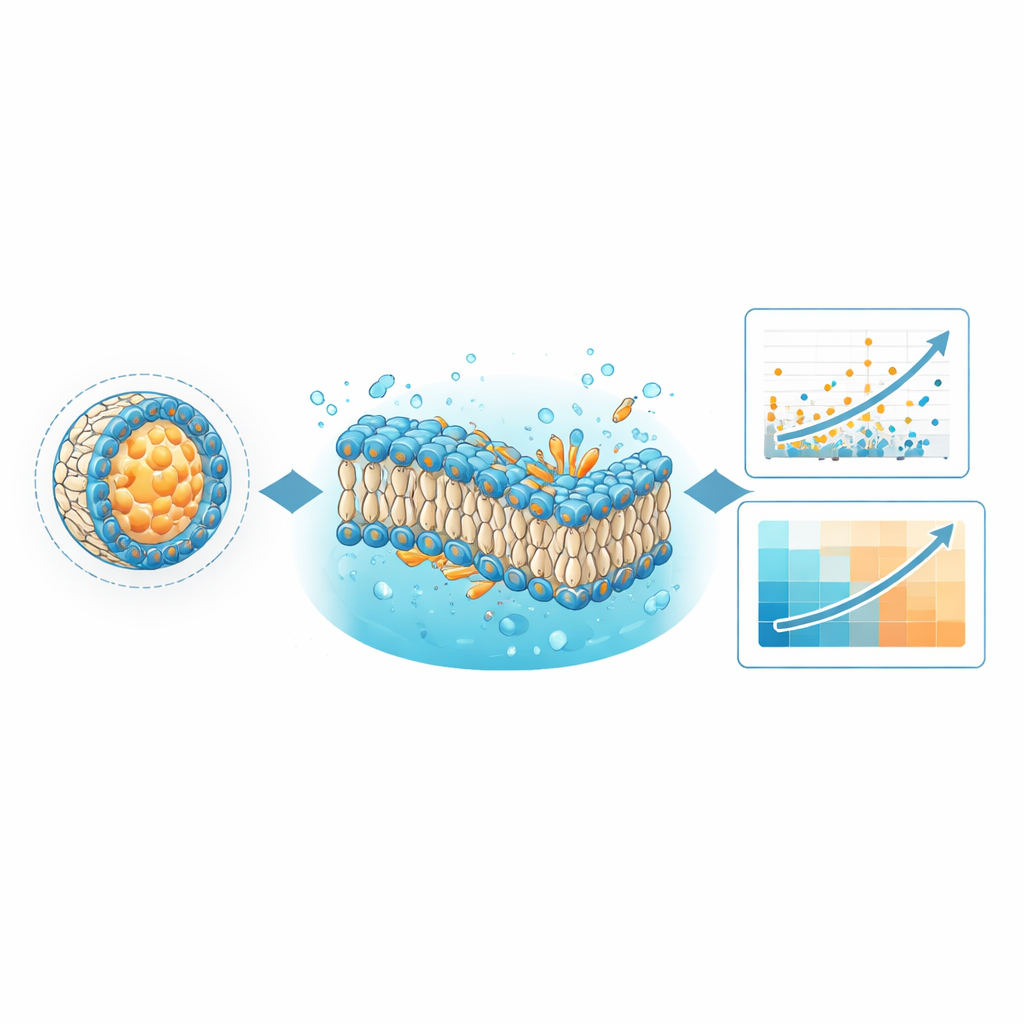
Eine unmittelbare Anwendung der LNPDB ist die Verbesserung von Modellen des maschinellen Lernens, die vorhersagen, welche Formulierungen genetisches Material am effektivsten liefern. Die Autorinnen und Autoren trainierten ihr bestehendes Deep-Learning-Modell namens LiON mit dem erweiterten LNPDB-Datensatz neu und mehr als verdoppelten damit die Anzahl der verfügbaren Beispiele. LiON lernt Muster, die die chemischen Strukturen der ionisierbaren Lipide, das Gemisch der Hilfskomponenten und den Testkontext mit der Performance jeder Formulierung verknüpfen. Mit den reichhaltigeren Daten stimmten LiONs Vorhersagen für die meisten Testsets besser mit experimentellen Ergebnissen überein und übertrafen in mehreren unabhängigen Datensätzen ein Konkurrenzmodell namens AGILE. Das deutet darauf hin, dass ein breiter, vielfältiger und kontinuierlich wachsender Trainingssatz entscheidend ist, um allgemein einsetzbare Entwurfswerkzeuge für zukünftige LNP-Medikamente zu entwickeln.
Modellmembranen beobachten, um verborgene Regeln zu entdecken
Die Datenbank ist auch für eine ganz andere Art von Berechnung ausgelegt: physikbasierte Simulationen mittels molekularer Dynamik. Mithilfe der mit LNPDB gebündelten Simulationsdateien baute das Team vereinfachte Membranen, die ausgewählte LNP-Formulierungen repräsentieren, und beobachtete ihr Verhalten über Mikrosekunden simulierte Zeit. Sie stellten zwei Fragen: Bleiben die modellierten Lipiddoppelschichten intakt, und welche Gesamtform nehmen die Schlüssellipide innerhalb der Membran an? Die Simulationen zeigten, dass Formulierungen, deren Membranen stabil blieben, experimentell eher erfolgreich waren. Außerdem quantifizierten sie ein Merkmal, das als „kritischer Packungsparameter“ bezeichnet wird und widerspiegelt, ob ein Lipid in der Membran eher konusförmig oder invert-konusförmig ist. In mehreren getesteten Bibliotheken zeigten Lipide, deren Form eine negative Krümmung begünstigte — was als förderlich für das Verschmelzen mit und das Stören endosomaler Membranen angesehen wird — stärkere Lieferwirkung, gelegentlich mit besserer Korrelation zur Performance als das Deep-Learning-Modell selbst.
Eine neue Grundlage für intelligentere Nanomedizin
Für Nicht-Spezialisten lautet die Kernbotschaft, dass diese Arbeit eine gemeinsame, wachsende „Landkarte“ darüber aufbaut, wie die Zutaten und die Struktur winziger Fettbläschen mit ihrer Fähigkeit zusammenhängen, genetische Therapien zu liefern. Indem sie Zehntausende vergangener Experimente zusammenführt, leistungsfähige Vorhersagemodelle ermöglicht und Werkzeuge bereitstellt, um zu simulieren, wie Partikel auf molekularer Ebene verhalten, legt LNPDB das Fundament für rationalere Gestaltung statt Versuch-und-Irrtum. Im Laufe der Zeit könnte dieser datengestützte Ansatz die Entwicklung wirksamerer Impfstoffe, Geneditierungsbehandlungen und anderer nukleinsäurebasierter Therapien beschleunigen und Forschern helfen zu verstehen, warum bestimmte Nanopartikel-Rezepturen funktionieren — und andere nicht.
Zitation: Collins, E., Ji, J., Kim, SG. et al. Lipid Nanoparticle Database towards structure-function modeling and data-driven design for nucleic acid delivery. Nat Commun 17, 2464 (2026). https://doi.org/10.1038/s41467-026-68818-1
Schlüsselwörter: Lipid-Nanopartikel, mRNA-Delivery, Nanomedizin, Maschinelles Lernen, Molekulare Dynamik