Clear Sky Science · de
Chemisch geführte Einzelzell-Transkriptomik enthüllt sulfotransferasevermittelte Gerüstumbildung in der Securinine-Biosynthese
Warum die Chemie eines Strauchs wichtig ist
Securinega-Alkaloide sind potente Moleküle, die in einem kleinen Zierstrauch, Flueggea suffruticosa, vorkommen und lange wegen ihres Potenzials gegen Krebs und neurologische Erkrankungen untersucht wurden. Bislang war jedoch weitgehend unbekannt, wie die Pflanze diese komplexen Verbindungen tatsächlich synthetisiert. Diese Studie kombiniert moderne Einzelzell-Genexpressionsanalyse mit geschickten chemischen Experimenten, um Schritt für Schritt zu zeigen, wie die Pflanze diese Moleküle zusammenbaut und umformt – und entdeckt dabei überraschend eine neue Funktion für einen verbreiteten Enzymtyp. 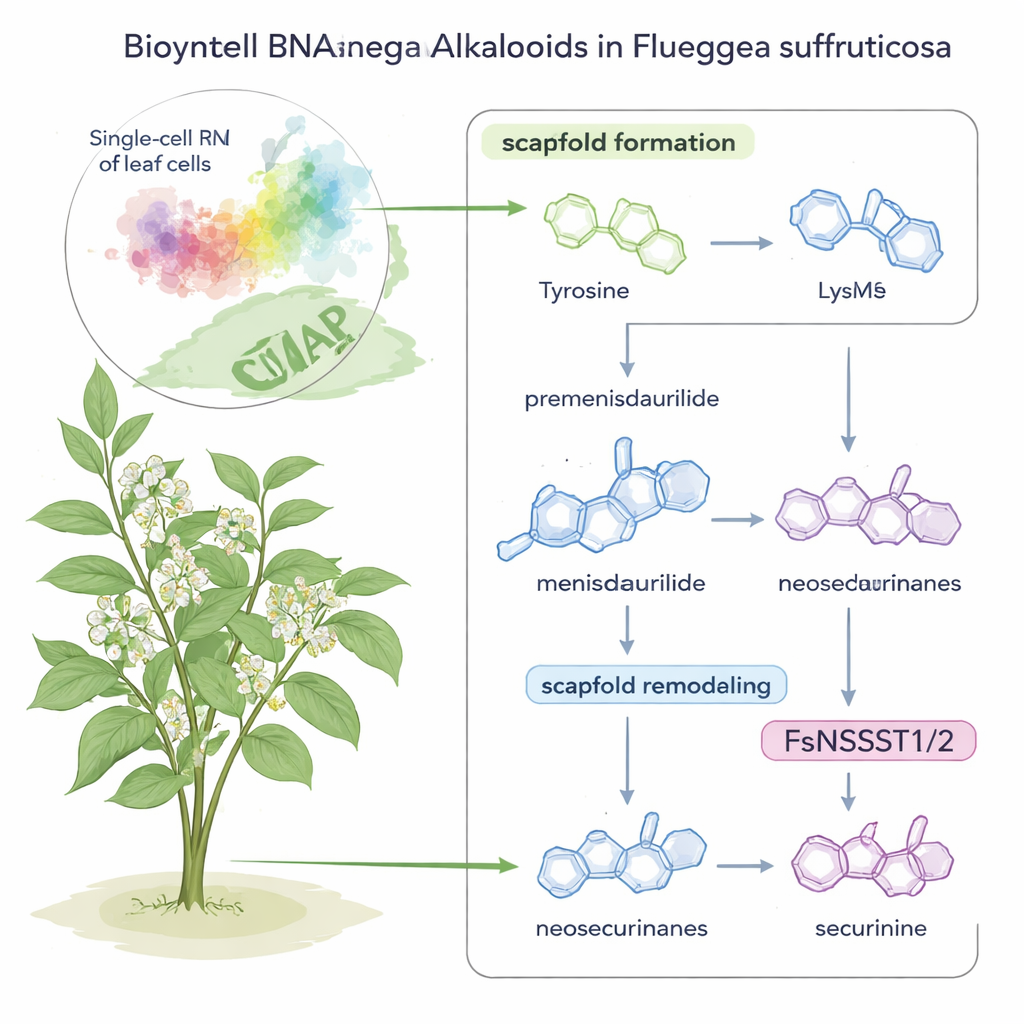
Bausteine aus alltäglichen Aminosäuren
Die Geschichte beginnt mit zwei vertrauten Nährstoffen: den Aminosäuren Tyrosin und Lysin. In F. suffruticosa wird Tyrosin in ein ungewöhnliches ringförmiges Molekül namens Premenisdaurilid umgewandelt, das dann durch ein neu entdecktes Enzym, das die Autoren FsMS (für „menisdaurilide synthase“) nennen, zu Menisdaurilid reduziert wird. Parallel dazu wird Lysin durch ein anderes Enzym, FsPS, das in früheren Arbeiten entdeckt wurde, in einen kleinen stickstoffhaltigen Ring namens 1‑Piperidein verwandelt. Treffen Menisdaurilid und 1‑Piperidein unter leicht basischen, wässrigen Bedingungen aufeinander, fusionieren sie spontan zu „Neosecurinane“-Alkaloiden – Zwischenstrukturen auf dem Weg zu den finalen, medizinisch relevanten Verbindungen.
Chemie in Echtzeit beobachten
Um zu belegen, dass diese vorgeschlagenen Schritte nicht nur theoretisch sind, synthetisierte das Team Versionen der vermuteten Zwischenprodukte, die mit schweren Kohlenstoffatomen markiert waren. Durch das Füttern dieser markierten Moleküle an Pflanzenextrakte konnten die Wissenschaftler genau verfolgen, wo die Atome landeten. Sie beobachteten, wie markiertes Menisdaurilid in markierte Neosecurinane und diese wiederum in die bekannten Alkaloide Allosecurinine und Securinine übergingen, was bestätigte, dass diese Zwischenstufen tatsächlich entlang des natürlichen Weges liegen. Wichtig ist, dass einige der entscheidenden ringbildenden Reaktionen sogar in abgekochten Extrakten stattfanden, was zeigt, dass Teile der Route ohne Enzyme ablaufen können und allein durch die Chemie der Moleküle angetrieben werden.
Fokussieren auf die richtigen Zellen
Zu wissen, welche Moleküle wo auftreten, ist nur die halbe Aufgabe; um die Gene zu identifizieren, die jeden Schritt steuern, muss man wissen, welche Zellen die Arbeit verrichten. Die Forschenden sequenzierten RNA aus Tausenden einzelner Zellen von F. suffruticosa‑Blättern und gruppierten sie anhand von Genaktivitätsmustern in verschiedene Zelltypen. Dabei fiel ein Cluster, das mit den Blattadern assoziiert ist, besonders auf: Es zeigte eine starke Expression bekannter Weggene und vieler Enzyme, die mit Tyrosin-, Lysin‑ und Schwefelstoffwechsel verknüpft sind. Durch die Untersuchung, welche Gene innerhalb dieses Clusters im Gleichklang mit den Wegenzymen variierten, konzentrierte das Team seine Suche auf FsMS und zwei Sulfotransferasen, FsNSST1 und FsNSST2, als vielversprechende Kandidaten für die fehlenden Schritte. 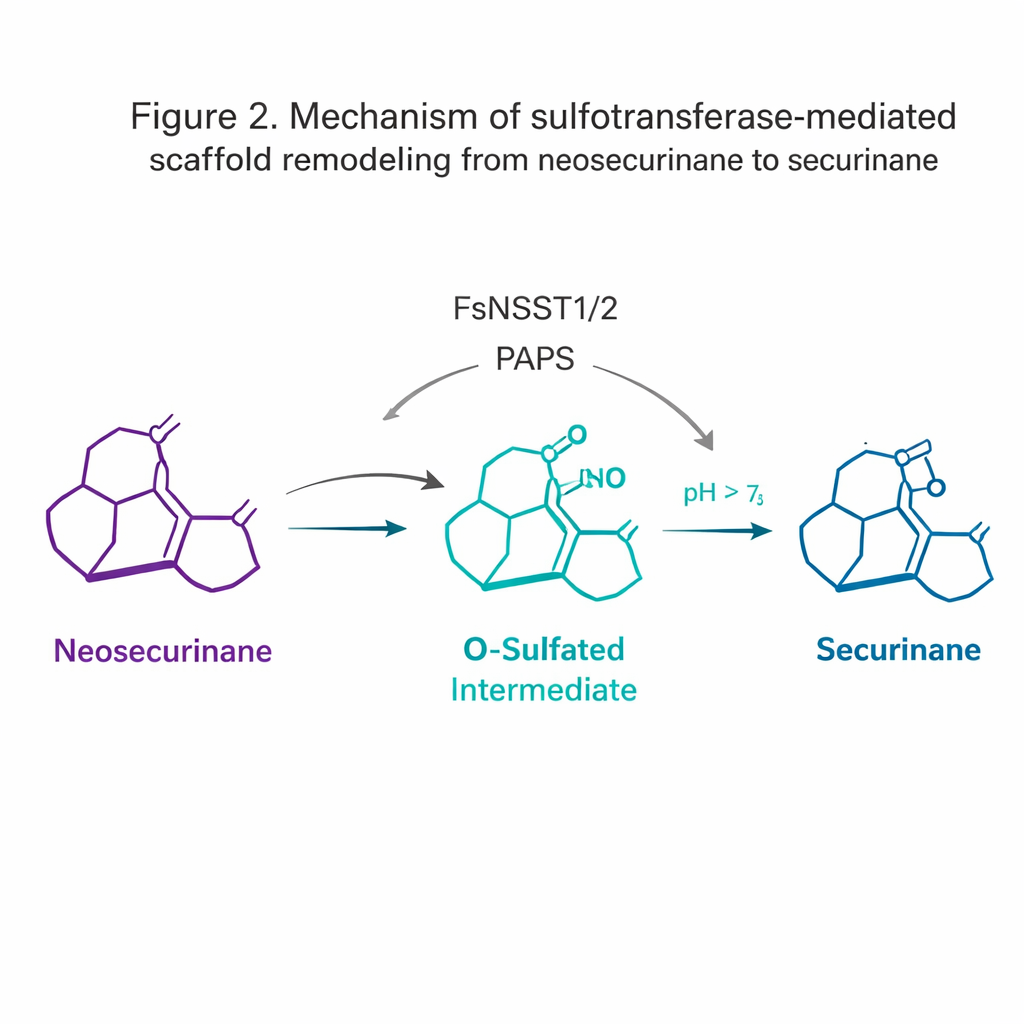
Ein Enzym, das das molekulare Gerüst umgestaltet
Die überraschendste Entdeckung betraf die Sulfotransferasen. Sulfotransferasen hängen normalerweise eine Sulfatgruppe an Moleküle an, um deren Löslichkeit zu verbessern oder sie zum Abbau zu markieren. Hier wirken FsNSST1 und FsNSST2 jedoch als Umschalter: Sie heften Sulfat an das Neosecurinane‑Gerüst an und erzeugen kurzzeitig ein energiereiches „O‑sulfatiertes“ Zwischenprodukt. Diese aktivierte Form durchläuft dann spontan eine 1,2‑Amin‑Verschiebung – eine kleine Umordnung, bei der ein Stickstoffatom wandert – und wandelt das [2.2.2] bicyclische „Neosecurinane“‑Gerüst in das [3.2.1] „Securinane“‑Gerüst um. Dieser subtile Umbauschritt erzeugt den charakteristischen tetracyclischen Kern der biologisch aktiven Alkaloide.
Warum dieser Weg von Bedeutung ist
Für Nicht‑Spezialisten ist die Kernbotschaft, dass die Pflanze Securinega‑Alkaloide in zwei Hauptphasen zusammensetzt: Zuerst baut sie aus alltäglichen Aminosäuren ein vorläufiges Ringsystem; dann formt sie dieses Gerüst chemisch mit einem Sulfat‑„Auslöser“ zu einer komplexeren Struktur um. Durch die Kombination von Einzelzell‑Genprofilierung mit isotopenmarkierter Chemie kartieren die Autoren diese Route im Detail und zeigen, dass Sulfotransferasen – Enzyme, die in allen Lebensformen vorkommen – mehr tun können, als Moleküle nur zu verzieren; sie können umfassende Umordnungen ihrer Struktur initiieren. Das Verständnis dieses Weges klärt nicht nur, wie eine vielversprechende Klasse von wirkstoffähnlichen Molekülen in der Natur hergestellt wird, sondern eröffnet auch Möglichkeiten, Pflanzen oder Mikroben so zu gestalten, dass sie neue, von Securinega inspirierte Arzneistoffe produzieren.
Zitation: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Schlüsselwörter: Pflanzenalkaloide, Biosynthese, Einzelzell-Transkriptomik, Sulfotransferase, Naturstoffchemie