Clear Sky Science · de
ALKB-1‑abhängige tRNA‑Methylierung ist für eine effiziente Eliminierung väterlicher Mitochondrien erforderlich
Warum die Mitochondrien der Väter still verschwinden
Jeder Mensch, jeder Wurm und die meisten anderen Tiere erben ihre zellulären Kraftwerke — die Mitochondrien — nahezu vollständig von der Mutter. Die Mitochondrien des Vaters gelangen mit dem Spermium in die Eizelle, werden dort jedoch rasch entfernt, ein biologischer Aufräumprozess, der verhindert, dass beschädigte mitochondriale DNA weitergegeben wird. Diese Studie an winzigen Fadenwürmern enthüllt eine molekulare „Stress‑Schaltstelle“, die mitentscheidet, ob väterliche Mitochondrien effizient beseitigt werden, und liefert Hinweise, die eines Tages mit bestimmter Unfruchtbarkeit und mitochondrialen Erkrankungen in Verbindung stehen könnten.
Die Kraftwerke, die wir von der Mutter erben
Mitochondrien erzeugen die Energie, die Zellen am Leben hält, und tragen eine eigene kleine ringförmige DNA. Im Laufe des Lebens kann diese mitochondriale DNA schädliche Mutationen anhäufen. Würden beide Eltern ihre Mitochondrien routinemäßig weitergeben, könnten sich diese Defekte mischen und über Generationen akkumulieren. Um das zu vermeiden, setzen die meisten Tiere auf maternale Vererbung: Der Embryo behält die Mitochondrien der Mutter und eliminiert fast alle des Vaters kurz nach der Befruchtung. Obwohl mehrere Entsorgungswege bekannt sind — etwa zelluläre Recycling‑Systeme und DNA‑schneidende Enzyme — haben Forscher noch nicht vollständig verstanden, wie subtile chemische Markierungen auf DNA und RNA die Eliminierung väterlicher Mitochondrien beeinflussen könnten.
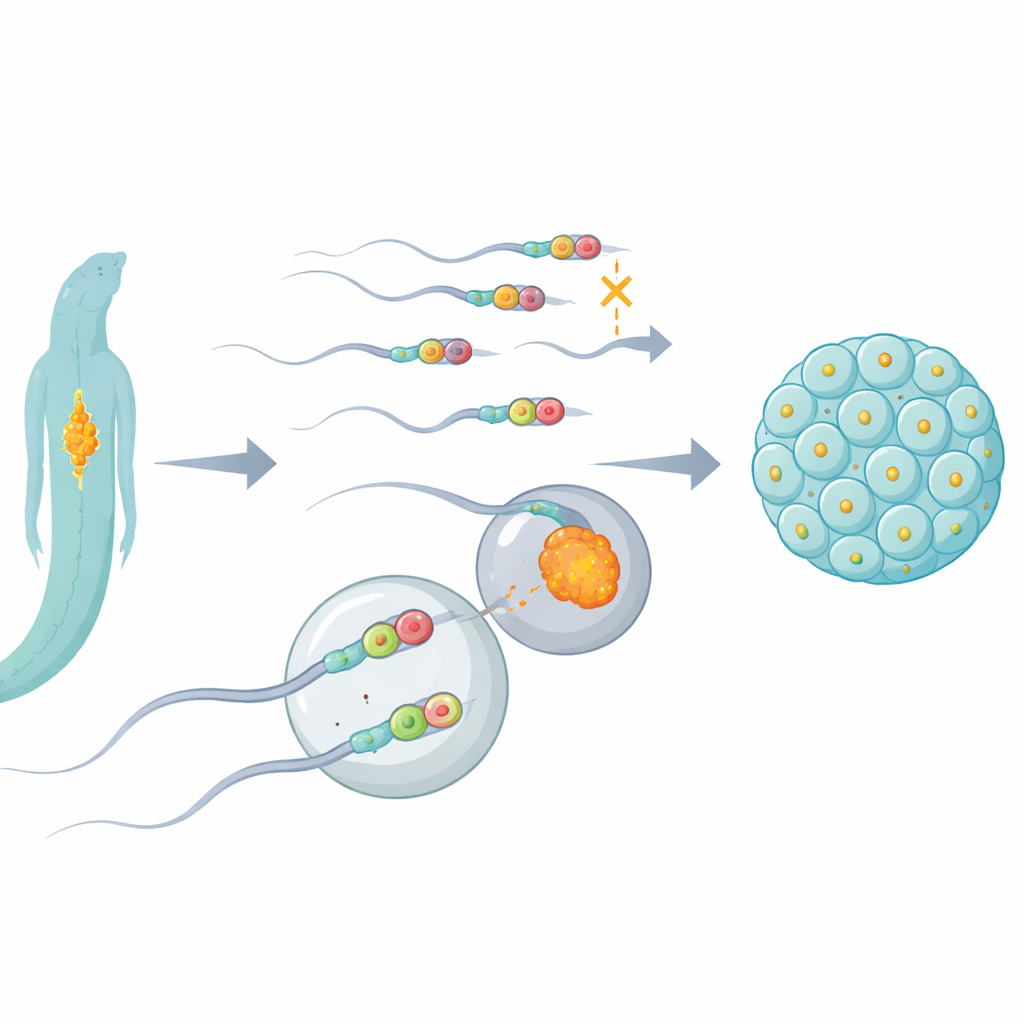
Ein molekularer Radiergummi mit wichtiger Fortpflanzungsaufgabe
Die Forscher konzentrierten sich auf ein Protein namens ALKB‑1 im Nematoden Caenorhabditis elegans, einem Arbeitstier der Genetik. ALKB‑1 ist eine Art molekularer Radiergummi, der Methylgruppen — winzige chemische Markierungen — von DNA und RNA entfernen kann. Durch selektives Ausschalten oder Reduzieren von ALKB‑1 verfolgte das Team, was mit Spermien‑Mitochondrien und deren DNA nach der Befruchtung geschieht. Sie fanden heraus, dass bei Verlust der „Radier“‑Aktivität von ALKB‑1 väterliche Mitochondrien und deren DNA ungewöhnlich lange in sich entwickelnden Embryonen verblieben, anstatt rasch entfernt zu werden. Diese Verzögerung trat hauptsächlich auf, wenn ALKB‑1 in den Spermien fehlte, und ging einher mit Spermien, die ungewöhnlich viele Mitochondrien und mitochondriale DNA enthielten.
Wie das Verändern der tRNA‑Chemie die Mitochondrien durcheinanderbringt
Bei genauerer Untersuchung fragten die Wissenschaftler, für welche chemischen Markierungen ALKB‑1 wirklich wichtig ist. Tests an DNA deuteten darauf hin, dass Veränderungen der DNA‑Methylierung allein das Eliminierungsproblem nicht erklären konnten. Stattdessen richtete sich die Aufmerksamkeit auf tRNAs, kleine Adaptermoleküle, die helfen, genetische Botschaften in Proteine zu übersetzen. Bei normalen Würmern entfernt ALKB‑1 eine spezifische Markierung — genannt m1A — von einer Untergruppe von tRNAs. Ohne ALKB‑1 häuften sich diese Markierungen an. Diese subtile Verschiebung in der tRNA‑Chemie veränderte breitflächig, wie effizient viele Proteine hergestellt wurden: Die Proteinproduktion im Zellplasma stieg, während die Proteinsynthese innerhalb der Mitochondrien schwächte. Das Resultat war eine Diskrepanz zwischen den für Mitochondrien bestimmten Proteinen und dem, was die Organellen bewältigen konnten, was zu Aggregaten schlecht verwalteter Proteine und zu Anzeichen von mitochondrialem Stress führte.
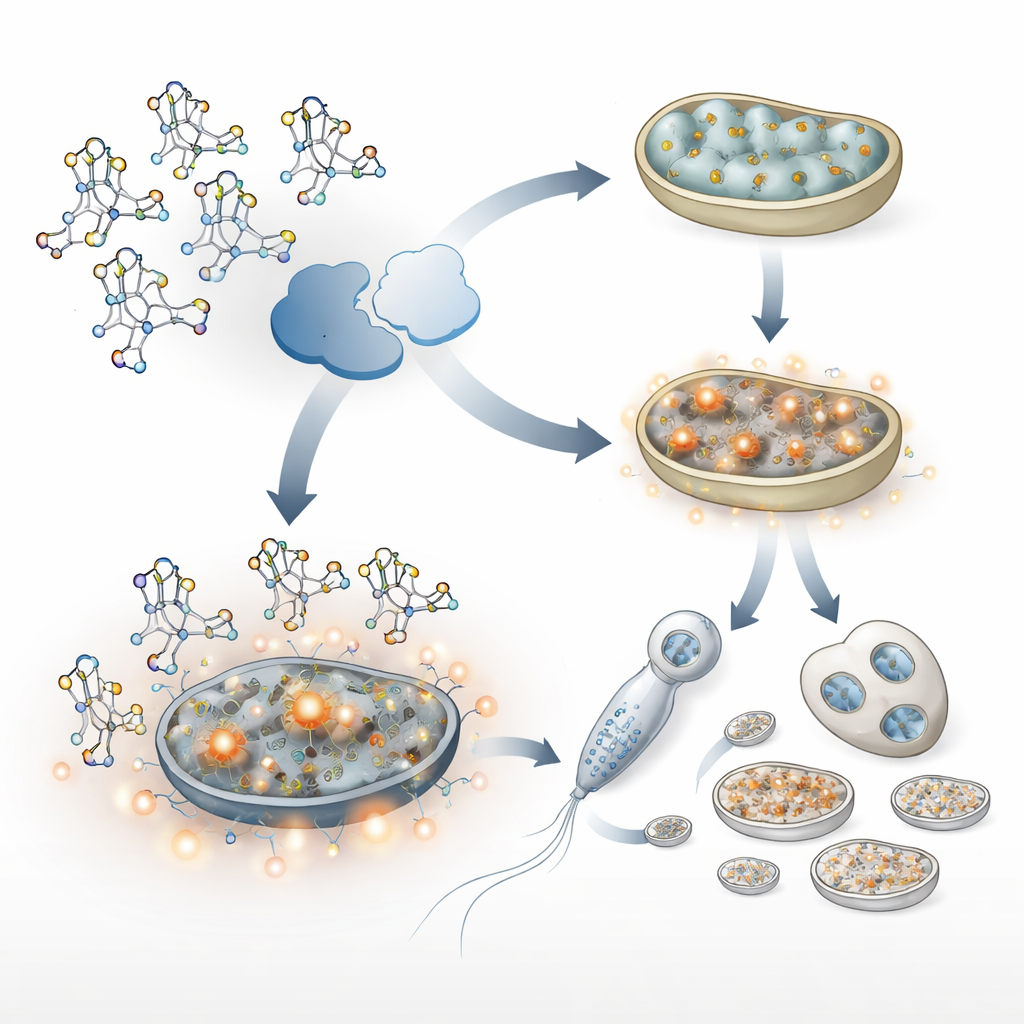
Stresssignale, die schützen — und unbeabsichtigt väterliche Mitochondrien bewahren
Gestresste Mitochondrien produzieren oft mehr reaktive Sauerstoffspezies, chemisch aggressive Stoffwechselnebenprodukte. In den ALKB‑1‑defizienten Würmern stiegen diese reaktiven Moleküle stark an. Das wiederum schaltete zwei wichtige Stress‑Antwortprogramme ein: eines, das von einem Faktor ähnlich dem menschlichen Nrf2 gesteuert wird (bei Würmern SKN‑1 genannt), und ein anderes, bekannt als die mitochondriale unfolded protein response. Gemeinsam steigerten diese Wege die Produktion neuer Mitochondrien und die Vervielfältigung der mitochondrialen DNA, insbesondere in Spermien. Während diese Antwort Zellen hilft, mit Schäden umzugehen, hatte sie auch eine unbeabsichtigte Nebenwirkung: Mehr väterliche Mitochondrien und mitochondriale DNA häuften sich an und waren nach der Befruchtung schwerer zu entfernen. Das Blockieren dieser Stresswege oder die Verringerung oxidativer Schäden mit Antioxidantien stellte die normale Beseitigung väterlicher Mitochondrien weitgehend wieder her.
Wenn das Aufräumen fehlschlägt, leiden Fruchtbarkeit und Embryonen
Die verzögerte Entfernung väterlicher Mitochondrien war nicht nur eine mikroskopische Kuriosität. Männliche Würmer ohne funktionelle ALKB‑1‑Aktivität zeugten weniger Nachkommen, und die von ihnen mitverursachten Embryonen starben häufiger. Ihre Spermien wurden jedoch in normaler Zahl gebildet und sahen strukturell intakt aus, was darauf hindeutet, dass das Hauptproblem in der mitochondriellen Qualitätskontrolle lag und nicht in der Spermienbildung selbst. Die Studie schlägt vor, dass von ALKB‑1 kontrollierte tRNA‑Markierungen als epigenetische Kontrollstelle fungieren: Wenn dieses System funktioniert, bleibt das mitochondriale Proteingleichgewicht erhalten, Stress bleibt kontrolliert und väterliche Mitochondrien werden sicher eliminiert. Führt es zu Versagen, bleiben gestresste und überzählige väterliche Mitochondrien zurück und schädigen Fruchtbarkeit und frühe Entwicklung. Obwohl diese Experimente an Würmern durchgeführt wurden, beleuchten sie ein grundlegendes Prinzip — dass winzige chemische Änderungen an RNA steuern können, wie wir unsere zellulären Kraftwerke vererben, und letztlich die reproduktive Gesundheit komplexerer Tiere, einschließlich des Menschen, beeinflussen könnten.
Zitation: Luo, Z., Li, Y., He, C. et al. ALKB-1-dependent tRNA methylation is required for efficient paternal mitochondrial elimination. Nat Commun 17, 2144 (2026). https://doi.org/10.1038/s41467-026-68813-6
Schlüsselwörter: mitochondriale Vererbung, väterliche Mitochondrien, tRNA‑Methylierung, oxidativer Stress, männliche Fruchtbarkeit