Clear Sky Science · de
Die funktionelle Landschaft des alternativen Spleißens bei der hämatopoetischen Linienentscheidung
Wie winzige Genbearbeitungen unser Blut formen
Sekündlich stellt Ihr Körper Millionen neuer Blutzellen her. Hinter diesem stillen Wunder steht ein molekulares Bearbeitungssystem, das genetische Nachrichten Stück für Stück ausschneiden und wieder zusammenfügen kann und so leicht unterschiedliche Versionen desselben Proteins erzeugt. Diese Studie untersucht, wie dieser Bearbeitungsprozess, genannt alternatives Spleißen, unreife Stammzellen dabei unterstützt, sich zu roten Blutkörperchen, weißen Blutkörperchen oder anderen Blutzelltypen zu entwickeln – und was passiert, wenn ein einzelnes, herausgeschnittenes Stück fehlt.
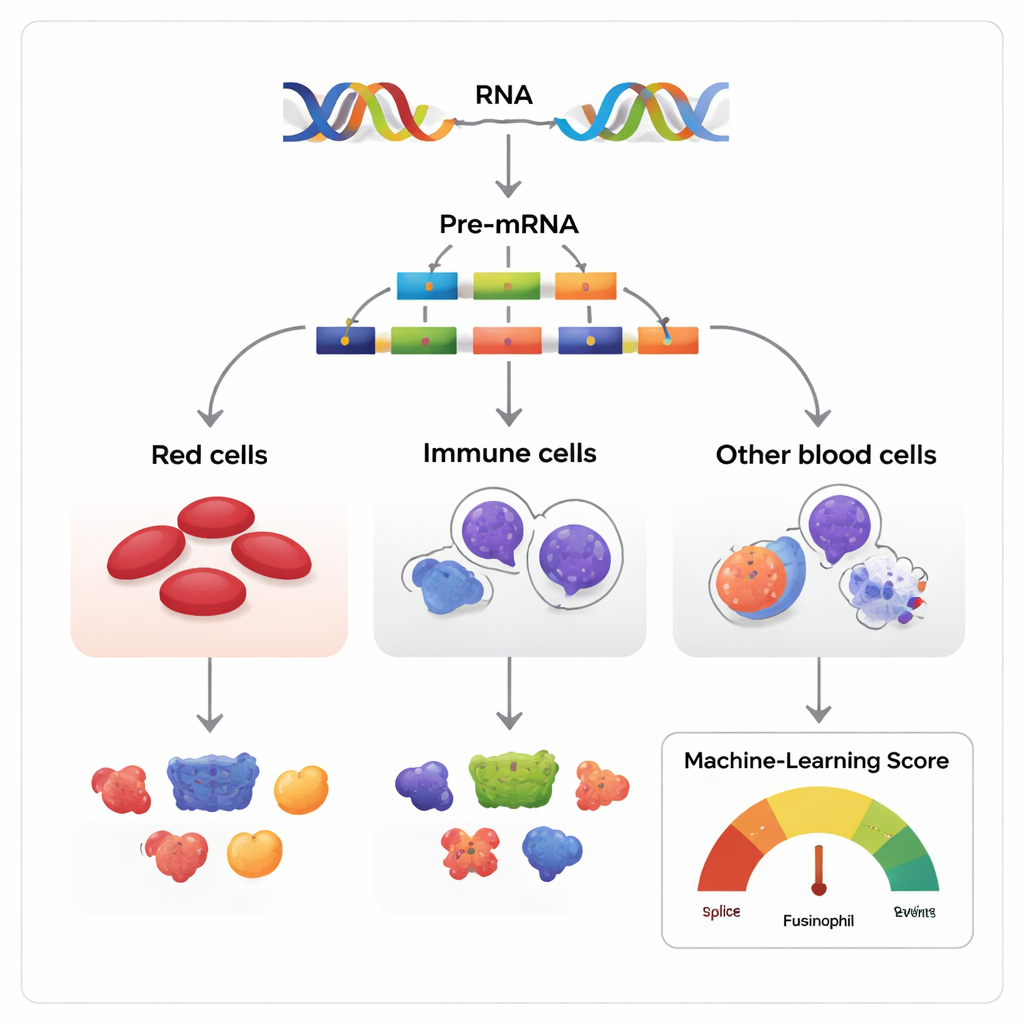
Viele Varianten aus demselben genetischen Text
Gene werden oft als Baupläne beschrieben, sind in Wirklichkeit aber eher wie Drehbücher, die umgestellt werden können. Wenn ein Gen gelesen wird, enthält die anfängliche RNA-Kopie Segmente, sogenannte Exons, die vor der endgültigen Übersetzung in Protein behalten oder ausgelassen werden können. Die Autoren betrachteten diesen Prozess, bekannt als Exon-Skipping, in blutbildenden Geweben von Menschen, Mäusen und mehreren anderen Wirbeltieren. Sie haben mehr als 270 RNA-Datensätze zusammengetragen, die gemeinsam zeigen, wie Blutstamm- und Vorläuferzellen reifen und sich in drei große Linien differenzieren: erythroid (rotzellbildend), myeloid (infektionsbekämpfend) und lymphoid (antikorperproduzierend).
Bewertung: Welche Spleißänderungen wirklich wichtig sind
Da die meisten Gene mit mehreren Exons auf viele Arten gespleißt werden können, besteht die zentrale Herausforderung darin, harmlose Varianten von solchen zu unterscheiden, die tatsächlich die Zellschicksale beeinflussen. Die Forscher entwickelten ein maschinelles Lernmodell, den Functional AS Score (FAScore), um dieses Problem anzugehen. Für jedes Exon-Skipping-Ereignis berücksichtigt das Modell 19 Informationen, etwa wie stark dessen Nutzung während der Zellentwicklung verändert ist, wie gut die umgebende DNA über Arten hinweg konserviert ist, ob es bekannte Proteindomänen verändert und ob es Stellen für chemische Modifikationen des Proteins enthält. Der Algorithmus, trainiert mit einer positive–unlabeled-Strategie und einem Random-Forest-Klassifikator, liefert einen Wert zwischen 0 und 1, der angibt, wie wahrscheinlich es ist, dass ein bestimmtes Spleißereignis eine funktionelle Auswirkung hat.
Konservierte, linien-spezifische Schalter finden
Bei Anwendung des FAScore auf Zehntausende von Exon-Skipping-Ereignissen klassifizierte das Team diese in wahrscheinlich funktionelle, nicht-funktionelle oder unsichere Gruppen. Ereignisse, die als funktionell vorhergesagt wurden, traten häufiger in Proteinregionen auf, die wichtig für Interaktionen sind, in evolutionär konservierten Sequenzen und in Segmenten, die chemische Markierungen wie Phosphorylierung oder SUMOylierung tragen. Viele dieser Ereignisse waren außerdem nur in bestimmten Blutlinien oder während der fetalen Blutbildung aktiv, was darauf hindeutet, dass sie als fein abgestimmte Schalter in bestimmten Entwicklungsfenstern wirken. Die Studie zeigte ferner, dass einige der ältesten Spleißereignisse — solche, die über Hunderte Millionen Jahre bei Wirbeltieren erhalten sind — besonders wahrscheinlich funktionell sind, analog dazu, dass ältere Gene oft zentrale biologische Rollen tragen.
Experimenteller Beweis: Steuerung der Blutzellprodukte
Um die Vorhersagen des Modells zu überprüfen, wählten die Autoren mehrere hoch bewertete Exons in Genen aus, die in verschiedenen Blutlinien aktiv sind, und entfernten diese Exons in murinen Blutstamm- und Vorläuferzellen mittels CRISPR. Die Ergebnisse stimmten mit den Modellvorhersagen überein: Das Entfernen bestimmter Exons in den Genen KLF6 und SSBP3 beeinträchtigte die Bildung myeloider Kolonien, ohne die Produktion roter Zellen zu schädigen, während das Löschen von Exons in EPB41L1 und TBC1D23 die Bildung erythroidaler Kolonien veränderte. Insbesondere führte das Überspringen von Exon 15 in TBC1D23 bei Mäusen und Zebrafischen zu einer reduzierten Produktion roter Vorläuferzellen, wodurch weniger zirkulierende rote Zellen und niedrigere Hämoglobinwerte entstanden, während die weißen Blutkörperchen weitgehend verschont blieben.
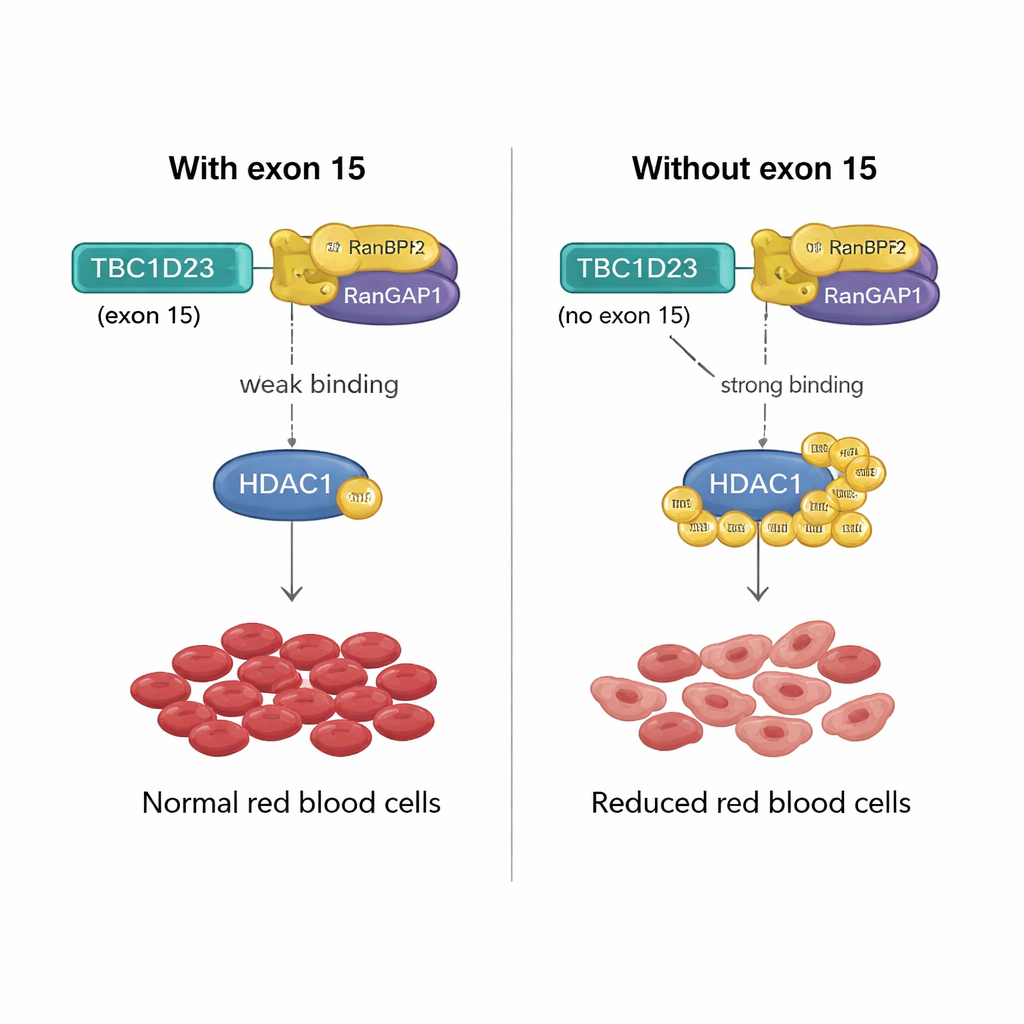
Ein molekularer Hebel für die Produktion roter Blutkörperchen
Wie kann ein 15 Aminosäuren langer Abschnitt, der von Exon 15 des TBC1D23 kodiert wird, einen solchen Effekt haben? Das Team fand heraus, dass die Einbeziehung dieses Exons die Bindung von TBC1D23 an ein Proteinpaar namens RANBP2/RANGAP1 schwächt, das zusammenarbeitet, um SUMO-Marker an andere Proteine anzuhängen. Ohne Exon 15 bindet TBC1D23 dieses Paar stärker, was die SUMOylierung eines Schlüsselenzyms, HDAC1, verstärkt. Diese verstärkte Markierung verändert die Aktivität vieler Transkriptionsfaktoren — der Hauptregulatoren der Genexpression — und bringt die Genprogramme durcheinander, die für die korrekte Reifung roter Blutkörperchen nötig sind. Als die Forscher eine Version von HDAC1 konstruierten, die an zwei entscheidenden Positionen nicht SUMO-modifiziert werden kann, stellte dies die Bildung roter Zellen in Zellen ohne TBC1D23-Exon 15 wieder her und bestätigte, dass diese chemische Markierung der kritische Schritt ist.
Warum das für Gesundheit und künftige Therapien wichtig ist
Für Nichtfachleute lautet die Botschaft dieser Arbeit: Nicht alle genetischen Veränderungen sind gleichwertig – manchmal entscheidet das Beibehalten oder Auslassen eines winzigen Genabschnitts im Endprodukt über gesunde Blutbildung oder Anämie. Durch die Kombination groß angelegter RNA-Daten mit einem ausgefeilten Bewertungssystem liefert die Studie eine Landkarte, um zu erkennen, welche Spleißvarianten am ehesten die Entscheidungen von Stammzellen beeinflussen. Dieser Ansatz vertieft nicht nur unser Verständnis der Blutbildung in Gesundheit und Krankheit, sondern bietet auch eine allgemeine Strategie, um wichtige Spleißereignisse in anderen Organen zu identifizieren und damit potenziell künftige gentherapiegestützte und präzisionsmedizinische Behandlungen zu informieren.
Zitation: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Schlüsselwörter: alternatives Spleißen, Hämatopoese, maschinelles Lernen, rote Blutkörperchen, Genregulation