Clear Sky Science · de
Strukturelle Grundlage der Transkriptionsregulation durch den Zellteilungsregulator MraZ in Mycoplasma genitalium
Wie ein winziges Bakterium steuert, wann es sich teilt
Jede lebende Zelle muss entscheiden, wann sie sich in zwei Teile teilt, und diese Entscheidung kann über gesundes Wachstum oder unkontrollierte Infektion entscheiden. Diese Studie blickt in eines der einfachsten bekannten Bakterien, Mycoplasma genitalium, und zeigt auf atomarer Ebene, wie ein einziges Protein, MraZ genannt, an die DNA bindet und zentrale Zellteilungs-Gene an- oder ausschaltet. Durch das Verständnis dieses minimalistischen Kontrollsystems hoffen Wissenschaftler, allgemeine Regeln bakteriellen Wachstums zu entschlüsseln, die eines Tages neue Antibiotikakonzepte oder synthetische „Minimierzellen“ inspirieren könnten.
Eine reduzierte Zelle mit großen Lehren
Mycoplasma genitalium ist für sein winziges Genom bekannt: nur ein Bruchteil der DNA, die in häufigen Bakterien wie E. coli vorkommt. Diese geringe Größe macht es zu einem aussagekräftigen Modell, um herauszufinden, welche Gene und Regulationssysteme wirklich lebenswichtig sind. Viele Bakterien bündeln ihre Zellteilungs- und Zellwand-Gene in einem Block, dem sogenannten dcw-Cluster. In wandlosen Mycoplasmen sind die meisten dieser Gene verschwunden, doch einige wenige bleiben erhalten, darunter mraZ ganz an der Spitze des Clusters. MraZ fungiert wie ein Verkehrspolizist und kontrolliert die Aktivität seiner Nachbar-Gene, die wiederum beeinflussen, wie und wann die Zelle sich teilt.
Ein wiederkehrendes DNA-Muster als Schaltstelle
Unmittelbar stromaufwärts des mraZ-Gens entdeckten die Forschenden eine stark konservierte DNA-Region, die als Andockstelle für das MraZ-Protein dient. Dieser Abschnitt enthält vier kurze, wiederholte Segmente oder „Boxen“, deren Sequenz bei vielen bakteriellen Arten nahezu identisch ist. Durch gezielte Mutationen einer, zweier oder mehrerer dieser Boxen und anschließende Messung der verbleibenden Bindestärke von MraZ zeigte das Team, dass das Protein kooperativ bindet: jede Box verstärkt den Gesamthalt. Reporter-Experimente mit einem fluoreszenten Marker bestätigten, dass je stärker diese Boxen gestört waren, desto weniger wirksam MraZ die Genaktivität unterdrücken konnte, was ihre Bedeutung als fein abgestimmtes Kontrollfeld unterstreicht. 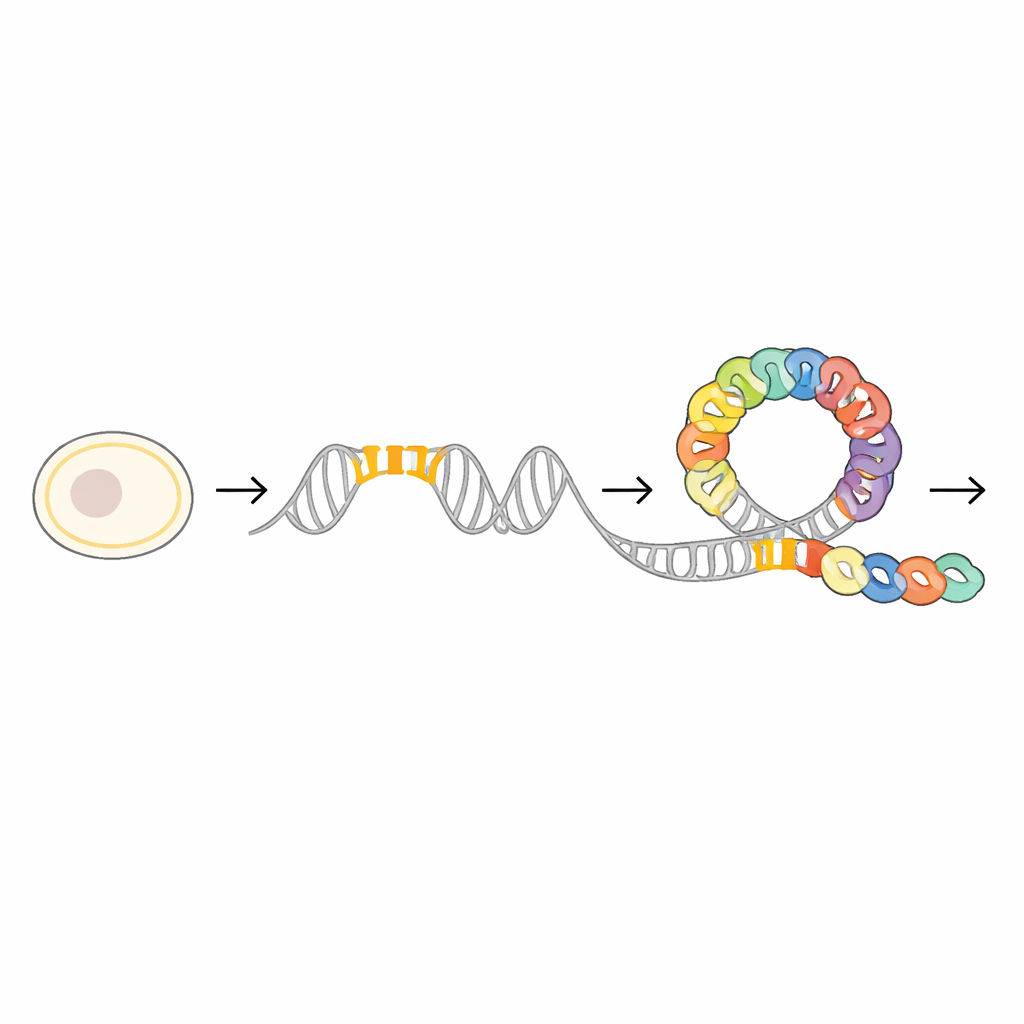
Ein ringförmiges Protein, das sich öffnet, um die DNA zu umschließen
Um zu verstehen, wie dieses Kontrollfeld auf atomarer Ebene funktioniert, nutzten die Forschenden Kryo-Elektronenmikroskopie und Röntgenkristallographie, um mehrere dreidimensionale Strukturen von MraZ allein und an DNA gebunden zu lösen. Alleinstehende MraZ-Moleküle fügen sich zu ringförmigen Assemblierungen aus acht oder neun identischen Untereinheiten zusammen. Diese Ringe besitzen eine charakteristische „wiegeartige“ Oberfläche, gebildet durch eine kleine Beta-Faltblatt-Struktur, anders als die spiraligen Helices, die oft bei DNA-bindenden Proteinen vorkommen. Trifft MraZ auf sein DNA-Segment mit vier Boxen, setzt sich der Ring nicht einfach auf die Helix; vielmehr klappt er auf und reorganisiert sich so, dass vier seiner Untereinheiten entlang der DNA ausgerichtet sind, wobei jede eine Box in der Hauptfurche umschließt.
Wichtige Kontaktpunkte, die den DNA-Code lesen
Die hochaufgelösten Strukturen zeigten, dass jede DNA-kontaktierende Untereinheit drei positiv geladene Seitenketten nutzt — spezifische Punkte auf der Proteinoberfläche — um die DNA-Sequenz zu lesen. Diese chemischen „Finger“ reichen in die Furche der Doppelhelix und bilden präzise Wasserstoffbrücken mit bestimmten Basenpaaren in den konservierten Boxen. Wenn die Forschenden eine dieser drei Aminosäurereste veränderten, verlor MraZ weitgehend seine Fähigkeit, an die DNA zu binden und den Test-Reporter zu unterdrücken. Zusätzliche Kontakte zum DNA-Rückgrat stabilisieren den Komplex, sind aber weniger sequenzspezifisch. Zusammen zeigen diese Befunde, wie MraZ einen hochspezialisierten Lesekopf mit einem flexiblen Mehruntereinheitskörper kombiniert, um seine Zielregion zu erkennen. 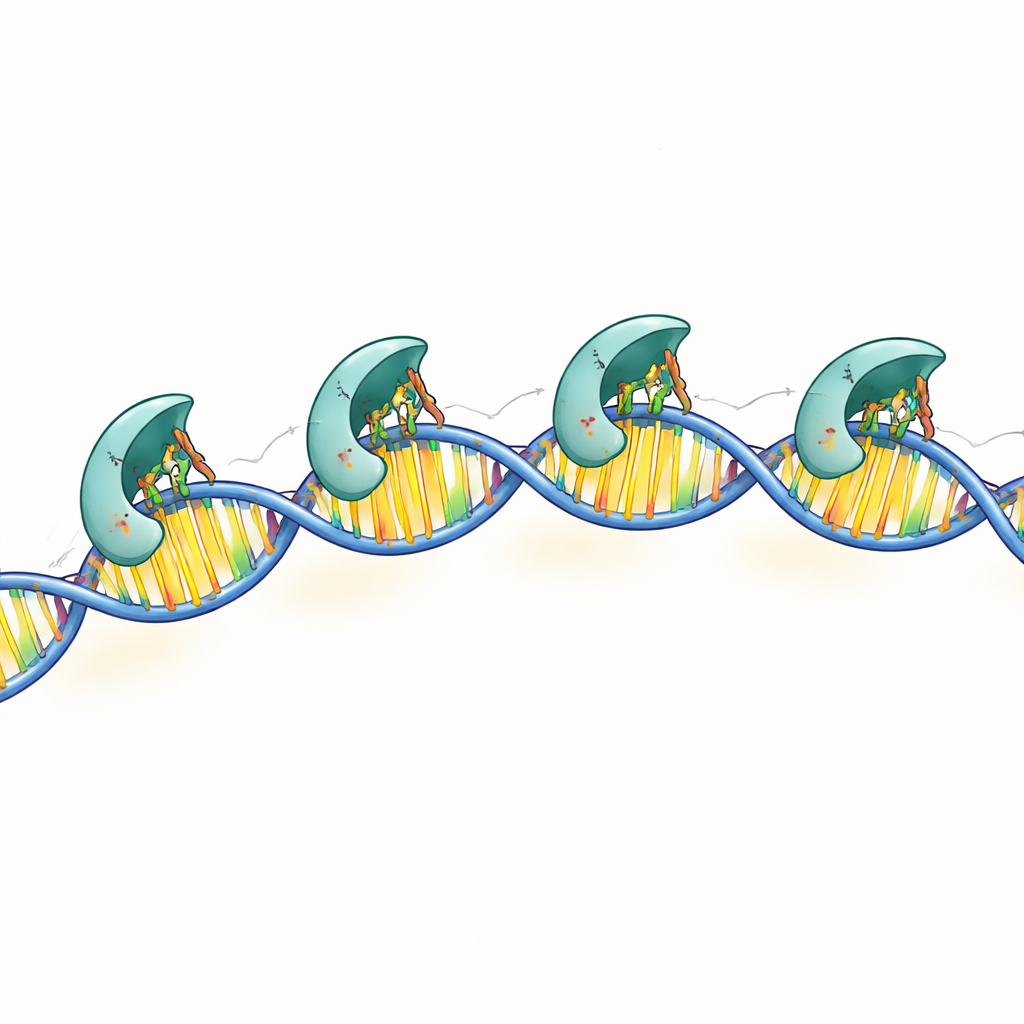
Oligomere, die die Stärke der Kontrolle feinjustieren
Da MraZ Ringe und andere Mehrfachstrukturen bildet, untersuchte das Team, ob dieses Zusammenlagerungs-Verhalten für die DNA-Bindung erforderlich ist oder sie nur feinabstimmt. Durch Konstruktion einer MraZ-Variante, die sich nicht mehr zu Ringen zusammenlagern konnte, fanden sie heraus, dass das Protein die vier-Box-DNA-Sequenz weiterhin band, jedoch mit geringerer Affinität. Diese monomere Form hatte besonders dann Schwierigkeiten, wenn der Abstand zwischen den Boxen verändert wurde, was darauf hindeutet, dass das vollständige Oligomer hilft, entfernte Boxen zu überbrücken und auszurichten und so die lokale Konzentration von Bindungsstellen entlang der DNA erhöht. Die Autoren schlagen ein dynamisches Modell vor, in dem MraZ zwischen einem geschlossenen Ring und einer offenen, DNA-gebundenen Form umschaltet und seinen Assemblierungszustand als Stellrad nutzt, um die Stärke der Repression am Promotor zu regulieren.
Was das für Bakterien und darüber hinaus bedeutet
Kurz gesagt erklärt diese Arbeit, wie ein kleines Protein in einem minimalen Bakterium ein wiederkehrendes Muster auf der DNA ergreift und als Hauptschalter für Zellteilungs-Gene nutzt. Die Kombination aus einem wiegenartigen Lesekopf und einem flexiblen Ringkörper ermöglicht es MraZ, sein Ziel mit großer Präzision zu erkennen und zugleich an unterschiedliche DNA-Anordnungen angepasst zu bleiben. Da ähnliche Proteine und DNA-Motive in vielen Bakterien vorkommen, ist der hier aufgedeckte Mechanismus wahrscheinlich eine gemeinsame Strategie zur Koordination von Wachstum und Teilung. Erkenntnisse aus diesem reduzierten System können Forschern helfen, schlanke genetische Schaltungen in synthetischen Zellen zu entwerfen und langfristig zu neuen Ansätzen führen, bakterielles Wachstum in Krankheiten zu stören.
Zitation: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Schlüsselwörter: bakterielle Zellteilung, DNA–Protein-Interaktion, transkriptionelle Regulation, Kryo-Elektronenmikroskopie, Mycoplasma genitalium