Clear Sky Science · de
Zelluläre und transkriptionelle Bahnen der neuronalen Schicksalsbestimmung bei Seeanemonen decken zwei Modi der adulten Neurogenese auf
Wie ein einfaches Meereswesen ständig neue Gehirnzellen bildet
Die meisten Tiere, einschließlich des Menschen, bilden den Großteil ihrer Neuronen früh im Leben und hören danach größtenteils auf. Einige vermeintlich einfache Lebewesen, wie Seeanemonen, fügen jedoch ihr Leben lang weiterhin neue Nervenzellen hinzu. Diese Studie untersucht, wie die Sternenanemone (Nematostella vectensis) ihr diffus angelegtes Nervensystem dauerhaft erneuert und umformt, und zeigt Strategien, die uralte Lösungen für Wachstum und Reparatur von Nervensystemen widerspiegeln könnten.
Ein wachsender Körper braucht ein wachsendes Nervennetz
Seeanemonen haben kein Gehirn; stattdessen besitzen sie ein netzartiges Nervennetz, das sich durch die Körperwand zieht. Wenn diese Tiere je nach Nahrungsverfügbarkeit wachsen oder schrumpfen, muss sich auch ihr Nervennetz entsprechend vergrößern oder verkleinern. Mithilfe eines lichtempfindlichen fluoreszenten Proteins als Zeitstempel markierten die Autor:innen bestehende Neuronen bei jungen Erwachsenen und verfolgten danach neu entstandene Zellen, die innerhalb der folgenden Woche auftraten. Sie fanden zahlreiche neue Neuronen entlang der Körperachse verstreut, nicht auf eine spezielle Wachstumszone beschränkt. Diese frischen Zellen traten sowohl am mundseitigen als auch am gegenüberliegenden Ende des Tiers auf, was zeigt, dass adulte Neurogenese räumlich weit verbreitet und anhaltend ist.
Die Herkunft neuer Nervenzellen nachverfolgen
Um herauszufinden, woher diese neuen Neuronen stammen, kombinierten die Forschenden Live-Imaging mit Einzelzell-RNA-Sequenzierung, einer Technik, die abliest, welche Gene in tausenden einzelnen Zellen aktiv sind. Sie konzentrierten sich auf Zellen mit fluoreszenten „Reportern“, die von drei Schlüsselngenen gesteuert werden: FoxL2, SoxC und Elav. FoxL2 markiert einen breiten Pool teilender, multipotenter Vorläuferzellen; SoxC wird kurz eingeschaltet, wenn Zellen zu spezialisieren beginnen; und Elav ist in peptidergenen Neuronen stark aktiv, die hauptsächlich über kleine Signalpeptide kommunizieren. Das Team zeigte, dass eine Population von FoxL2-positiven, Piwi1-positiven Vorläuferzellen sich wie Stammzellen verhält: Sie erneuern sich selbst und erzeugen gleichzeitig kontinuierlich vielfältige Nachkommen, darunter Neuronen, die als Cnidocyten bekannten Nesselkapselzellen und sekretorische Zellen. SoxC und Elav hingegen leuchten erst auf, wenn Zellen diesen Vorläuferpool verlassen und sich bestimmten neuronalen Schicksalen verpflichten.
Zwei verschiedene Wege zu adulten Neuronen
Durch Abgleich der Reporter-Zeitpunkte mit dem Genexpressionsprofil jeder Zelle deckte die Studie zwei unterschiedliche Wege zu reifen neuronalen Zellen auf. Peptidergene Neuronen folgen einem direkten Pfad: Sie entstehen aus Vorläufern, die bereits ein "peptidergisch verpflichtetes" molekulares Profil tragen, und differenzieren dann rasch in eine Vielfalt von Neuronentypen. Neue Mitglieder jedes Subtyps erscheinen proportional zu ihrer bereits vorhandenen Häufigkeit, was nahelegt, dass das System eine ausgeglichene Mischung von Neurontypen erhält, statt bestimmte Typen zu bevorzugen. In dieser Linie gibt es keine klare Serie zwischengeschalteter Stationen; stattdessen entstehen eng verwandte Neuronensubtypen parallel aus ähnlich primten Vorläuferzellen. 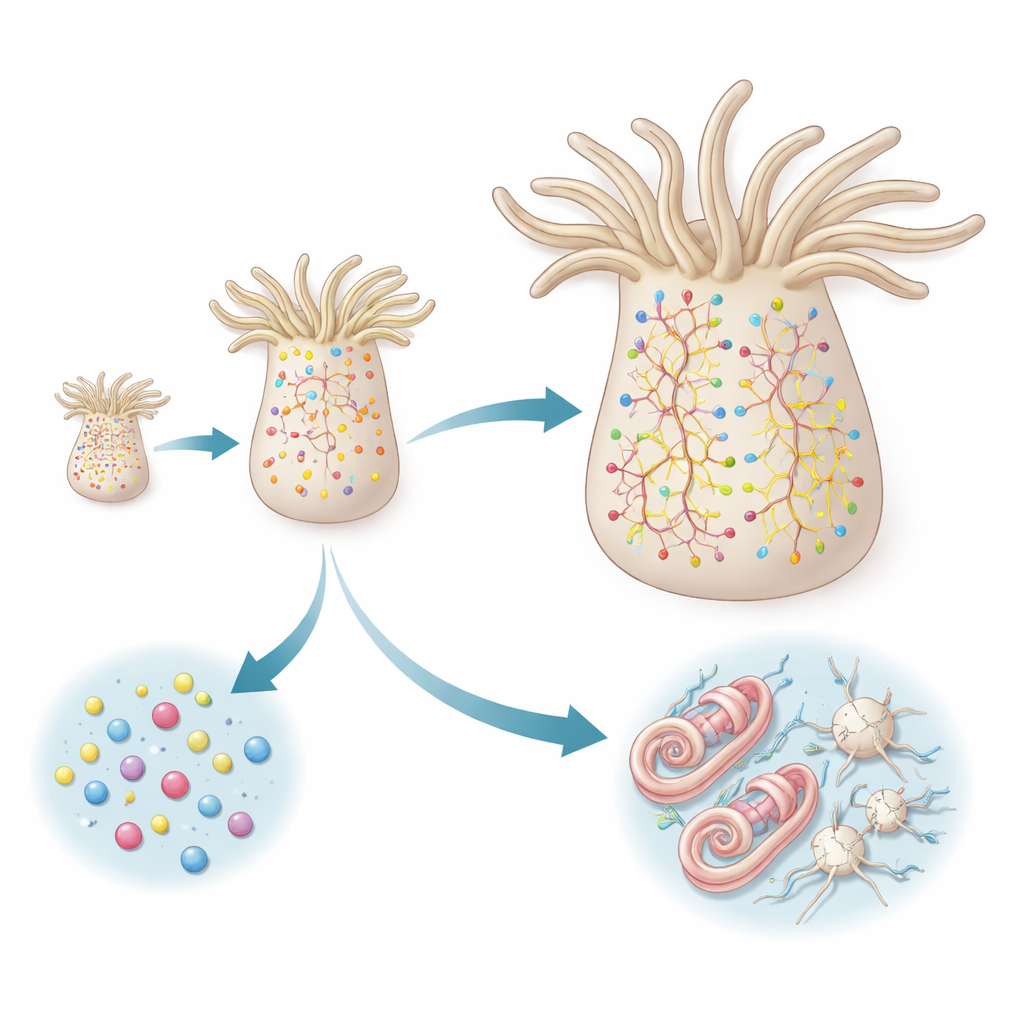
Der Sonderfall der Nesselkapselzellen
Cnidocyten, die für Cnidaria charakteristischen Nesselkapselzellen, nehmen einen schrittweisen Weg. Sie durchlaufen zunächst eine "Kapselaufbau"-Phase, in der sie ihre charakteristischen unter Druck stehenden Organellen herstellen, die ein mikroskopisches Harpunenprojektile abfeuern können. Diese Phase beruht auf einem spezifischen Satz regulatorischer Gene und Strukturproteine, die in anderen Zelltypen weitgehend fehlen. Erst nachdem dieses Zwischenprogramm abgeschlossen ist, schalten Cnidocyten ein zweites, eher konventionelles neuronales Programm ein und fügen Ionenkanäle und andere Komponenten hinzu, die für elektrische Signalisierung erforderlich sind. Genetische Daten aus Mutanten, die in der frühen Phase steckenbleiben, untermauern dieses Zwei-Phasen-Modell: Wird der Übergang blockiert, erscheinen die späteren neuronalen Merkmale nicht. 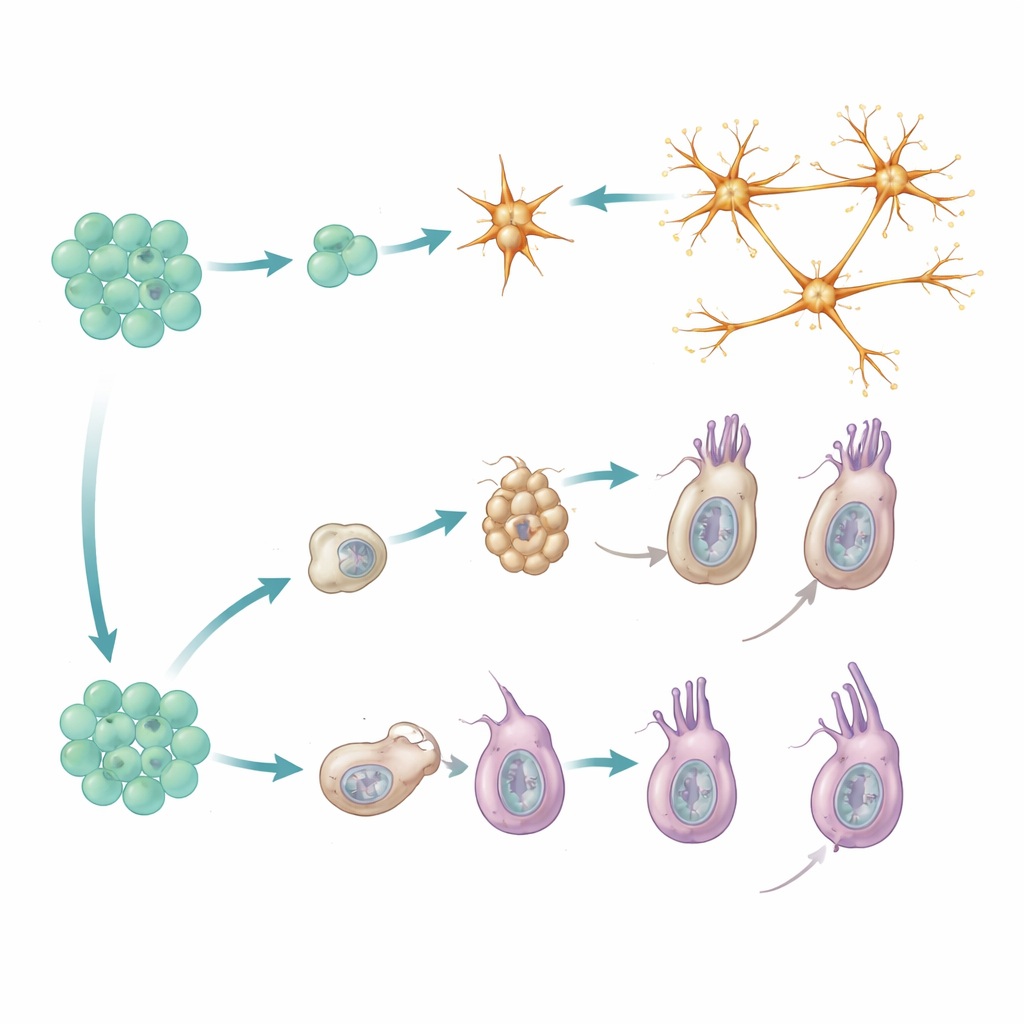
Geteilte Regeln und uralte Wurzeln
Trotz ihrer unterschiedlichen Wege stützen sich peptidergene Neuronen und Cnidocyten auf überlappende Familien regulatorischer Gene, um ihre Identitäten festzulegen. Breite neuronale Merkmale sind mit bHLH- und bZIP-Transkriptionsfaktoren assoziiert, während die fein abgestimmte Identität jedes Neuronensubtyps durch einzigartige Kombinationen von Homeodomain- und Zinkfinger-Genen spezifiziert wird — ein "Code", der an die Definition von Neuronentypen in komplexeren Tieren, einschließlich Würmern und Wirbeltieren, erinnert. Die Autor:innen argumentieren, dass diese modularen Strategien — stammzellähnliche Vorläufer, vorübergehende SoxC-Aktivität während der Festlegung und subtypebestimmende Homeodomain-Codes — tief konservierte Prinzipien der Neurogenese repräsentieren könnten. Bei Seeanemonen unterstützen sie die lebenslange Erneuerung und Skalierung des Nervennetzes; bei anderen Tieren könnten verwandte Mechanismen sowohl begrenzte adulte Neurogenese als auch die bemerkenswerten regenerativen Fähigkeiten mancher Linien zugrunde liegen.
Zitation: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Schlüsselwörter: adulte Neurogenese, Seeanemone, neuronale Vorläuferzellen, Cnidocyten, Einzelzell-Transkriptomik