Clear Sky Science · de
Vergleichende Multi-Omik-Analyse zeigt konservierte und abgeleitete Mechanismen der Flossen- und Gliedmaßenregeneration
Warum das Nachwachsen verlorener Körperteile wichtig ist
Viele Tiere können verlorene Körperteile nachbilden, von Echsenschwänzen bis zu Salamandergliedmaßen. Zu verstehen, wie sie das tun, ist mehr als reine Neugier: Dieselben Regeln, die einem Fisch erlauben, eine Flosse wiederaufzubauen, oder einem Salamander, ein Bein zu ersetzen, könnten eines Tages neue Behandlungen für schwere Verletzungen beim Menschen inspirieren. Diese Studie vergleicht verschiedene Tiere, die außergewöhnlich gut regenerieren können, und blickt tief in ihre Zellen, um herauszufinden, welche Reparaturtricks alt und gemeinsam sind und welche neuere Erfindungen darstellen.
Verschiedene Tiere, verschiedene Gliedmaßen, dieselbe große Frage
Die Forschenden konzentrierten sich auf drei Arten: den Axolotl, der ganze Gliedmaßen nachbilden kann; den weit verbreiteten Zebrafisch, bekannt für seine Flossenreparatur; und Polypterus, einen primitiven Strahlenflosser, der nicht nur die dünnen äußeren Flossenstrahlen regenerieren kann, sondern die gesamte Flosse, einschließlich innerer Knochen und Muskeln. Durch den Vergleich dieser Tiere fragte das Team, ob es ein gemeinsames „Werkzeugset“ zum Wiederaufbau komplexer Körperteile gibt, das bis in die frühe Wirbeltierentwicklung zurückreicht. Sie nutzten moderne genomische Methoden, die ablesen, welche Gene in Tausenden einzelner Zellen aktiv sind, und abbilden, wo diese Zellen im Gewebe liegen.
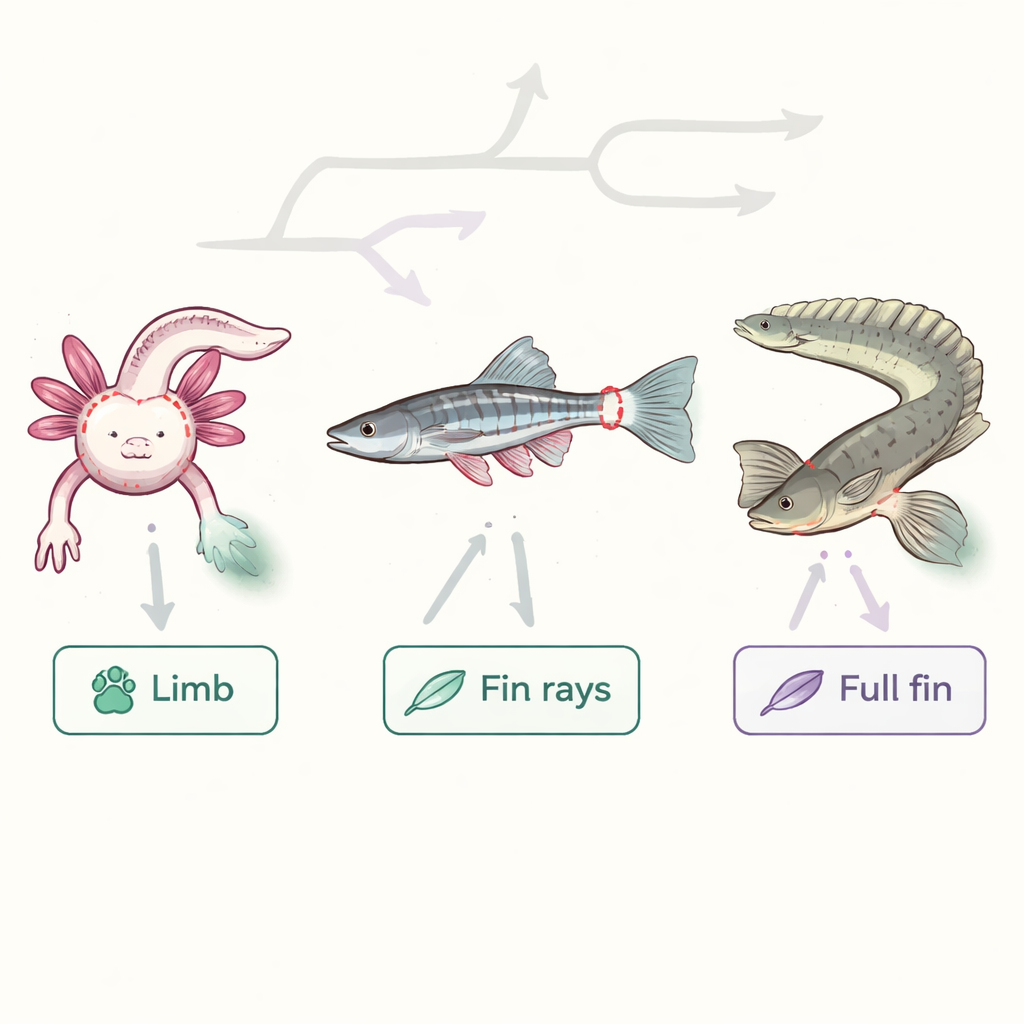
Die Zellen einer nachwachsenden Flosse kartieren
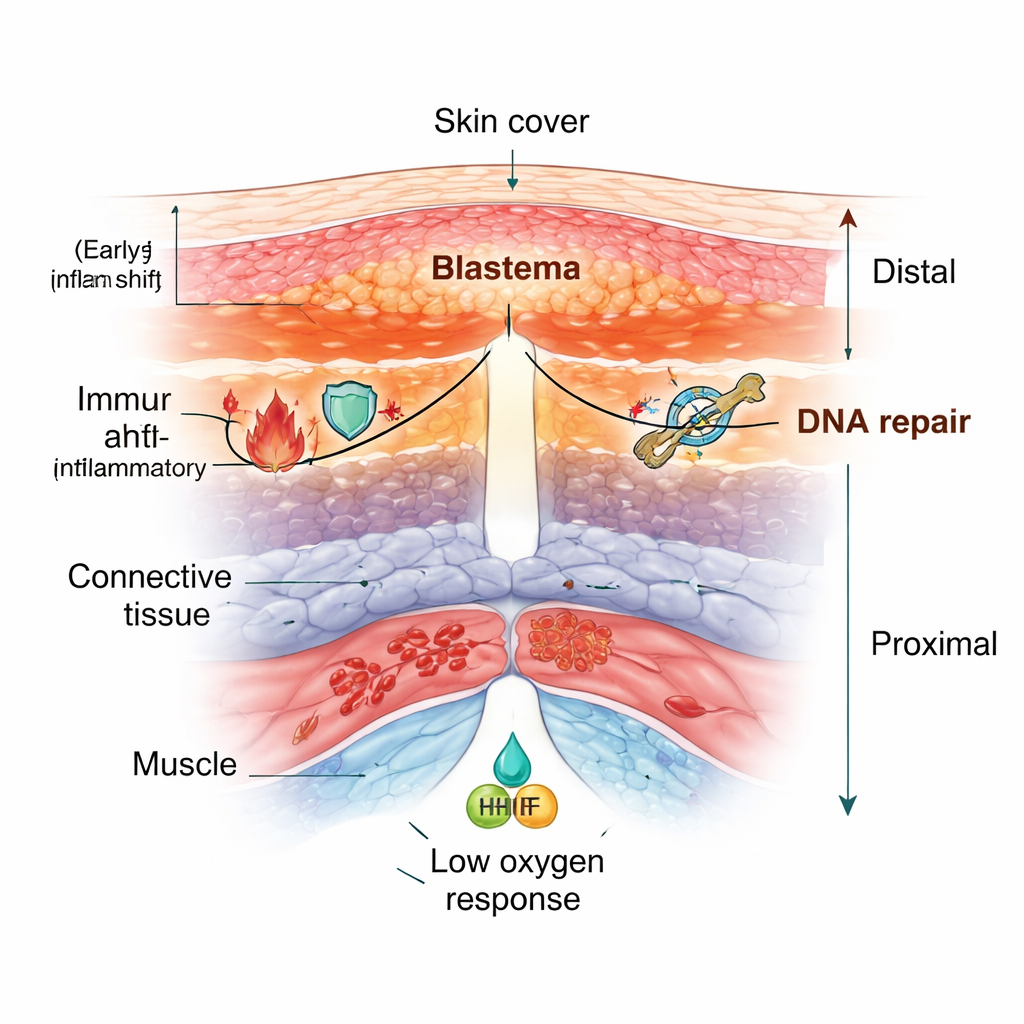
Bei Polypterus entnahmen die Wissenschaftler Proben der Flossen vor der Verletzung und an mehreren Tagen nach der Amputation. Sie fanden mehr als dreißig unterschiedliche Zellgruppen, darunter verschiedene Hautschichten, Immunzellen, Blutgefäße, Muskel-, Bindegewebszellen und teilende „Blastema“-Zellen – die Zellmasse, die das neue Wachstum antreibt. Während die Flosse heilte, wichen ruhende adulten Gewebe einer aktiven Reparaturzone: Immunzellen strömten ein, die Haut verdickte sich zu einer spezialisierten Wundabdeckung, und Bindegewebszellen bewegten sich zum Schnittbereich, um das Blastema zu bilden. Ähnliche Muster zeigten sich bei der Untersuchung von Axolotl-Gliedmaßen und Zebrafisch-Flossen, was darauf hinweist, dass dieses Umverteilen von Zelltypen ein gemeinsames Merkmal der Anhängselregeneration ist.
Alte Baupläne und neue Varianten
Ein genauerer Blick zeigte, dass die wachende Spitze nicht einheitlich ist. Sowohl in Polypterus-Flossen als auch in Axolotl-Gliedmaßen teilte sich das Bindegewebe unter der Wundhaut entlang der Länge der Gliedmaße in zwei Zonen: eine distale Region nahe der Spitze, reich an schnell teilenden, matrixproduzierenden Fibroblasten, und eine proximalere Region näher am Körper mit Zellen, die eher stabilisierende, kontraktile Stützfunktionen haben. Die Haut über der Wunde reaktivierte zudem ein genetisches Programm, das normalerweise in Embryonen zum Aufbau des „apikalen Ektodermalrands“ verwendet wird, eines Signalstreifens, der für das Gliedmaßenwachstum entscheidend ist. Dieses Programm tauchte sowohl in der Wundhaut als auch im angrenzenden Bindegewebe auf, was darauf hindeutet, dass die Regeneration bei Erwachsenen alte Entwicklungsanweisungen wiederverwendet, diese aber über mehrere Gewebe verteilt.
Stresssignale, Sauerstoffregulierung und der Immunumschalter
Über die Arten hinweg zeigten verletzte Flossen und Gliedmaßen eine starke Aktivierung von Genen zur DNA-Schädigungserkennung und -reparatur, als würden die Zellen ihr Genom überprüfen und reparieren, bevor sie in die intensive Wachstumsphase eintreten. Die Immunantwort folgte ebenfalls einem ähnlichen Muster: Eine frühe Welle proinflammatorischer Signale half, beschädigtes Gewebe zu räumen, gefolgt von einem Anstieg antiinflammatorischer Signale, die den Wiederaufbau anstatt Narbenbildung förderten. Ein weiteres gemeinsames Thema war eine „Niedrig-Sauerstoff“-Reaktion. Zellen stabilisierten hypoxieempfindliche Faktoren und steigerten Gene, die die Glykolyse unterstützen, einen Stoffwechselweg, der auch bei Sauerstoffknappheit funktioniert. Bei Polypterus und Axolotl gab es außerdem eine auffällige Zunahme roter Blutkörperchen in der Nähe der Verletzung, die eine spezielle, sauerstoff-sensible Genvariante trugen, was nahelegt, dass Blutzellen helfen könnten, die Heilungsumgebung abzustimmen. In Polypterus und Zebrafisch schaltete sogar die Wundhaut ein Myoglobin-Gen ein – normalerweise in Muskeln zu finden –, das während des Nachwachsens helfen könnte, Sauerstoff und schädliche reaktive Moleküle abzufangen.
Kontrollschalter im Genom
Um die DNA-Schalter zu finden, die Regenerationsgene an- und ausschalten, maß das Team, welche Bereiche des Genoms nach Flossenverletzung bei Polypterus sich öffneten. Hunderte Regionen wurden zugänglicher, viele lagen in der Nähe von Genen, die bereits in Wundhaut und Blastema aktiv waren. Diese Regionen waren angereichert für Bindungsstellen von AP-1-Transkriptionsfaktoren, Proteinen, die als Master-Schalter für Gennetzwerke fungieren. Ähnliche Faktoren wurden bereits in der Regeneration von Zebrafisch und Axolotl in Verbindung gebracht, was darauf hindeutet, dass eine konservierte regulatorische Logik bei sehr unterschiedlichen Tieren und Anhängseln wirkt.
Was das für zukünftige Heilung bedeutet
Für eine allgemeine Leserschaft ist die Kernbotschaft, dass Flossen- und Gliedmaßenregeneration keine magischen Einzelfälle sind; sie beruhen auf einem gemeinsamen Satz zellulärer Akteure und genetischer Schaltkreise, die vor langer Zeit entstanden sind. Hoch regenerative Tiere kombinieren dieses alte Werkzeugset mit artspezifischen Anpassungen – etwa zusätzlichen Myoglobin-Genen oder ungewöhnlichem Verhalten von Blutzellen – um die Reparatur fein abzustimmen. Indem die Studie diese gemeinsamen und einzigartigen Strategien kartiert, rückt sie uns näher an das Verständnis, warum einige Wirbeltiere komplexe Strukturen nachbilden können, andere, einschließlich des Menschen, jedoch nicht, und sie weist auf molekulare Wege hin, die eines Tages genutzt werden könnten, um die Heilung in unseren eigenen Körpern zu verbessern.
Zitation: F. Sousa, J., Lima, G., Perez, L. et al. Comparative multi-omic analysis reveals conserved and derived mechanisms of fin and limb regeneration. Nat Commun 17, 1922 (2026). https://doi.org/10.1038/s41467-026-68801-w
Schlüsselwörter: Gliedmaßenregeneration, Flossenregeneration, Wundheilung, Stammzellen, Evolution