Clear Sky Science · de
YL1004 ist ein SARS-CoV-2-Papain‑ähnlicher Proteaseinhibitor mit immunmodulierender und antiviraler Aktivität bei Mäusen
Warum eine neue COVID‑19‑Pille weiterhin wichtig ist
Die Welt verfügt über Impfstoffe und mehrere antivirale Tabletten gegen COVID‑19, doch das Coronavirus entwickelt sich weiter, umgeht Immunität und entwickelt Resistenzen gegen bestehende Medikamente. Diese Studie stellt YL1004 vor, ein experimentelles orales Medikament, das eine andere Schwachstelle von SARS‑CoV‑2 angreift und zugleich die körpereigenen Abwehrkräfte stärkt. Bei Mäusen verringerte es nicht nur die Viruslast verschiedener Varianten, einschließlich einer gegen Medikamente resistenten Linie, sondern verhinderte auch den Tod bei ansonsten tödlichen Infektionen.
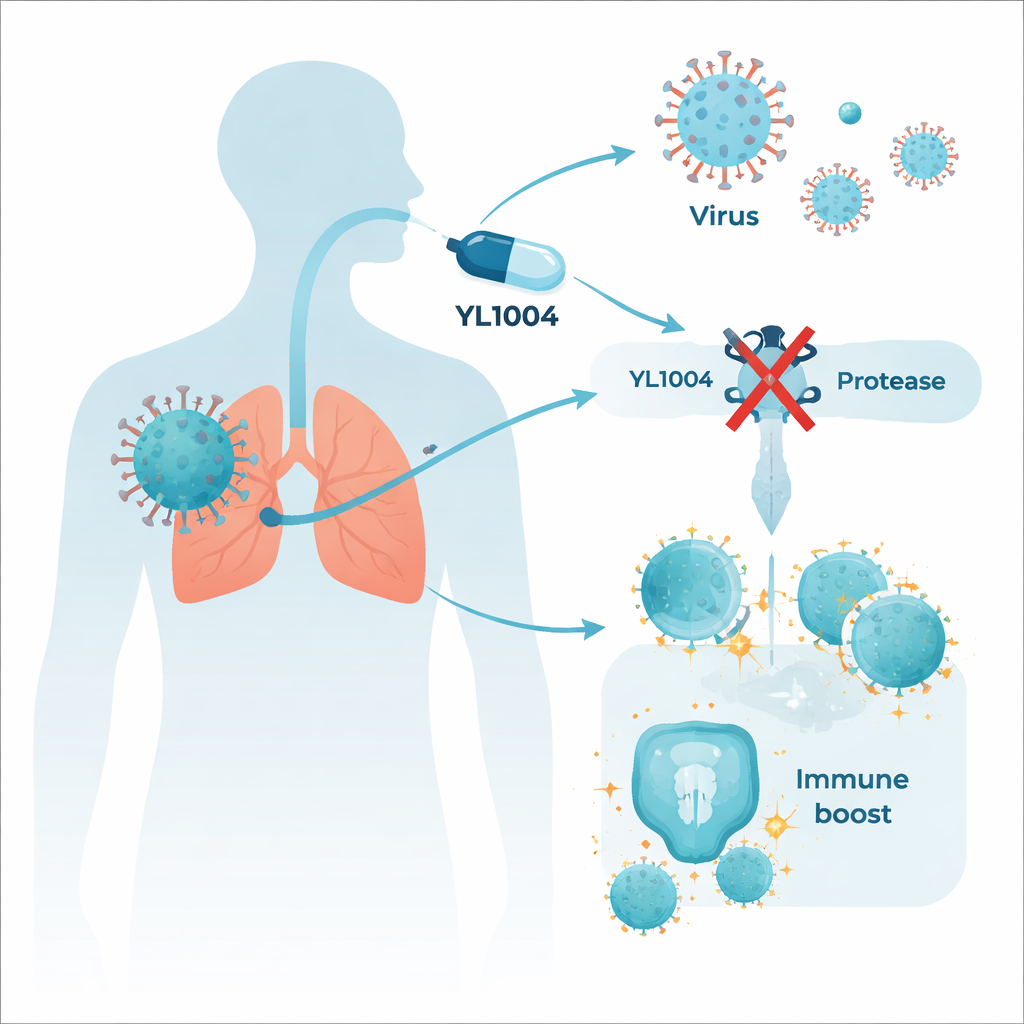
Ein virales Werkzeug mit doppelter Funktion
YL1004 wurde entwickelt, um ein virales Enzym namens papainähnliche Protease, oder PLpro, zu blockieren. Dieses Enzym wirkt wie eine molekulare Schere: Es zerschneidet lange virale Proteine in funktionale Teile, die das Virus zur Vermehrung benötigt. PLpro hat jedoch eine zweite, tückischere Aufgabe. Es entfernt kleine chemische Markierungen von unseren eigenen Immunproteinen und dämpft damit Alarmsignale, die normalerweise Immunzellen aktivieren würden. Wegen dieser Doppelrolle kann die Hemmung von PLpro sowohl die Virusreplikation verlangsamen als auch frühe antivirale Abwehrreaktionen wiederherstellen.
Entwurf eines präzisen molekularen Schlosses
Die Forscher begannen mit einem Screening von etwa 35.000 Verbindungen auf ihre Fähigkeit, PLpro in einem Reagenzglas‑Assay zu stören. Sie entdeckten eine vielversprechende „trizyklische“ chemische Gestalt und verfeinerten diese dann systematisch, geleitet durch Vergleiche mit älteren PLpro-Hemmern. Dutzende Variationen wurden hergestellt, optimiert und auf Wirksamkeit, Unbedenklichkeit in Zellen und pharmakokinetisches Verhalten in Tieren getestet. YL1004 ging als bester Kandidat hervor: Es hemmte PLpro stark bei sehr niedrigen Konzentrationen, zeigte geringe Toxizität in mehreren menschlichen und Affenzelllinien und wies günstige „arzneimittelähnliche“ Eigenschaften auf, etwa gute Stabilität in Lebertests, vernünftige Löslichkeit und die Fähigkeit, Zellschichten effizient zu passieren.
Visuelle Einsichten, wie das Medikament das Virus greift
Um zu verstehen, warum YL1004 so gut wirkt, löste das Team eine 3D‑Kristallstruktur des Wirkstoffs gebunden an PLpro. Die Bilder zeigten, dass YL1004 in eine Tasche nahe einer flexiblen Schleife auf der Enzymoberfläche passt und mehrere enge Kontakte ausbildet. Teile des Moleküls bilden Wasserstoffbrücken—spezifische richtungsgebundene Anziehungen—zu mehreren Aminosäuren, während andere ringförmige Bereiche eine breite hydrophobe, also wasserabweisende, Oberfläche schaffen, die das Molekül verankert. Im Vergleich zu einem klassischen PLpro-Inhibitor knüpft YL1004 mehr und stärkere Kontakte, was seinen verbesserten Halt erklärt. Strukturelle Vergleiche mit ähnlichen menschlichen Enzymen zeigten außerdem, warum YL1004 diese verschont und so das Risiko von Off‑Target‑Nebenwirkungen verringert.
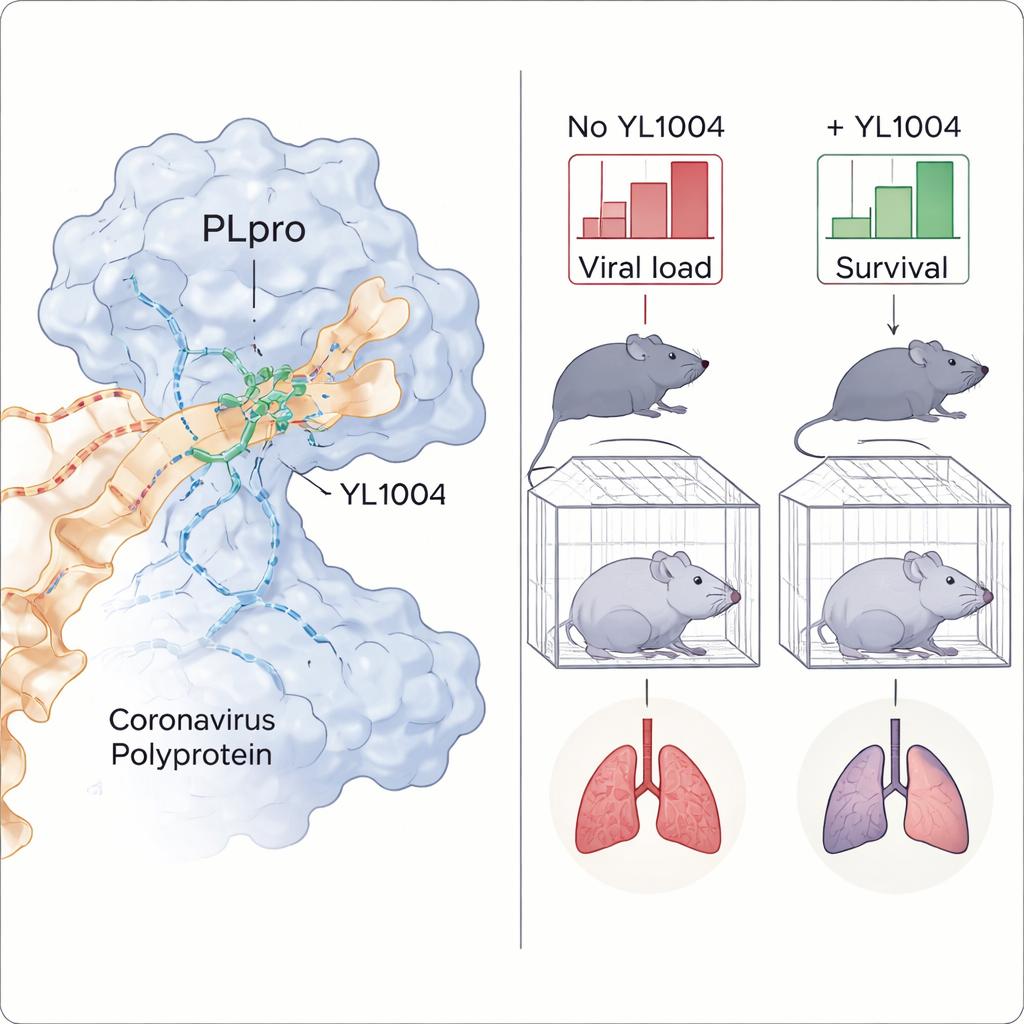
Stärkung antiviraler Abwehrkräfte und Bekämpfung von Varianten
In Zellen kehrte YL1004 die Fähigkeit des Enzyms um, regulatorische Markierungen von Immun‑Signalproteinen zu entfernen, und stellte dadurch wichtige Warnwege wie die Interferon‑Signalübertragung und NF‑κB wieder her, die zentral für die frühe antivirale Abwehr sind. Genomweite RNA‑Analysen bestätigten, dass die Expression von PLpro normalerweise viele immunbezogene und Stress‑Antwort‑Gene unterdrückt, während die Zugabe von YL1004 diese Wege wieder aktivierte. Als das Medikament gegen lebendes Virus in aus menschlicher Lunge stammenden Zellen getestet wurde, reduzierte es sowohl virales genetisches Material als auch infektiöse Partikel der ursprünglichen SARS‑CoV‑2‑Stammlinie und mehrerer wichtiger Varianten deutlich, darunter Delta und Omicron‑Unterlinien JN.1 und KP.3. Bemerkenswerterweise blieb es gegen ein so konstruiertes Virus aktiv, das gegen Nirmatrelvir, den Hauptbestandteil der antiviralen Pille Paxlovid, widerstandsfähig ist.
Schutz infizierter Mäuse vor tödlicher Krankheit
Die eindrücklichsten Ergebnisse stammen aus Experimenten an genetisch veränderten Mäusen, die hoch empfänglich für SARS‑CoV‑2 sind. Nach oraler Gabe erreichte YL1004 Blutspiegel, die hoch genug und lange genug waren, um die in Zellkulturen benötigten hemmenden Konzentrationen zu erreichen oder zu übertreffen. Bei Mäusen, die mit einer Omicron‑JN.1‑Linie infiziert wurden, senkte die Behandlung die Viruszahlen in Nase und Lunge deutlich und reduzierte Gewebeschäden sowie die Färbung viraler Proteine in Lungenabschnitten. In einem härteren Test wurden Mäuse, die mit einer tödlichen Dosis der Delta‑Variante herausgefordert wurden, entweder mit YL1004 oder mit einem Vergleichs‑PLpro-Inhibitor behandelt. Alle Tiere, die YL1004 erhielten, überlebten mit milderen Gewichtsverlusten, während die meisten unbehandelten Mäuse starben und die ältere Verbindung schlechter abschnitt.
Was das für die künftige COVID‑19‑Behandlung bedeuten könnte
Für Nichtfachleute lautet die Quintessenz: YL1004 ist eine experimentelle Next‑Generation‑COVID‑19‑Pille, die das Virus aus zwei Richtungen gleichzeitig trifft: Sie blockiert ein Schlüsselenzym, das das Virus zur Reproduktion benötigt, und hebt die Bremse auf, die das Virus dem angeborenen Immunsystem auferlegt. In Labor‑ und Mausstudien wirkte sie gegen mehrere Varianten, einschließlich einer, die einem bestehenden oralen Medikament ausweicht, und zeigte ermutigende Sicherheits‑ und Dosierungseigenschaften. Obwohl noch Studien am Menschen erforderlich sind, könnten YL1004 und ähnliche PLpro-Inhibitoren wertvolle Ergänzungen unseres Werkzeugkastens werden—insbesondere für Hochrisikopatienten und angesichts zukünftiger Varianten, die die Wirksamkeit aktueller Behandlungen abschwächen.
Zitation: Nan, J., Shuai, H., Qiao, J. et al. YL1004 is a SARS-CoV-2 papain-like protease inhibitor with immunomodulatory and antiviral activity in mice. Nat Commun 17, 2035 (2026). https://doi.org/10.1038/s41467-026-68795-5
Schlüsselwörter: SARS-CoV-2, COVID-19-Antivirale, papainähnliche Protease, Immunmodulation, Medikamentenresistenz