Clear Sky Science · de
Auslieferung von Peptid‑Koazervaten zur Bildung stabiler Interaktionszentren in Zellen
Neue „Arbeitsplätze“ innerhalb von Zellen aufbauen
Unsere Zellen sind voller kleiner Arbeitsplätze, an denen wichtige Aufgaben—wie Energiegewinnung oder Stressreaktionen—ablaufen. Im Laufe der Zeit oder bei Krankheiten können diese natürlichen Arbeitsplätze versagen. Diese Studie untersucht eine Methode, um lebenden Zellen brandneue „Interaktionszentren“ einzubauen, mithilfe einfacher, im Labor hergestellter Tropfen aus kurzen Peptiden. Diese synthetischen Zentren können bestimmte Proteine binden, sie konzentrieren und sogar beim Abbau unterstützen, was auf neue Strategien für künftige Therapien und Zelltechnik hinweist.
Warum Zellen maßgeschneiderte Arbeitsplätze brauchen
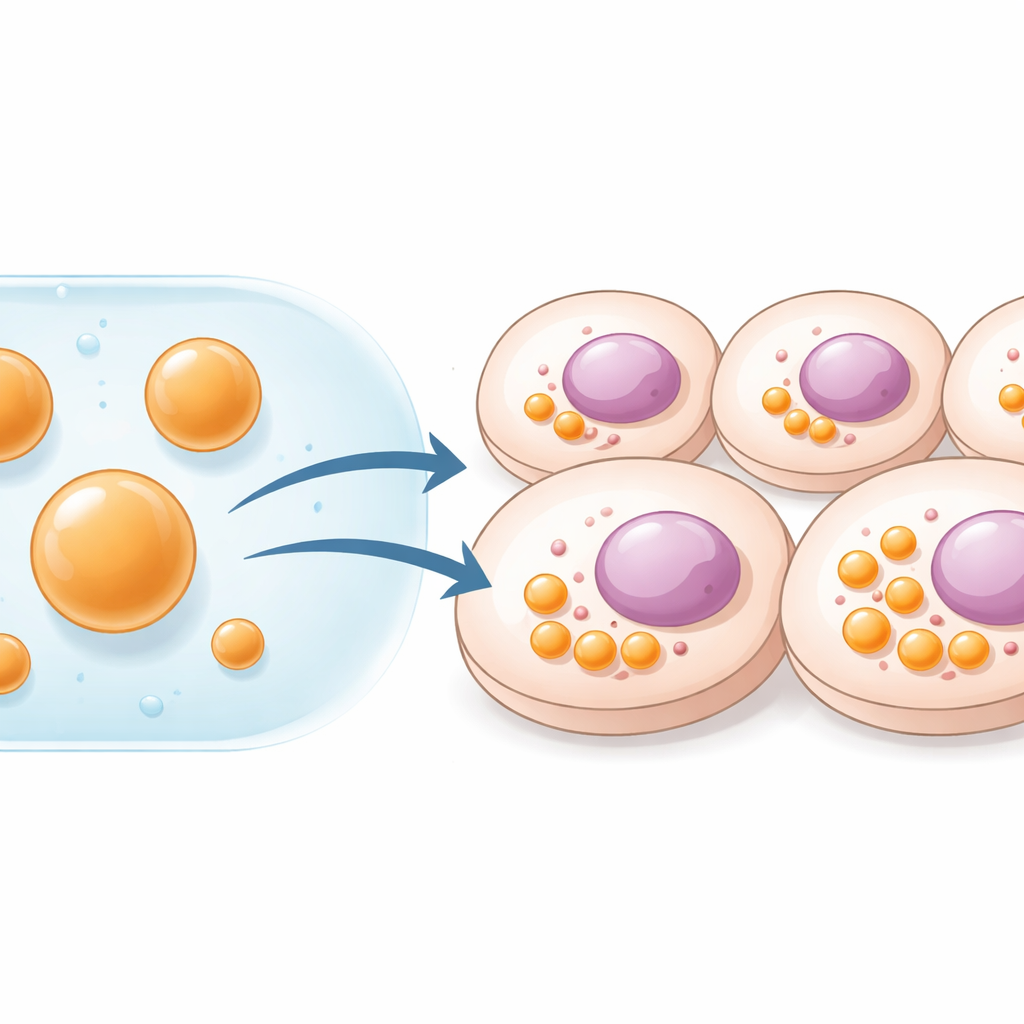
Zellen schaffen Ordnung, indem sie verschiedene Aufgaben in getrennte Kompartimente aufteilen. Einige sind von Membranen umgeben, wie Mitochondrien; andere sind weich, tropfenartige Strukturen, die entstehen, wenn sich bestimmte Proteine und RNAs zusammenlagern. Diese flüssigen Tropfen oder Kondensate fungieren als Reaktionszentren, die bestimmte biochemische Wege beschleunigen oder abschalten. Wissenschaftlerinnen und Wissenschaftler haben solche Kompartimente zuvor erzeugt, indem sie Zellen zwangen, spezielle Gerüstproteine über eingeschleuste Gene herzustellen. Diese Methode ist zwar wirkungsvoll, erfordert aber Genlieferung und begrenzt die Menge des Materials, das die Zelle produzieren kann. Die Autorinnen und Autoren dieser Studie wollten die DNA umgehen und stattdessen fertige Kompartimente außerhalb der Zelle herstellen und diese direkt als stabile, mikrometergroße Tropfen einbringen.
Peptidtropfen, die stabile Zentren bilden
Das Team arbeitete mit kurzen, ungeordneten Peptiden, bekannt als HBpep, und einer redox‑sensitiven Variante, HBpep‑SA. Unter leicht sauren Bedingungen bleiben diese Peptide gelöst, doch wenn der pH‑Wert auf nahe‑physiologische Werte angehoben wird—oder wenn die Temperatur gesenkt wird—trennen sie sich in weiche, gelartige Tropfen von etwa 1–5 Mikrometern Durchmesser ab. Durch Anpassung der Peptidkonzentration konnten die Forschenden sowohl Tropfengröße als auch Anzahl steuern. Mit Fluoreszenzmethoden zeigten sie, dass sich Peptidmoleküle innerhalb dieser Tropfen langsam bewegen, was auf einen Gel‑Zustand hinweist, der robust genug ist, Verdünnung und Handhabung zu überstehen. Werden die Tropfen Kulturen menschlicher Krebszellen, muriner Melanomzellen und primärer humaner Immunzellen zugesetzt, werden sie effizient aufgenommen und reichern sich im Zytoplasma an. Insbesondere größere Tropfen blieben mindestens fünf Tage intakt und wirkten damit als langlebige synthetische Organellen in lebenden Zellen.
Beladen und Ausrichten der Zentren
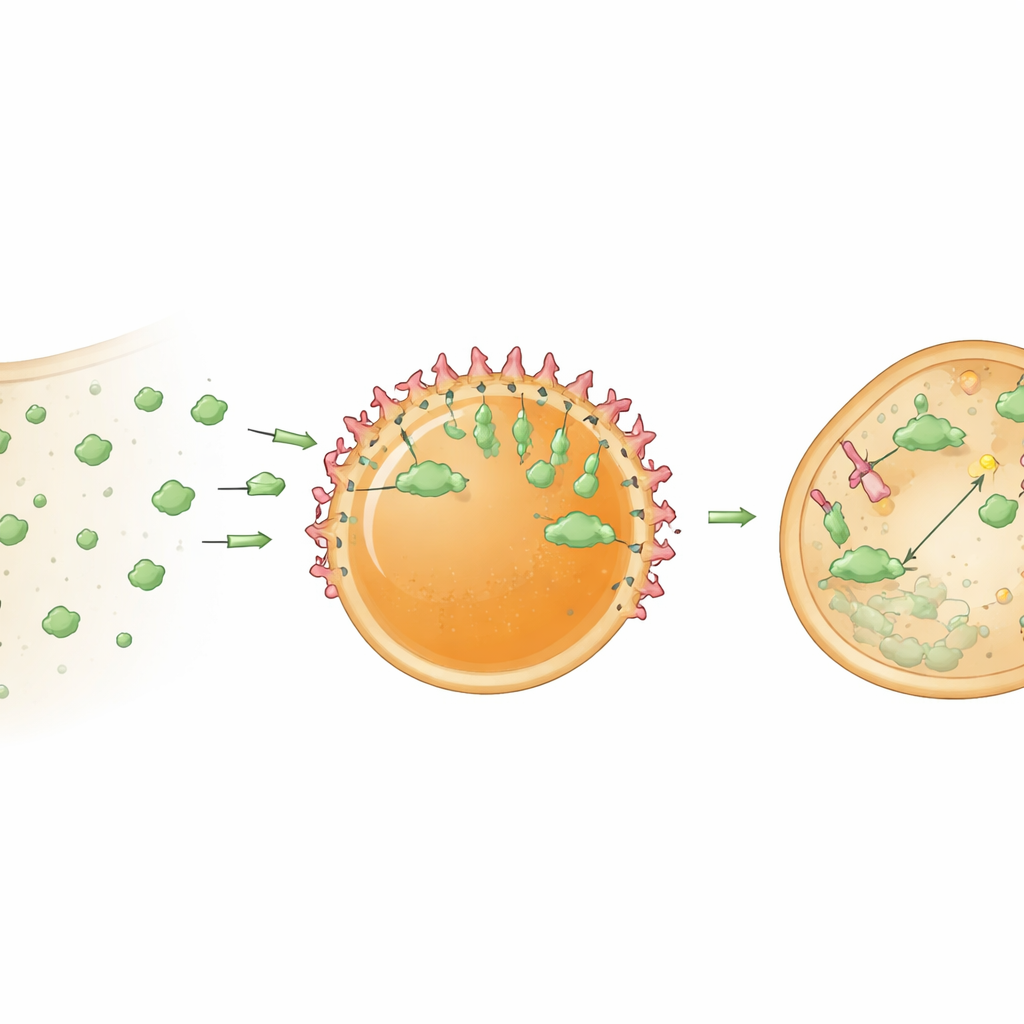
Damit diese Zentren nützlich sind, müssen sie Frachtproteine halten und organisieren. Die Forschenden verbesserten zunächst das Beladen, indem sie einem Modellprotein, GFP, ein kurzes, von HBpep abgeleitetes Tag anhängten. Dieses Tag förderte die starke Partitionierung von GFP in die Tropfen und konzentrierte es interessanterweise nahe ihrer Oberfläche, wodurch eine Kern‑Schale‑Organisation entstand. Anschließend integrierten sie Nanobodies—kompakte, Antikörper‑ähnliche Proteine, die feste Bindungen an ausgewählte Ziele eingehen—innerhalb der Tropfen. Ein GFP‑bindender Nanobody erlaubte es den Zentren, GFP selektiv sowohl in Reagenzgläsern als auch in Zellen zu erfassen. Da das Peptidgel relativ dicht ist, sammelte sich anfangs der Großteil des gefangenen GFP an der Tropfenoberfläche. Wurde die innere Struktur jedoch teilweise gelockert, etwa durch Änderungen der Redox‑Bedingungen oder dadurch, dass Tropfen aus den umgebenden endosomalen Membranen entkamen, begann GFP auch in das Innere vorzudringen. In Zellen erhöhten chemische Hilfsmittel, die die Endosomenflucht fördern, deutlich den Anteil der Zentren, die ihre Ziele erfolgreich rekrutierten.
Zentren zu Protein‑Schreddern umfunktionieren
Die Autorinnen und Autoren rüsteten diese Zentren anschließend von passiven Fallen zu aktiven Verarbeitungsstellen auf. Sie beluden die Tropfen mit einem bioPROTAC—einem Fusionsprotein, das einen zielbindenden Nanobody mit einem Teil eines Enzymadapters kombiniert, der Proteine für den Abbau durch die zelluläre Abfallentsorgungsmaschine markiert. Wurden diese „Degradosom“‑Tropfen in Zellen geliefert, die GFP stabil exprimieren, sanken die zytosolischen GFP‑Spiegel innerhalb eines Tages um etwa 78 Prozent. Kontrollzentren, die nur den Nanobody enthielten, sequestrierten GFP, senkten dessen Gesamtmenge jedoch nicht nennenswert, was bestätigt, dass der starke Rückgang durch gerichtete Degradation und nicht durch bloßes Einfangen verursacht wurde. Die Ergebnisse deuten darauf hin, dass das Clustern von bioPROTACs in einem konzentrierten Mikro‑Umfeld sie deutlich wirksamer macht als wenn sie frei im Zytoplasma verteilt sind.
Was das für künftige Therapien bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass Forschende peptidbasierte Tropfen im Reagenzglas herstellen, sie mit maßgeschneiderten Proteinwerkzeugen beladen und dann in lebende Zellen einbringen können, wo sie wie neue, langlebige Organellen funktionieren. Diese synthetischen Zentren können natürliche Proteine selektiv anziehen und, wenn sie mit Abbaumachinerie bestückt sind, ausgewählte Ziele aktiv aus der Zelle entfernen. Da diese Plattform eine Veränderung des Zellgenoms vermeidet und modular ist in dem, was sie tragen kann, eröffnet sie einen Weg zu Therapien, die zelluläre Funktionen wiederherstellen oder umschreiben—etwa durch Entfernen schädlicher Proteine oder Umprogrammieren fehlerhafter Signalwege—indem man einfach neue, programmierbare „Arbeitsplätze“ in unsere Zellen installiert.
Zitation: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Schlüsselwörter: synthetische Organellen, Peptid‑Koazervate, intrazelluläre Lieferung, Proteinabbau, Zell‑Engineering