Clear Sky Science · de
Ein bakterielles Abwehrsystem, das modifiziertes Cytosin in Phagen-Genom‑DNA erkennt
Wie Bakterien eindringende Viren überlisten
Viren, die Bakterien infizieren — sogenannte Phagen — befinden sich in einem ständigen Wettrüsten mit ihren mikrobiellen Wirten. Viele dieser Phagen verändern die chemischen Buchstaben in ihrer DNA, um bakteriellen Abwehrmechanismen zu entgehen. Diese Studie zeigt einen zuvor verborgenen bakteriellen Gegenzug: ein Proteinsystem namens CMoRE, das Phagen‑DNA mit solchen chemischen Modifikationen erkennt und zerstört. Neben der Aufdeckung einer neuen Facette des Mikroben‑Virus‑Kriegs könnte CMoRE zu einem präzisen Werkzeug werden, um subtile DNA‑Markierungen zu detektieren, die mit menschlichen Erkrankungen in Verbindung stehen.
Ein verstecktes Zeichen an DNA‑Buchstaben
Sowohl Phagen als auch Tiere modifizieren gelegentlich den Basenbuchstaben Cytosin, indem sie kleine chemische Gruppen hinzufügen. In vielen T‑even‑Phagen, darunter der klassische T4‑Phage, der E. coli befällt, wird Cytosin durch eine modifizierte Form ersetzt, das 5‑Hydroxymethylcytosin (5hmC), das wiederum weiter modifiziert werden kann zu 5‑Glucosyl‑hydroxymethylcytosin (5ghmC). Diese Veränderungen helfen Phagen, gängige bakterielle Abwehrsysteme zu umgehen, die normalerweise unveränderte „fremde“ DNA zerschneiden und das eigene Genom schonen. Bei Säugetieren gilt eine verwandte Markierung, 5hmC, inzwischen als wichtiges epigenetisches Signal, das an Genregulation, Gehirnfunktion und Krebs beteiligt ist — sie ist jedoch sehr selten und schwer zuverlässig zu messen.
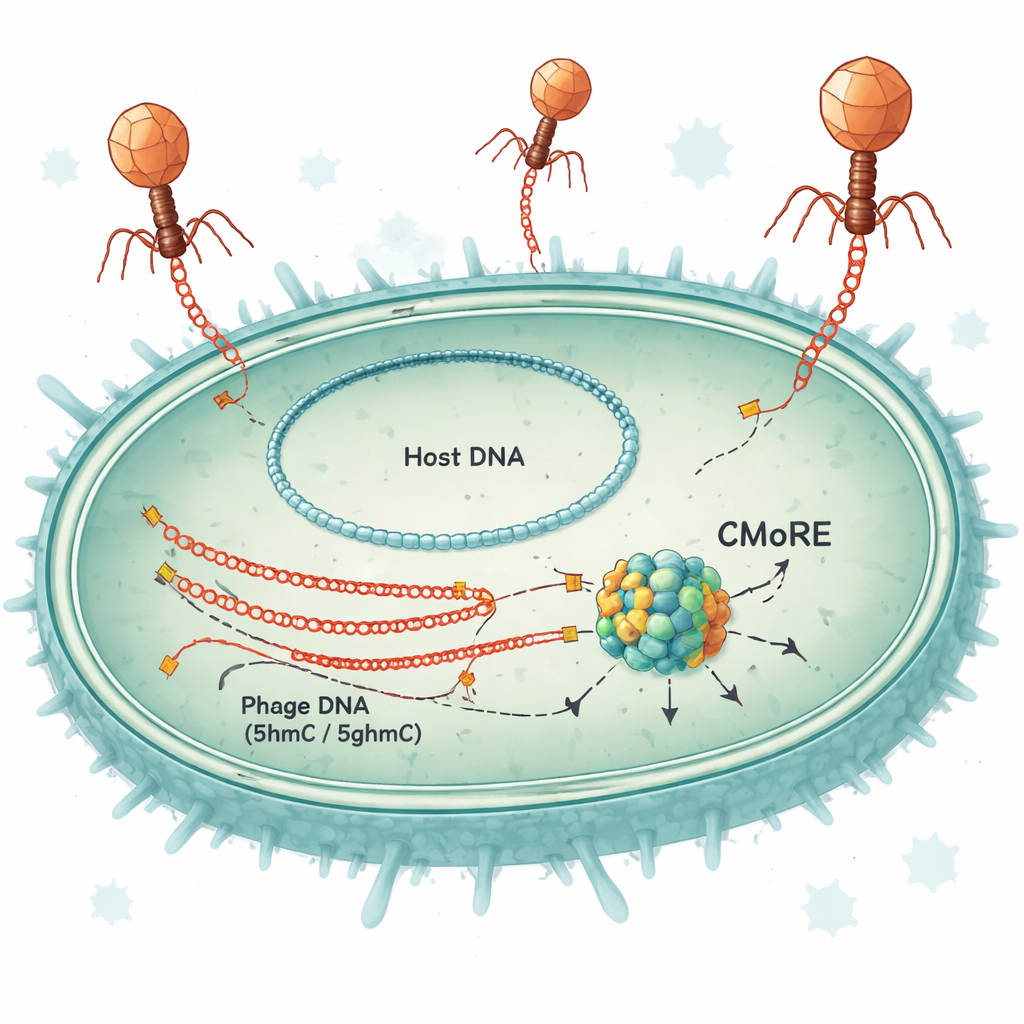
Ein einkettiges Sicherheits‑System
Die Forschenden untersuchten ein Abwehrgen, das ursprünglich in bestimmten Stämmen von E. coli und verwandten Bakterien gefunden wurde. Wenn sie dieses Gen — inzwischen CMoRE genannt — in Laborstämme einführten, die es normalerweise nicht besitzen, wurden die Bakterien nahezu vollständig resistent gegen mehrere T‑even‑Phagen, darunter T2, T4 und T6. Unter starkem Virusangriff wuchsen Zellen mit CMoRE weiter, was zeigt, dass das System schützt, ohne die Wirtszelle in einer „Suizid“‑Antwort zu opfern. Tests in Flüssigkultur und auf festen Platten zeigten, dass die Phageninfektion um bis zu etwa hunderttausendfach zurückging, während Bakterien ohne CMoRE verwundbar blieben.
Präzise Ausrichtung auf modifizierte virale DNA
Um zu untersuchen, was CMoRE tatsächlich schneidet, reinigte das Team das Protein und setzte es der DNA verschiedener Phagen und Bakterien aus. CMoRE zersetzte selektiv die DNA von T‑even‑Phagen, ließ bakterielle DNA aber weitgehend unberührt. Als sie Test‑DNA‑Fragmente mit verschiedenen Cytosin‑Varianten herstellten, ignorierte CMoRE normales Cytosin und eine häufige methylierte Form (5mC), degradiere jedoch effizient DNA, die 5hmC oder 5ghmC enthielt. Ein mutierter T4‑Phage, dessen Genom unverändertes Cytosin verwendete, wurde vollständig resistent gegen die Abwehr — ein Beleg dafür, dass die chemische Modifikation und nicht eine bestimmte Sequenz von CMoRE erkannt wird. Sequenzierung der Fragmente nach dem Schnitt zeigte, dass CMoRE wie ein Restriktionsenzym wirkt: Es bindet zwei modifizierte Cytosine mit charakteristischem Abstand und erzeugt saubere Schnitte, die kurze Überhänge an den DNA‑Enden hinterlassen.
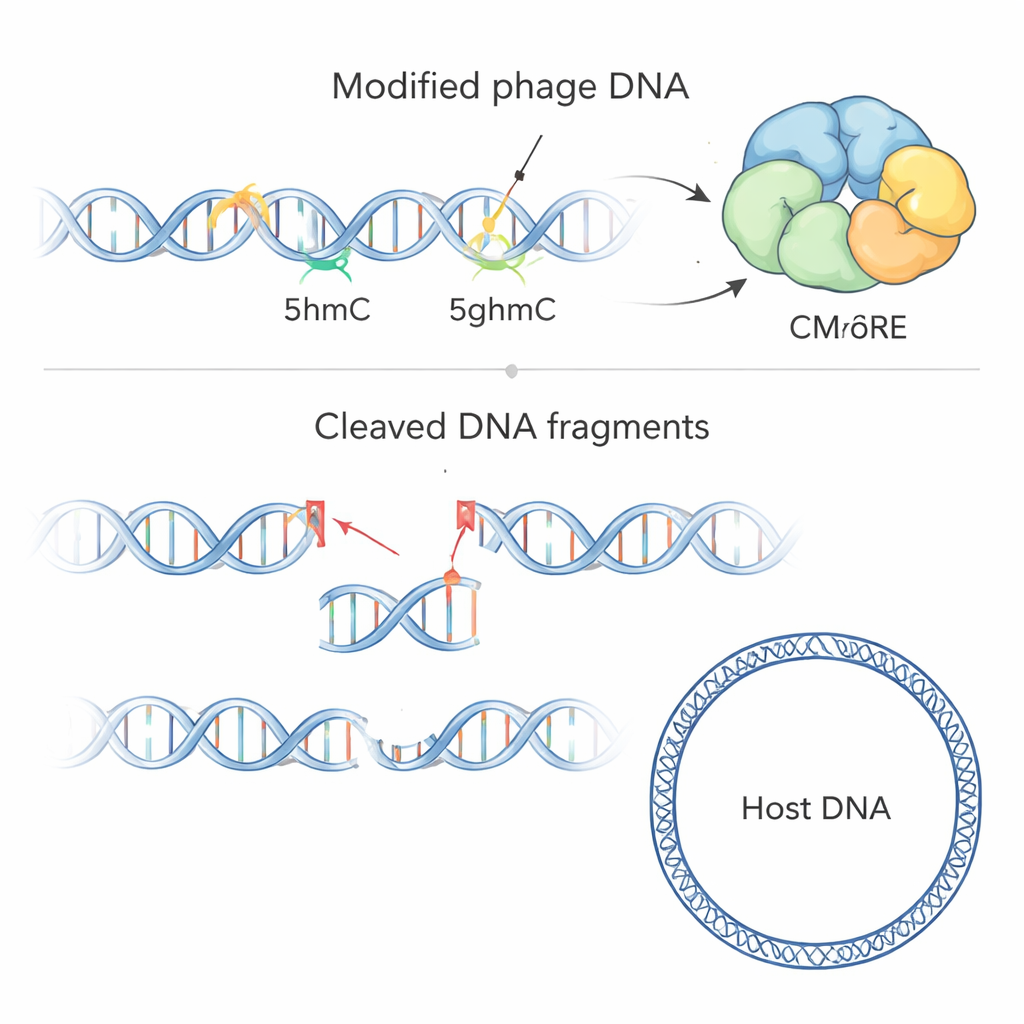
Die Struktur und der Sicherheitsverschluss von CMoRE
Mithilfe der Röntgenkristallographie bestimmten die Autorinnen und Autoren hochaufgelöste Strukturen von CMoRE aus zwei Bakterienarten. Das Protein besteht aus zwei verbundenen Teilen: einer N‑terminalen „Klinge“, die den DNA‑Schnitt ausführt und zur GIY‑YIG‑Nukleasefamilie gehört, und einem C‑terminalen „Sensor“, der das modifizierte Cytosin erfasst. Vier Kopien von CMoRE ordnen sich zu einem kompakten Tetramer, und die Störung dieser Assemblierung beseitigt größtenteils die antivirale Aktivität. Die Schnittdomäne trägt ein charakteristisches „GIYxY–YIG“‑Motiv und eine ungewöhnliche, negativ geladene Schleife, die wie ein Deckel über dem aktiven Zentrum liegt. Wenn die Forschenden diese Schleife neutralisierten, wurde CMoRE überaktiv, begann normale bakterielle DNA anzugreifen und verlangsamte das Zellwachstum — Hinweise darauf, dass die Schleife als eingebauter Sicherheitsverschluss wirkt und dem Protein hilft, stark zugunsten von Phagen‑DNA mit 5hmC oder 5ghmC zu diskriminieren.
Von mikrobialer Kriegsführung zu medizinischen Werkzeugen
Beim Durchsuchen tausender mikrobieller Genome fanden die Forschenden Hunderte verwandter CMoRE‑Systeme in vielen Bakteriengruppen, die alle dieselben Schlüsselmerkmale teilen: die zusätzliche Tyrosin‑Residue im katalytischen Motiv und die negativ geladene Sicherheits‑Schleife. Das deutet darauf hin, dass CMoRE eine weit verbreitete Strategie in der bakteriellen Abwehr gegen chemisch getarnte Phagen ist. Da CMoRE 5hmC und 5ghmC sauber von dem fast identischen 5mC unterscheiden kann und das Protein stabil sowie im Labor leicht handhabbar ist, könnte es auch als hochselektives „molekulares Skalpell“ zum Kartieren von 5hmC in Säugetiergenomen dienen. Das könnte die Werkzeuge zur Erkennung krankheitsassoziierter epigenetischer Veränderungen verbessern und damit einen praktischen Nutzen aus dem Verständnis liefern, wie Bakterien ihre mikroskopischen Feinde überleben.
Zitation: Liu, R., Tang, D., Niu, M. et al. A bacterial defense system targeting modified cytosine of phage genomic DNA. Nat Commun 17, 1920 (2026). https://doi.org/10.1038/s41467-026-68792-8
Schlüsselwörter: Abwehr gegen Bakteriophagen, DNA‑Modifikation, 5‑Hydroxymethylcytosin, Restriktionsenzym, Epigenetik