Clear Sky Science · de
CRISPR-Cas9-Trans-Cleavage wird durch ein flankiertes R-Loop, einen verlängerten Spacer und eine inaktive HNH-Domäne gehemmt
Warum winzige DNA-Schnitte wichtig sind
CRISPR-Cas9 ist als molekulares Skalpell bekannt, das DNA an gewählten Stellen schneiden kann, doch dieses Werkzeug zeigt ein zweites, weniger beachtetes Verhalten: Sobald es aktiviert ist, kann es auch an anderen in der Nähe befindlichen genetischen Fragmenten nagen. Zu verstehen, wann dieses „kollaterale“ Schneiden an- oder ausgeht, ist entscheidend, um sicherere Gentherapien und empfindlichere Diagnosetests zu entwickeln. Diese Studie zerlegt die physikalischen Merkmale des Cas9–DNA–RNA-Komplexes, die darüber entscheiden, ob Cas9 nur seinen beabsichtigten Schnitt setzt oder zusätzlich fremde einzelsträngige DNA zerkaut.
Wie die CRISPR-Schere in Gang kommt
Um aktiv zu werden, bindet Cas9 ein kurzes Stück Guide-RNA, das es zu einer passenden DNA-Sequenz im Genom lenkt. Findet Cas9 sein Ziel, paaren sich Guide-RNA und ein DNA-Strang, wodurch sich die beiden DNA-Stränge trennen und eine DNA–RNA-Hybridregion entsteht, das sogenannte R-Loop. In seiner klassischen Rolle schneidet Cas9 dann beide DNA-Stränge an dieser Stelle. Neuere Arbeiten zeigten jedoch, dass nach dieser Aktivierung die RuvC-Schneidedomäne von Cas9 auch unverwandte einzelsträngige DNA zerschneiden kann, etwa Poly(T)-Sequenzen, die anderswo in der Lösung vorkommen. Die Autoren fragten daher: Welche genauen geometrischen und strukturellen Merkmale von Ziel-DNA und Guide-RNA machen diese kollaterale Aktivität stark, schwach oder gar nicht vorhanden?
Kurze vs. lange Ziele: Cas9 Platz zum Bewegen geben
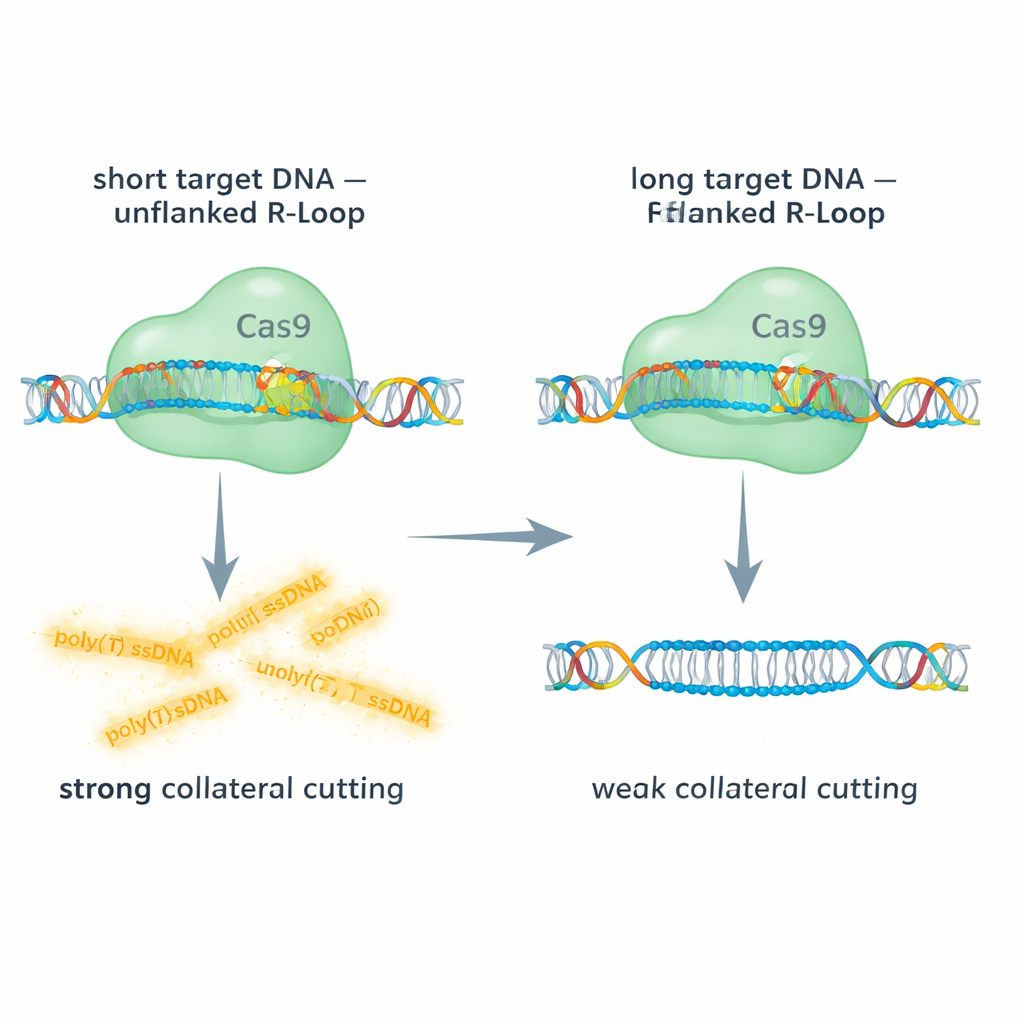
Das Team verglich Cas9 an kurzen und langen doppelsträngigen DNA-Zielen und nutzte Fluoreszenzsignale, um sowohl den On-Target-Schnitt als auch die kollaterale Spaltung einer einzelsträngigen DNA-Sonde zu verfolgen. Bei kurzen DNA-Zielen ist das R-Loop am 5′-Ende der Guide-RNA „unflankiert“ – es gibt keine zusätzliche doppelsträngige DNA, die über die Hybridregion hinaus fortläuft. Unter diesen Bedingungen zeigte Cas9 eine starke kollaterale Aktivität gegen einzelsträngige DNA. Im Gegensatz dazu nahm die kollaterale Spaltung bei Verwendung längerer DNA-Segmente, die das R-Loop seitlich flankierende doppelsträngige DNA ließen, drastisch ab, manchmal um etwa 90 %, obwohl der primäre On-Target-Schnitt weiterhin stattfand. Die Verwendung langer einzelsträngiger Zielsequenzen, die das R-Loop ganz entfernen, stellte die kollaterale Aktivität weitgehend wieder her. Diese Vergleiche zeigen, dass eine doppelsträngige „Kappe“ neben dem R-Loop den Komplex versteift und physisch den Zugang oder die Flexibilität behindert, die die RuvC-Domäne von Cas9 benötigt, um andere Stränge zu zerschneiden.
Feinabstimmung mit Guide-Länge und Mismatch
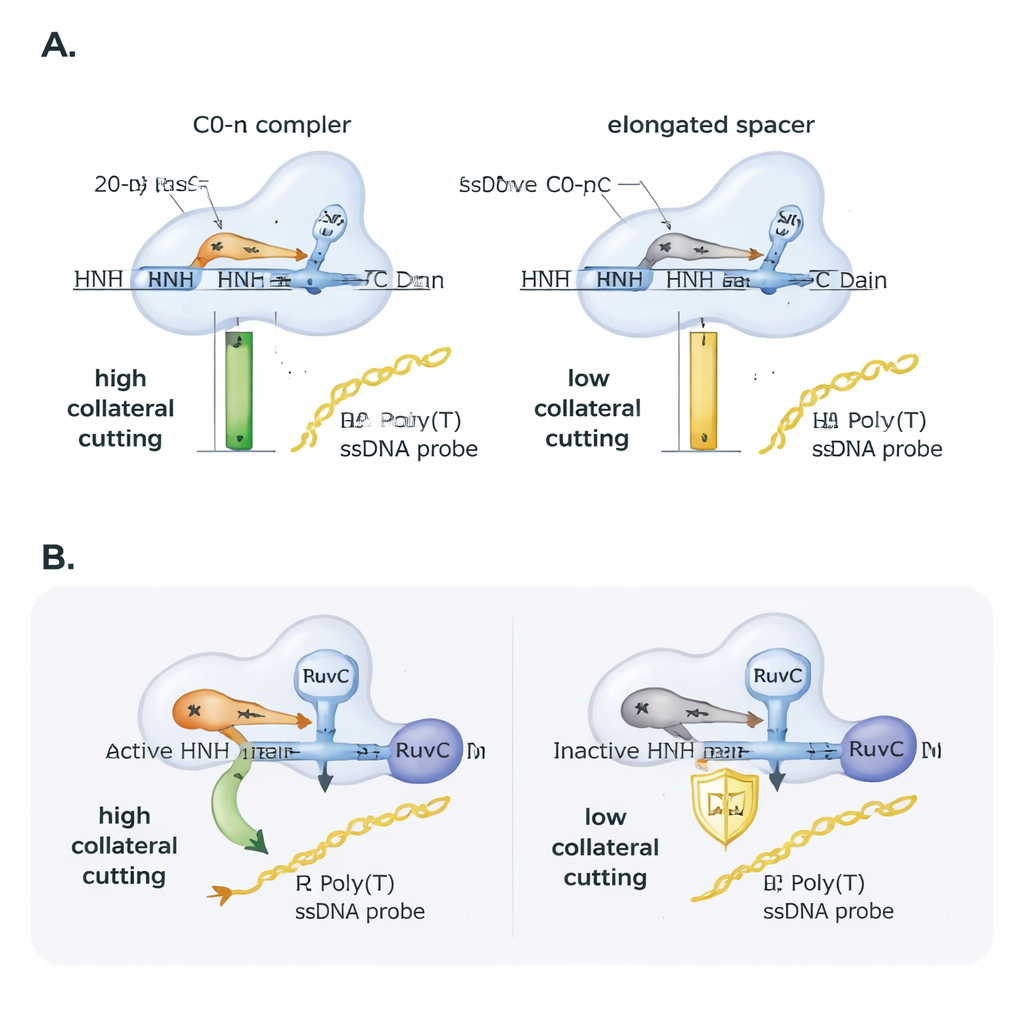
Die Forscher untersuchten anschließend, wie die Guide-RNA dieses Verhalten einstellt. Sie führten kleine Mismatches zwischen Guide und Ziel-DNA ein und verfolgten, wie gut Cas9 noch schnitt. Der Haupt-On-Target-Schnitt tolerierte viele Einzelbasen-Mismatches, doch die kollaterale Spaltung war empfindlicher und hing stark davon ab, wo genau der Mismatch lag, was ihre Sensitivität unterstreicht. Danach verlängerten sie systematisch den Guide-RNA-Spacer über die üblichen 20 Nukleotide hinaus. Obwohl Cas9 das Ziel weiterhin binden und schneiden konnte, fiel die kollaterale Aktivität nahezu linear mit zunehmender Spacer-Länge: Das Hinzufügen von nur zwei Basen halbierte die kollaterale Aktivität ungefähr, vier zusätzliche Basen reduzierten sie noch stärker. In praktischen Tests mit SARS-CoV-2-Material zeigten nur DNA-Amplikons, die so angeordnet waren, dass sie ein unflankiertes R-Loop mit einem Guide normaler Länge erzeugten, ein starkes kollaterales Signal – ein Hinweis darauf, wie Primer- und Guide-Design CRISPR-basierte Nachweismethoden machen oder brechen können.
Eine wesentliche Helfer-Domäne im Hintergrund
Cas9 besitzt zwei Schneidedomänen, RuvC und HNH. Frühere Arbeiten verknüpften die kollaterale Spaltung direkt mit RuvC, doch diese Studie zeigt, dass HNH trotzdem eine Rolle spielt. Als die Autoren eine Cas9-Variante mit inaktiver HNH-Domäne verwendeten, brach die kollaterale Aktivität ein, obwohl die Bindung an das Ziel und das Nicken weiterhin bestanden. Interessanterweise gewann die inaktive-HNH-Version die kollaterale Spaltung zurück, wenn man Cas9 ein DNA-Ziel anbot, das bereits in einem Strang genickt war, und zwar ähnlich wie das normale Enzym. Das legt nahe, dass die Rolle von HNH teilweise mechanisch ist: Durch das Schneiden oder Lockern des zielgerichteten Strangs hilft sie dem Protein, in eine Konformation zu gelangen, die RuvC gegenüber nahegelegener einzelsträngiger DNA exponiert. Strukturelle Analysen vorhandener 3D-Modelle stützten diese Sicht: Unflankierte R-Loops und Guides normaler Länge lassen das 5′-Ende der RNA an Cas9 „anliegen“ und positionieren die katalytischen Bereiche günstig, während flankierte R-Loops und verlängerte Guides das Protein dichter packen und wahrscheinlich die RuvC-Stelle vor fremden Strängen abschirmen.
Was das für künftige Werkzeuge bedeutet
Für Nicht-Spezialisten lautet die Hauptbotschaft: Cas9s Verhalten ist nicht alles-oder-nichts. Kleine geometrische Details – wie weit die DNA reicht, wie lang der Guide ist und ob eine Helfer-Domäne ihren Schnitt vollenden kann – entscheiden, ob das Enzym bei seiner Hauptaufgabe bleibt oder zusätzlich nahegelegene Einzelstränge zerschreddert. Kurze Ziele, die das R-Loop unflankiert lassen, standardmäßige 20-Basen-Guides und eine aktive HNH-Domäne fördern gemeinsam starke kollaterale Spaltung; lange flankierende DNA, verlängernde Guides oder eine inaktive HNH-Domäne unterdrücken sie. Diese Erkenntnisse geben Forschern ein präziseres Einstellrad für Cas9 an die Hand, das hilft, sicherere Geneditierungs-Systeme zu entwickeln, die unerwünschte Kollateralschäden vermeiden, oder leistungsfähigere Diagnostika, die diese kollaterale Aktivität bewusst nutzen, um winzige Mengen viraler oder genetischer Materie nachzuweisen.
Zitation: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Schlüsselwörter: CRISPR-Cas9, kollaterale Spaltung, R-Loop, Guide-RNA-Spacer, nukleinsäurebasierte Diagnostik