Clear Sky Science · de
Kollagen-bindendes Adhäsin begrenzt Hautinfektionen durch Staphylococcus aureus
Warum das „Klettband“ eines Hautkeims wichtig ist
Staphylococcus aureus ist die Hauptursache für schmerzhafte Hautfurunkel und Abszesse. Medikamentenresistente Stämme wie MRSA erschweren die Behandlung. Diese Studie untersucht eine unerwartete Wendung: ein bakterielles Oberflächenprotein namens Cna, das wie Klettband an Kollagen haftet, dem wichtigsten Strukturprotein in Haut und Wunden. Statt die Infektionen zu verschlimmern, finden die Autoren, dass dieses Kollagen-erfassende Protein die Hauterkrankung bei Mäusen tatsächlich dämpft, indem es beeinflusst, wie Immunzellen die Bakterien angreifen.
Ein klebriges Protein mit überraschender Aufgabe
Kollagen ist das am häufigsten vorkommende Protein in unserem Körper und wesentlich dafür, Haut zusammenzuhalten und Wunden zu heilen. Manche S.-aureus-Stämme tragen Cna, ein Protein, das in der bakteriellen Zellwand verankert ist und sowohl an Kollagen als auch an einen kollagenähnlichen Schaft des Blutproteins C1q bindet. C1q markiert normalerweise Mikroben für die Zerstörung durch das Immunsystem. Frühere Arbeiten brachten Cna mit schweren Infektionen in Gelenken und Augen in Verbindung, aber seine Rolle bei Hauterkrankungen war unklar. Die Forschenden nutzten ein Mausmodell für Hautabszesse und genetisch veränderte Bakterien, die entweder Cna produzierten, es nicht besaßen oder es auf einem Plasmid wiederhergestellt hatten, um zu untersuchen, wie dieses einzelne Adhäsin den Verlauf der Infektion verändert.
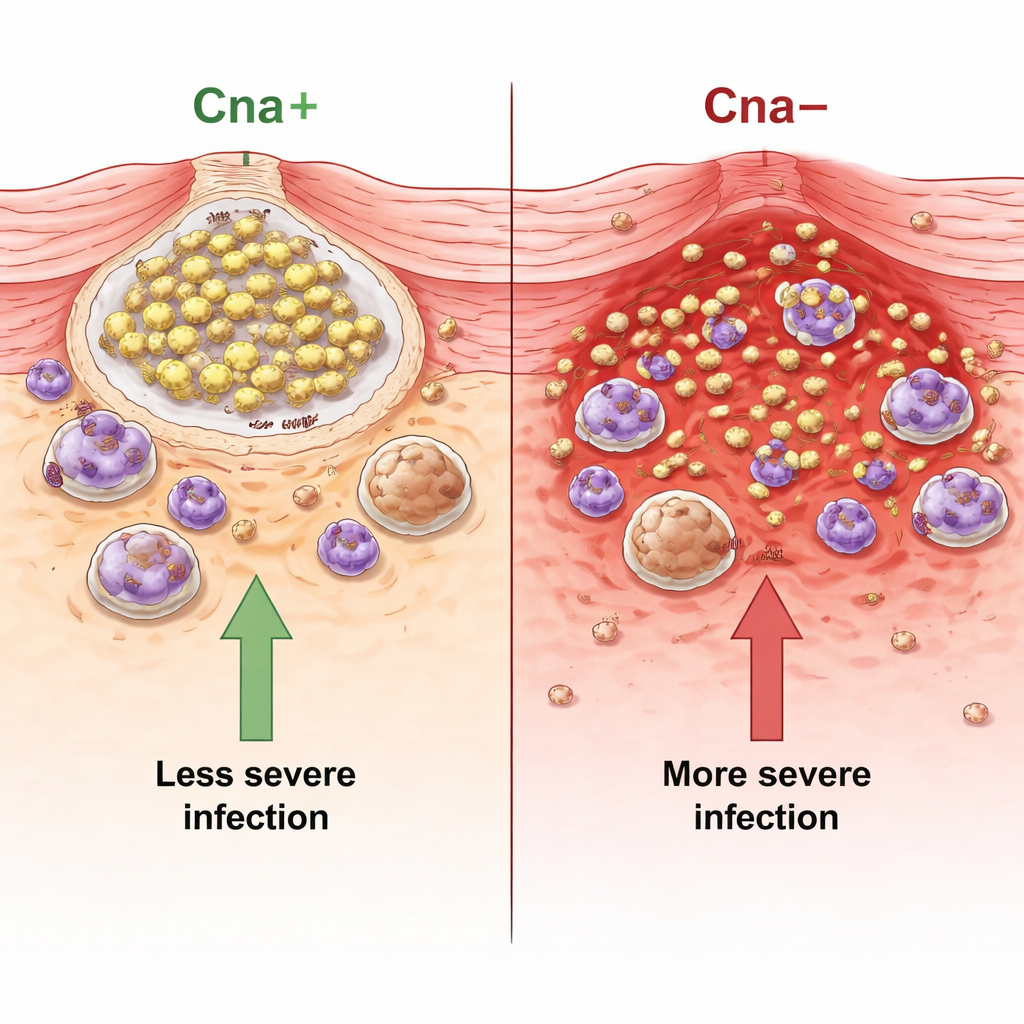
Wenn Bakterien Kollagen nicht greifen können, werden Infektionen schlimmer
Bei Mäusen, die mit Cna-positivem S. aureus infiziert wurden, blieben Hautläsionen kleiner, die Tiere verloren weniger Gewicht und aus den Abszessen wurden deutlich weniger Bakterien isoliert als bei Mäusen, die mit Cna-negativen Mutanten infiziert waren. Die Wiederherstellung von Cna kehrte diese Effekte um, was zeigte, dass das Protein selbst verantwortlich war. Das Team testete außerdem USA300, einen verbreiteten MRSA-Stamm, der natürlicherweise kein Cna besitzt und für menschliche Hautinfektionen bekannt ist. Auch bei diesem Stamm reduzierte das Hinzufügen von Cna die Läsionsgröße und die Bakterienzahlen. Untersuchungen klinischer Isolate aus Hautinfektionen, nasalen Trägern und Pneumonien ergaben, dass die meisten zirkulierenden S.-aureus-Stämme das cna-Gen gar nicht tragen, was nahelegt, dass der Verlust dieses Proteins tatsächlich aggressivere, sich ausbreitende Erkrankungen begünstigen könnte.
Wie Kollagen Bakterien schützt und Entzündung dämpft
Gewebeschnitte aus Mausabszessen erzählten eine klare Geschichte. Infektionen mit Cna-positiven Bakterien zeigten kompakte Bakteriencluster, umhüllt von Kollagen, mit Immunzellen wie Neutrophilen und Makrophagen an den Rändern. Im Gegensatz dazu waren Cna-negative Infektionen zerfleddert und durchdrungen, voll mit toten Immunzellen und starker Entzündung. Chemische Analysen des Gewebes zeigten, dass Cna-negative Infektionen höhere Spiegel entzündlicher Signalstoffe wie IL-6, TNF-α und IL-1β sowie von Enzymen der Matrix-Metalloproteinasen (MMP-9 und MMP-12) und dem Lipidmediator Leukotrien B4 auslösten — alles Faktoren, die den Zustrom von Immunzellen und Gewebeschaden verstärken. Durch Durchflusszytometrie und Bildgebung bestätigten die Autoren, dass Neutrophile in Cna-negativen Abszessen viel häufiger tot oder im Sterben begriffen waren, während lebende Immunzellen relativ rar waren.
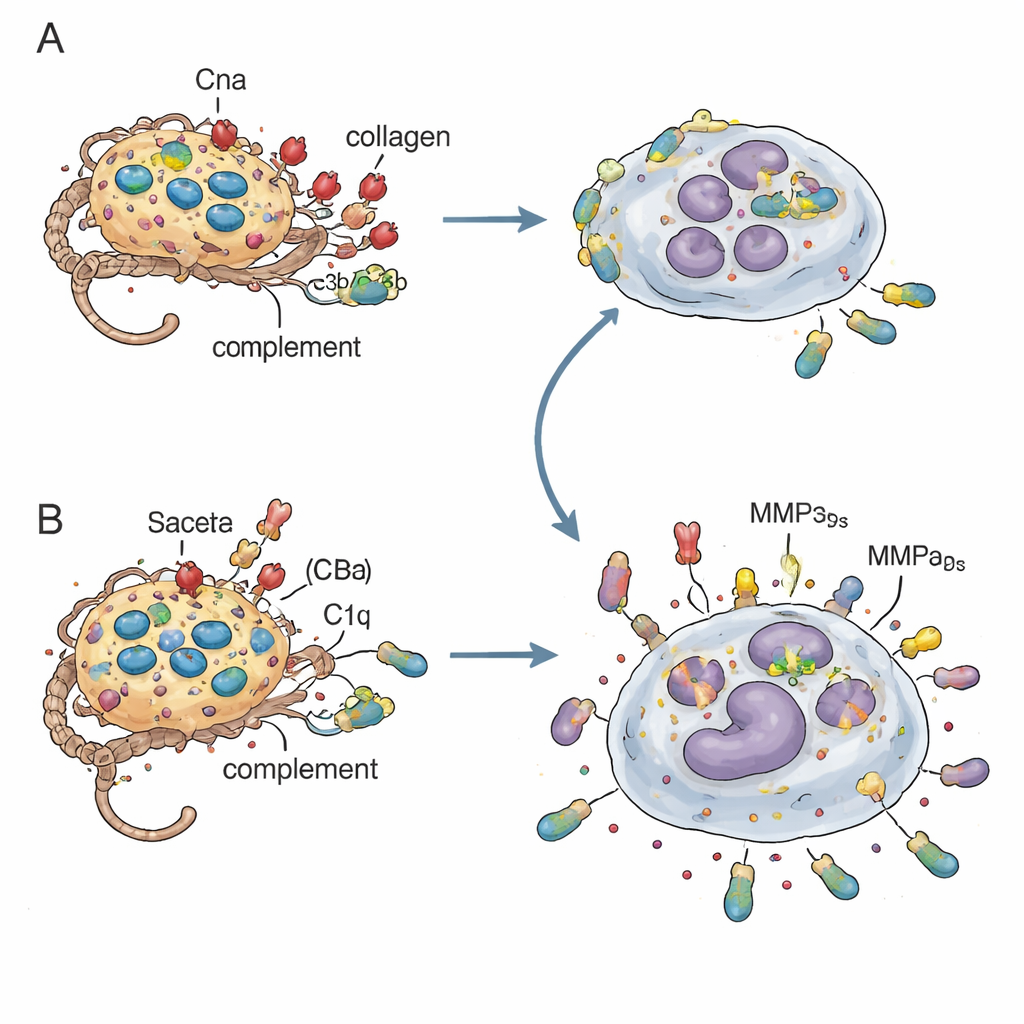
Komplement kapern, um einen tödlichen Griff zu vermeiden
Die entscheidende mechanistische Verbindung war C1q, ein Initiatormolekül des Komplementsystems, das Bakterien überzieht, damit Neutrophile sie aufnehmen können. In Reagenzglas-Experimenten akkumulierten Bakterien ohne Cna mehr Komplementkomponenten (C4b und C3b) auf ihrer Oberfläche und wurden von menschlichen Neutrophilen stärker aufgenommen. Doch dieses übertriebene Aufnehmen rächte sich: Neutrophile, die mit Cna-negativen Bakterien überfüllt waren, neigten zur Lyse und setzten lebende Bakterien und entzündliche Moleküle wieder in das Gewebe frei. Als die Forschenden Serum ohne C1q verwendeten oder Mäuse genetisch ohne C1q einsetzten, schrumpften die Unterschiede zwischen Cna-positiven und Cna-negativen Infektionen, was zeigte, dass Cnas Bindung an den kollagenähnlichen Schaft von C1q das Komplement-Tagging abschwächt und die Überreaktion der Neutrophilen dämpft. Gleichzeitig scheint an Cna-positiven Bakterien gebundenes Kollagen eine physische Barriere zu bilden, die den direkten Kontakt mit Neutrophilen verlangsamt und eine kontrolliertere Abtötung ermöglicht.
Abwägung von Abwehr und Schaden bei Hautinfektionen
Für Nichtfachleute lautet die Hauptbotschaft: Nicht alle bakteriellen „Klebigkeit“ macht Infektionen schlimmer. In diesem Fall rufen S.-aureus-Stämme, die an Kollagen und C1q haften können, eine maßvollere Immunantwort hervor: weniger explodierende Neutrophilen‑Zelltode, geringere Entzündung und weniger Hautschaden, auch wenn die Bakterien weiterhin vorhanden sind. Stämme ohne Cna, darunter viele wichtige MRSA-Klone, werden leichter vom Komplement markiert, lösen einen Sturm neutrophiler Aktivität aus und verursachen größere, zerstörerischere Abszesse. Das Verständnis dieses feinen Gleichgewichts zwischen bakteriellem Verstecken und immunologischer Überreaktion könnte neue Strategien zur Behandlung von Hautinfektionen informieren — entweder durch das Anvisieren der Interaktion von Bakterien mit Kollagen und C1q oder durch die Modulation der entzündungsfördernden Enzyme und Lipide, die aus einem begrenzten Abszess eine schädliche Läsion machen.
Zitation: Bhattacharya, M., Spencer, B.L., Kwiecinski, J.M. et al. Collagen binding adhesin restricts Staphylococcus aureus skin infection. Nat Commun 17, 1980 (2026). https://doi.org/10.1038/s41467-026-68788-4
Schlüsselwörter: Staphylococcus aureus, Hautabszess, Kollagen, Neutrophile, Komplementsystem