Clear Sky Science · de
NatA geht am Ausgang des ribosomalen Polypeptidtunnels Mehrfachkomplexe ein
Wie Zellen neue Proteine bei der Entstehung feinabstimmen
Sekündlich stellen Ihre Zellen tausende neuer Proteine auf winzigen Maschinen, den Ribosomen, her. Sobald jede Proteinkette herauskommt, muss sie zugeschnitten, markiert und korrekt gefaltet werden, sonst kann sie fehlfunktionen und zur Krankheitsentstehung beitragen. Diese Studie untersucht eines der zentralen Markiersysteme, eine Modifikation namens N‑terminale Acetylierung, und zeigt, wie ein zentrales Enzymkomplex, NatA, gemeinsam mit mehreren Partnern genau dort wirkt, wo neue Proteine das Ribosom verlassen. Das Verständnis dieses Zusammenspiels erklärt, wie Zellen ihre Proteinfabriken reibungslos am Laufen halten.
Das winzige chemische Etikett, das zählt
Die meisten Proteine beginnen ihr Dasein mit demselben ersten Baustein, der Aminosäure Methionin. Häufig wird dieses anfängliche Methionin entfernt und durch eine kleine chemische Markierung, eine Acetylgruppe, ersetzt. Diese Markierung, die an der sehr Spitze des Proteins (seinem N‑Termin) angebracht wird, kann beeinflussen, wie lange das Protein überdauert, wohin es in der Zelle gelangt und wie es funktioniert. Zwei Haupttypen von Enzymen sitzen am Ausgang des Ribosomentunnels, um dieses erste Umstyling zu steuern: Methionin‑Aminopeptidasen (MAPs), die das startende Methionin abschneiden, und N‑terminale Acetyltransferasen (NATs), die das Acetyl‑Etikett hinzufügen. Unter den NATs ist NatA der Arbeitspferdkomplex in menschlichen Zellen und modifiziert möglicherweise fast 40 % aller Proteine. Weil viele Proteine gleichzeitig hergestellt werden, muss die Zelle diese Enzyme so organisieren, dass Abschneiden und Markieren schnell und in der richtigen Reihenfolge ablaufen.
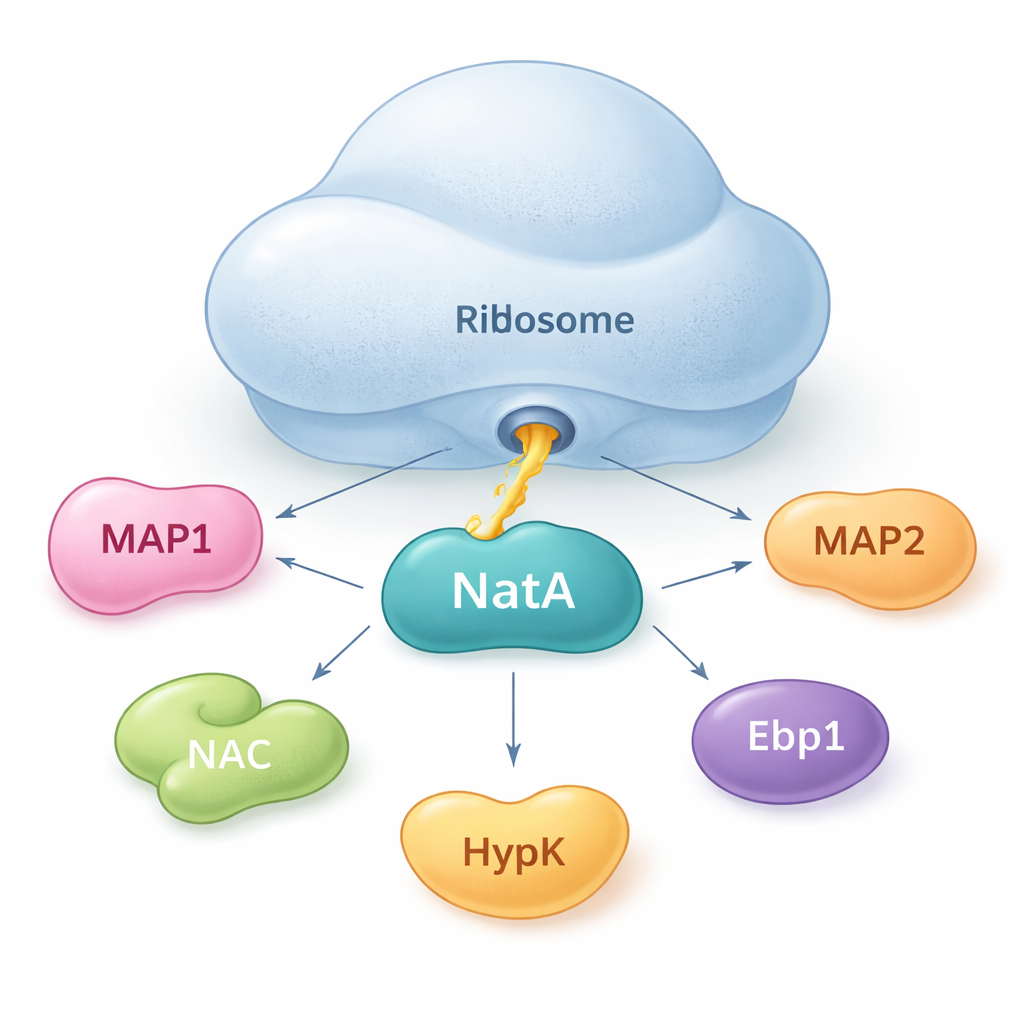
NatA als Treffpunkt für Proteinhelfer
Die Autoren zeigen, dass NatA nicht allein agiert. Stattdessen funktioniert es wie ein Knotenpunkt, der mehrere Helferproteine zusammenbringt, sowohl am Ribosom als auch frei in Lösung. Mittels empfindlicher Bindungsmessungen in Lösung fanden sie heraus, dass NatA enge Komplexe mit MAP1, dem naszierenden Polypeptid‑assoziierten Komplex (NAC), dem regulatorischen Protein HypK und einem weiteren Enzym, Naa50, bilden kann – selbst ohne vorhandenes Ribosom. NAC kann NatA mit MAP1 verbinden, sodass beide Schritte, das Schneiden und das Markieren, in einer einzigen Einheit verknüpft werden. HypK, das normalerweise die Aktivität von NatA dämpft, kann jedoch die Bindung von NAC blockieren. Das legt nahe, dass Zellen NatA je nach Bedarf zwischen einem aktiveren, mit NAC verbundenen Zustand und einem zurückgehaltenen, HypK‑gebundenen Zustand umschalten können.
Ein zweiter Andockplatz direkt am Tunnelausgang
Mit Kryo‑Elektronenmikroskopie, einer Technik, die große Moleküle in nahezu atomarer Detailansicht abbildet, entdeckten die Forscher, dass NatA in zwei verschiedenen Positionen am Ribosom binden kann. Eine bereits bekannte Stelle liegt etwas entfernt vom Tunnelausgang. Die neu entdeckte „proximale“ Stelle platziert den katalytischen Kern von NatA sehr nah an dem Punkt, an dem die wachsende Proteinkette austritt, wodurch die Distanz verkürzt wird, die die Kette zurücklegen muss, um modifiziert zu werden. Überraschenderweise können beide Positionen gleichzeitig besetzt sein, sodass zwei NatA‑Komplexe auf demselben Ribosom sitzen können. Die weiter entfernte Kopie fungiert als Gerüst und Anker, während die proximale Kopie optimal platziert ist, um neue Proteine zu markieren. Die beiden NatA‑Moleküle berühren sich zudem, was darauf hindeutet, dass NatA seine eigenen Duplikate zu multienzymatischen Teams koordinieren kann.
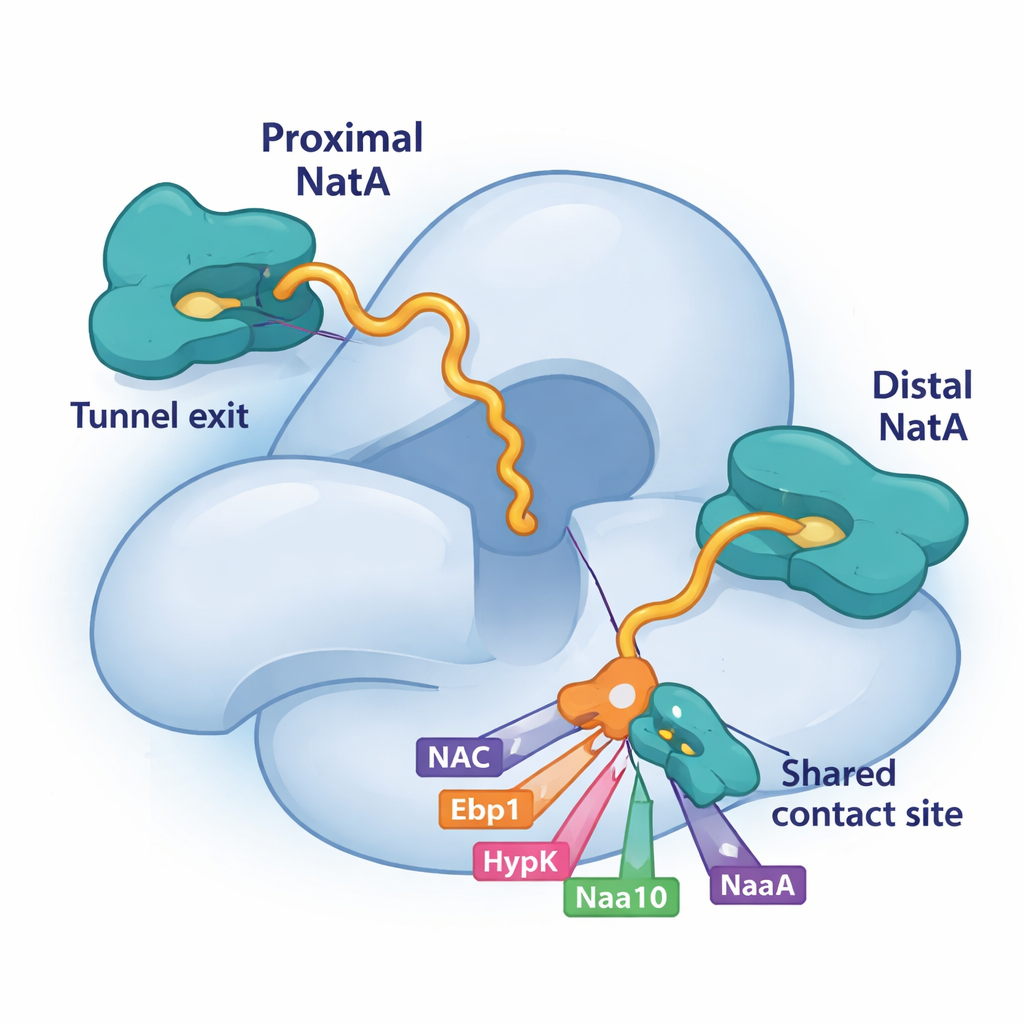
Wettstreit um eine gemeinsame Landefläche auf NatA
Ein wichtiger Teil dieses Puzzles ist eine kleine Rinne auf der großen NatA‑Untereinheit Naa15. Die Studie zeigt, dass vier verschiedene ribosomassoziierte Faktoren – NAC, HypK, Ebp1 und sogar ein Schwanzabschnitt der katalytischen NatA‑Untereinheit Naa10 – kurze Helices verwenden, um genau an derselben Stelle auf Naa15 anzudocken. Weil sie alle auf diese gemeinsame Landefläche angewiesen sind, konkurrieren sie um den Zugriff. Wenn HypK die Stelle besetzt, unterdrückt es nicht nur die Aktivität von NatA, sondern verhindert auch, dass NatA mit NAC paart oder NatA‑NatA‑Dimeren bildet. Wenn stattdessen NAC, das Pseudoenzym Ebp1 oder proximal‑gebundenes Naa10 dort binden, können sie die Position oder die Verbindungen von NatA am Ribosom umgestalten. Diese konkurrierende Bindung gibt der Zelle eine flexible Möglichkeit, jeweils auszuwählen, welche Partner sich um NatA herum zusammenlagern.
Ein Pseudoenzym als Verkehrsregler
Das Protein Ebp1 ist besonders faszinierend. Es ähnelt einem der Methionin‑entfernenden Enzyme, besitzt jedoch keine katalytische Aktivität; es ist ein „Pseudoenzym“. Frühere Arbeiten zeigten, dass Ebp1 am Ribosom nahe dem Tunnelausgang sitzen und ein langes RNA‑Segment einklemmen kann. In dieser Studie finden die Autoren, dass Ebp1, wenn NatA am Ribosom ankommt, seine Position verschiebt, die RNA loslässt und stattdessen mit seiner eigenen Helix dieselbe Bindestelle auf Naa15 besetzt, die auch NAC und HypK nutzen. Diese Umstrukturierung legt nahe, dass Ebp1 als Platzhalter oder Organisator fungieren kann: Es formt die lokale RNA‑Umgebung und übergibt dann die Kontrolle an aktive Enzyme wie MAPs und NatA, ohne selbst direkt chemisch zu wirken.
Warum diese molekulare Verkehrssteuerung wichtig ist
Für Nicht‑Spezialisten mögen die Details zu Helices und Bindestellen abstrakt klingen, doch die Botschaft ist einfach: Zellen betreiben ein hochchoreographiertes, mehrstufiges Qualitätskontrollsystem genau dort, wo Proteine entstehen. NatA sitzt im Zentrum dieses Systems und kann je nach den Faktoren, die Zugang zu einer entscheidenden Andockstelle gewinnen, verschiedene Partner anziehen oder freigeben – und je nachdem, welche Ribosomenstelle NatA einnimmt. Dieses flexible Netzwerk hilft sicherzustellen, dass Abschneiden und Acetylierung für tausende verschiedener Proteine mit der richtigen Reihenfolge und zum richtigen Zeitpunkt erfolgen. Da Fehler in der N‑terminalen Verarbeitung mit Entwicklungsstörungen, Neurodegeneration und Krebs in Verbindung stehen, liefert die Kartierung, wie NatA und seine Partner sich zusammenlagern, Forschern eine klarere Blaupause dafür, wie frühe Proteinverarbeitung gesteuert wird – und wie man eingreifen könnte, wenn sie gestört ist.
Zitation: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Schlüsselwörter: Protein-Qualitätskontrolle, N-terminale Acetylierung, Ribosom-Tunnelausgang, NatA-Komplex, co‑translationelle Modifikation