Clear Sky Science · de
Pflanzliche Fucosyltransferase FUT11 verformt das Zucker-Akzeptor-Molekül, um über einen transienten oxocarbenium-ähnlichen Zwischenzustand zu katalysieren
Wie Pflanzen die Zucker an ihren Proteinen feinabstimmen
Proteine in unseren Zellen und in Pflanzen sind häufig mit komplexen Zuckerketten verziert, die wie Barcodes wirken und steuern, wie die Proteine faltbar sind, wie lange sie stabil bleiben und mit welchen Partnern sie interagieren können. Diese Studie konzentriert sich auf ein pflanzliches Enzym namens FUT11, das ein kleines Zuckerbaustein, Fucose, an diese Ketten anhängt. Indem die Autoren auf atomarer Ebene aufdecken, wie FUT11 arbeitet, zeigen sie einen überraschenden Trick: das Enzym biegt sein Zucker-Akzeptor-Molekül vorübergehend aus der Form, um einen schwierigen chemischen Schritt voranzutreiben. Das Verständnis dieses Prozesses ist nicht nur für die Grundlagenbiologie wichtig, sondern auch für das Design sicherer, in Pflanzen hergestellter Medikamente, die keine unerwünschten Immunreaktionen beim Menschen auslösen.
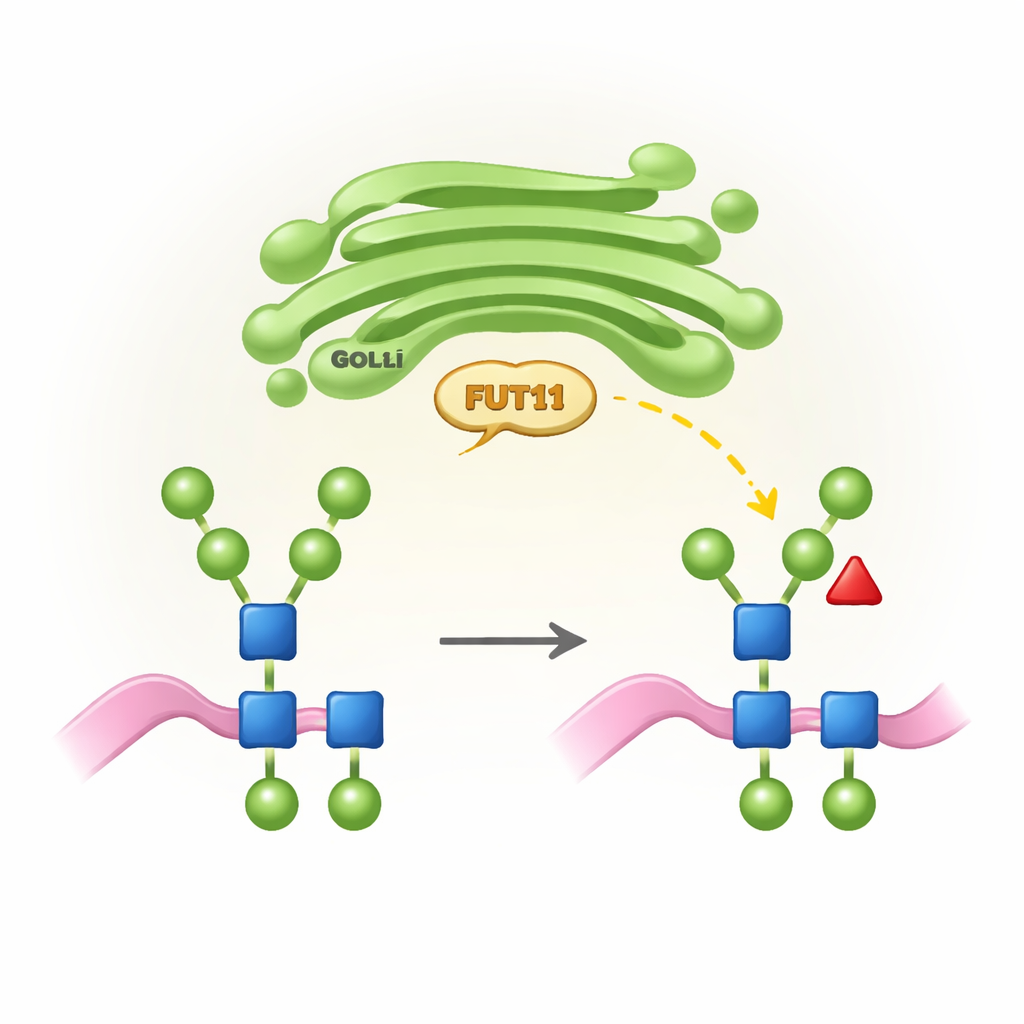
Pflanzenspezifische Zuckerkennzeichen und warum sie wichtig sind
Alle höheren Organismen nutzen einen Prozess namens N-Glykosylierung, um Zuckerketten (N-Glykane) an bestimmte Stellen von Proteinen zu koppeln. Bei Tieren werden diese Ketten im Golgi-Apparat der Zelle zu aufwendigen Strukturen umgebaut, die häufig mit Sialinsäuren enden und ein Kern-Fucose an einer bestimmten Position tragen. Pflanzen folgen jedoch einer anderen „Designregel“: ihre N-Glykane enthalten typischerweise keine Sialinsäure, tragen dafür eine Kern-Fucose an einer anderen Position (als b1,3 bezeichnet) sowie eine zusätzliche Xylose. Diese pflanzenspezifischen Merkmale sind für normales Wachstum und Fortpflanzung essenziell, können aber vom menschlichen Immunsystem als fremd erkannt werden. FUT11 ist eines der Schlüsselenzyme in Pflanzen, das diese Kern-Fucose anbringt, und seine Aktivität beeinflusst sowohl die Pflanzenentwicklung als auch die Wahrnehmung pflanzlich hergestellter Therapeutika im menschlichen Körper.
Kartierung, wo FUT11 an komplexen Zuckerzweigen wirken kann
Um zu verstehen, was FUT11 erkennt, testeten die Forschenden das Enzym auf einem Microarray mit 144 verschiedenen N-Glykan-Strukturen. Sie fanden heraus, dass FUT11 gegenüber einem bestimmten Ast des Zuckerbaums sehr selektiv ist — dem sogenannten b1,3-Arm — der eine bestimmte Baueinheit (ein terminales N‑Acetylglucosamin, GlcNAc) tragen muss, damit die Reaktion ablaufen kann. Gleichzeitig ist FUT11 gegenüber anderen Modifikationen tolerant: Es funktioniert weiterhin, wenn die zentrale Mannose eine pflanzenspezifische Xylose trägt, und sogar wenn bereits eine Fucose an der für Säugetiere typischen Kernposition angefügt wurde. Der gegenüberliegende Ast (b1,6) liegt größtenteils solventexponiert und macht nur schwache Kontakte zum Enzym, was erklärt, warum FUT11 dort eine breite Vielfalt an Modifikationen toleriert. Diese Bindungspräferenzen helfen zu erklären, warum Pflanzen einen charakteristischen Satz von N‑Glykan-Strukturen herstellen, und zeigen, wie FUT11 bei der gentechnischen Manipulation pflanzlicher Zellen genutzt oder vermieden werden könnte.
Ein einzigartiges strukturelles Design zum Erfassen und Positionieren von Zuckern
Mithilfe der Röntgenkristallographie löste das Team die dreidimensionale Struktur von FUT11 gebunden an seinen Zuckerspender (GDP‑Fucose) und einen N‑Glykan-Akzeptor. Das Enzym besitzt eine zweigeschichtige GT‑B-Architektur: eine Lappen hält das GDP‑Fucose, während ein ungewöhnlich ausgebauter Akzeptor-Lappen, einschließlich einer pflanzenspezifischen N‑terminalen Unterdomäne, den N‑Glykan umschließt. Diese zusätzliche Unterdomäne, durch Disulfidbrücken mit dem Rest des Enzyms verbunden, verankert den zentralen Teil des Glykans und hilft dabei, die reaktive GlcNAc‑Einheit dem Donor gegenüber auszurichten. Mutationen an Schlüsselaminosäuren bestätigten deren Rollen: die Veränderung eines einzelnen Glutamats (Glu158) beseitigte die Aktivität, während Änderungen an zwei benachbarten Resten die Fucosylierung in gentechnisch veränderten menschlichen Zellen stark abschwächten. Diese Befunde verbinden strukturelle Schnappschüsse mit realer zellulärer Funktion und zeigen genau, welche Proteinbereiche für Bindung und Katalyse unentbehrlich sind.
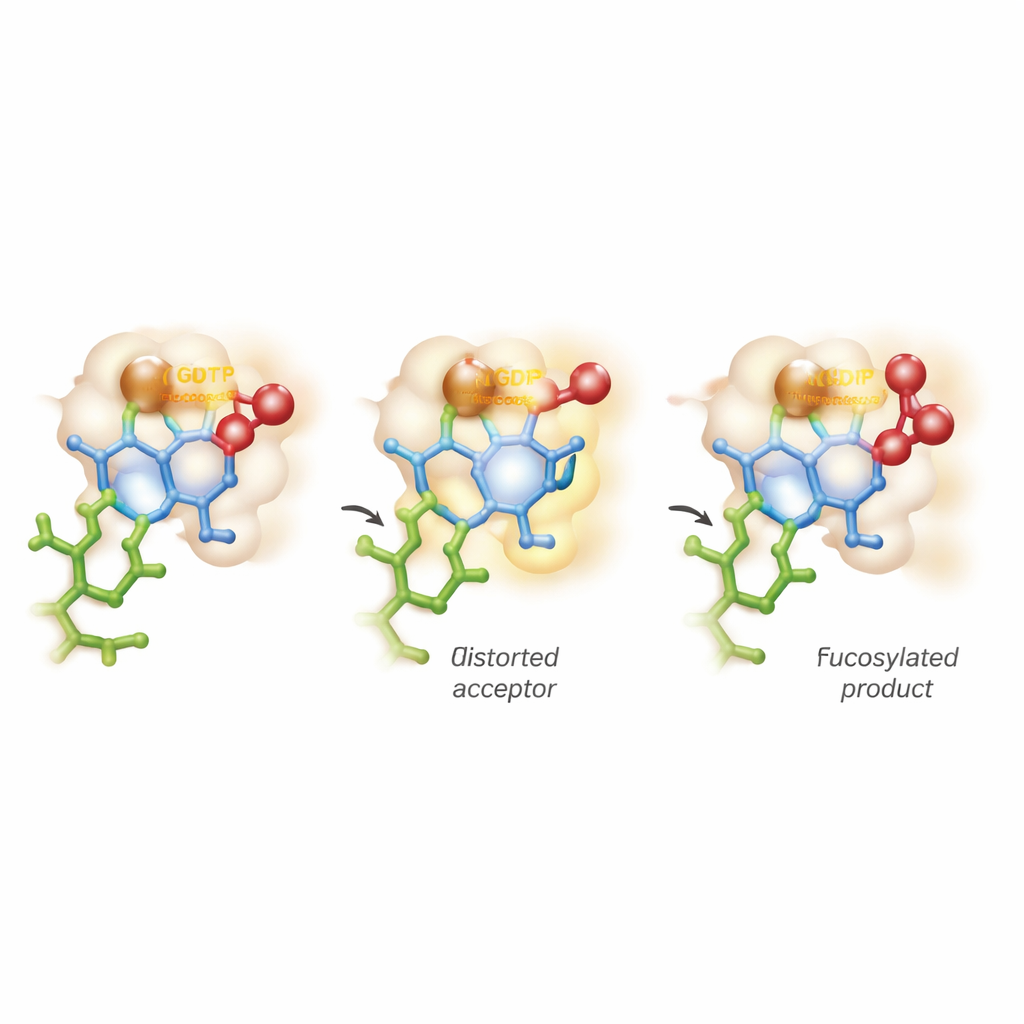
Das Zucker verformen und die Gratwanderung zwischen zwei Reaktionswegen
Die eindrücklichste Einsicht stammt aus fortgeschrittenen Computersimulationen, die Quantenmechanik und molekulare Dynamik kombinieren. Klassische Vorstellungen gehen davon aus, dass das Akzeptor‑Zucker seine stabile, sesselähnliche Gestalt beibehält, während das Enzym lediglich den Donor aktiviert. Hier verhält sich FUT11 aggressiver: Wechselwirkungen, vermittelt durch Glu158, verzerren vorübergehend den innersten GlcNAc‑Ring in eine weniger komfortable, gepuckerte Form. In dieser angespannten Lage ist die kritische Hydroxylgruppe ideal ausgerichtet, um den Fucose‑Donor anzugreifen. Die Berechnungen zeigen, dass beim Aufbrechen der chemischen Bindung zum GDP kurzzeitig ein kurzlebiger, positiv geladener „oxocarbenium‑ähnlicher“ Zustand am Zucker entsteht, bevor die neue Bindung zum Akzeptor vollständig ausgebildet ist. Das bedeutet, dass die Reaktion sich nicht sauber in die Lehrbuchkategorien SN1 oder SN2 einordnen lässt, sondern entlang eines Kontinuums in asynchroner, nahezu schrittweiser Weise verläuft.
Versteckte Flexibilität und evolutionäre Echos
Im Vergleich von FUT11 mit einem verwandten menschlichen Enzym, FUT9, fanden die Autoren, dass das pflanzliche Enzym auch, wenn auch schwach, ein anderes Zucker‑Motiv (LacNAc) modifizieren kann, um eine Struktur zu erzeugen, die als Lewis X bekannt ist. Diese Nebenaktivität ist in Pflanzen wahrscheinlich biologisch nicht relevant, da Lewis X dort normalerweise nicht vorkommt, hebt aber hervor, wie ähnliche Proteingerüste im Laufe der Evolution für unterschiedliche Zucker‑Kontexte umgenutzt werden können. Die Studie legt nahe, dass FUT11 und seine Verwandten einen modularen Rahmen für die Erkennung von N‑Glykanen teilen, mit feinen Anpassungen, die die Spezifität zwischen pflanzlichen Kernen und tierischen Antennen verschieben.
Warum dieser Verformungstrick für Wissenschaft und Medizin wichtig ist
Zusammengefasst zeigt die Arbeit, dass FUT11 mehr tut, als nur zwei Zuckerpartner zusammenzubringen: es verbiegt aktiv das Akzeptor‑Zucker in eine reaktive Pose und kanalisiert die Chemie durch einen flüchtigen, geladenen Zwischenzustand. Für eine nicht‑fachliche Leserschaft bedeutet das: der Zucker am Protein ist kein starrer Andockpunkt, sondern ein flexibler Mitspieler, den das Enzym nach seinen Bedürfnissen formt. Diese neue Sicht auf „konformationelle Katalyse“ hilft zu erklären, wie Enzyme sowohl Geschwindigkeit als auch Selektivität erreichen, und bietet eine Blaupause zur Umgestaltung von Glykosylierungswegen. Praktisch gesehen kann das genaue Wissen darüber, wie FUT11 pflanzliche N‑Glykane erkennt und modifiziert, die gezielte Veränderung von Nutzpflanzen und pflanzenbasierten Produktionssystemen leiten, um immunstimulierende Zuckerstrukturen in Humantherapeutika zu minimieren oder um Designer‑Glykoproteine mit maßgeschneiderten biologischen Eigenschaften zu erzeugen.
Zitation: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Schlüsselwörter: pflanzliche Glykosylierung, Fucosyltransferase FUT11, N-Glykane, Enzymmechanismus, Glycoengineering