Clear Sky Science · de
Proteomische Kartierung von UV-Schadensreparaturpatches deckt Histon-Chaperone mit zentralen Funktionen in der Chromatinreparatur auf
Wie unsere Zellen Sonnenschäden heilen
Jedes Mal, wenn unsere Haut starker Sonnenstrahlung ausgesetzt ist, entstehen unsichtbare Verletzungen in der DNA unserer Zellen. Werden sie nicht behoben, können sich diese kleinen Narben ansammeln und zu Alterung und Krebs beitragen. DNA liegt jedoch nicht nackt vor; sie ist sorgfältig um Proteine namens Histone gewickelt und bildet so das Chromatin, das zur Festlegung der Identität jeder Zelle beiträgt. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wenn Zellen UV-Schäden in ihrer DNA reparieren, wie bauen sie diese komplexe Chromatinarchitektur wieder auf, sodass die Zellidentität erhalten bleibt und nicht durcheinandergerät?
Aufdeckung der verborgenen Reparaturzone
Um dies zu beantworten, mussten die Forschenden gezielt die Stellen im Genom betrachten, an denen die Reparatur aktiv stattfindet, statt den gesamten Zellkern gleichzeitig zu untersuchen. Sie entwickelten einen Ansatz namens IPOND-R, der kurze Abschnitte frisch synthetisierter DNA, die während der Reparatur entstehen, chemisch markiert—im Unterschied zur normalen Replikation des Genoms. Indem sie diese markierten DNA‑„Reparaturpatches“ zusammen mit allen daran gebundenen Proteinen anreicherten und diese Proteine anschließend mittels hochauflösender Massenspektrometrie identifizierten, erstellten sie ein zeitlich aufgelöstes Verzeichnis der Akteure, die bei der Reaktion auf UV‑Schäden in menschlichen Zellen erscheinen und wann sie auftreten. Das lieferte einen unverzerrten Schnappschuss der spezialisierten Proteinumgebung, die sich direkt an Reparaturstellen bildet.
Ein geschäftiges Umfeld am Reparaturgerüst
Die IPOND-R‑Methode zeigte Hunderte von Proteinen, die kurz nach UV‑Exposition auf der zu reparierenden DNA angereichert waren. Wie zu erwarten waren bekannte DNA‑Reparaturfaktoren, die UV‑induzierte Läsionen erkennen und herausschneiden, vorhanden. Das Datenset reichte jedoch weiter und erfasste Proteine, die an Genregulation, Kernarchitektur und vor allem an Chromatinorganisation beteiligt sind. Viele dieser Besucher waren Histon‑Chaperone—spezialisierte Proteine, die Histone auf und von der DNA eskortieren. Der Vergleich früher und später Zeitpunkte zeigte, dass die meisten dieser Chaperone nur vorübergehend auftreten, was auf eine sorgfältig choreografierte Abfolge von Chromatin‑Auseinanderbau und -Wiederaufbau hindeutet, die eng an den DNA‑Reparaturprozess gekoppelt ist.
Neue Lieferanten und Recycler von Histonen
Unter den an Reparaturpatches angereicherten Proteinen stachen zwei Histon‑Chaperone hervor: DNAJC9 und MCM2. Diese Faktoren waren zuvor hauptsächlich für Rollen in der Nähe von Replikationsgabeln bekannt, wo das Genom kopiert wird, waren aber nicht mit UV‑Schadensreparatur in Verbindung gebracht worden. Die Arbeit zeigt hier, dass DNAJC9 ein zentraler Lieferant frischer Histon‑Einheiten (konkret H3–H4‑Paare) während der Reparatur ist. Mithilfe fluoreszenter Marker, die neue von alten Histonen unterscheiden, fanden die Forschenden heraus, dass eine Reduktion von DNAJC9 die Ankunft neu synthetisierter Histonvarianten an UV‑geschädigten Stellen deutlich verringerte, während die grundlegenden DNA‑Reparaturschritte intakt blieben. DNAJC9 wirkt dabei stromaufwärts der bekannten Histon‑Ablagerungschaperone CAF‑1 und HIRA und liefert ihnen neue Histone, ohne deren eigene Präsenz an Schadensstellen zu verändern.
Balance zwischen alten und neuen Bausteinen
Chromatin zu reparieren bedeutet nicht einfach, neue Teile einzusetzen. Die ursprünglichen Histone tragen auch chemische Markierungen, die epigenetische Informationen speichern—Signale, die einer Zelle sagen, welche Gene ein- oder ausgeschaltet bleiben sollen. Die Studie zeigt, dass DNAJC9 außerdem dabei hilft, diese elterlichen Histone zurückzubringen, nachdem sie sich vorübergehend aus beschädigten Bereichen entfernt hatten. Wurde DNAJC9 reduziert, kehrten alte Histone nicht vollständig zurück und die gesamte Histondichte an Reparaturstellen nahm ab. Die Forschenden entdeckten dann, dass DNAJC9 mit MCM2 zusammenarbeitet, um dieses empfindliche Gleichgewicht zu koordinieren: Beide sind nötig für die effiziente Wiederverwertung alter Histone und für die korrekte Ablagerung neuer, selbst in Zellen, die ihr DNA‑Material nicht aktiv replizieren. Das weist auf eine replikationsunabhängige Rolle von MCM2 hin und etabliert eine funktionelle Partnerschaft der beiden Chaperone an Reparaturstellen.
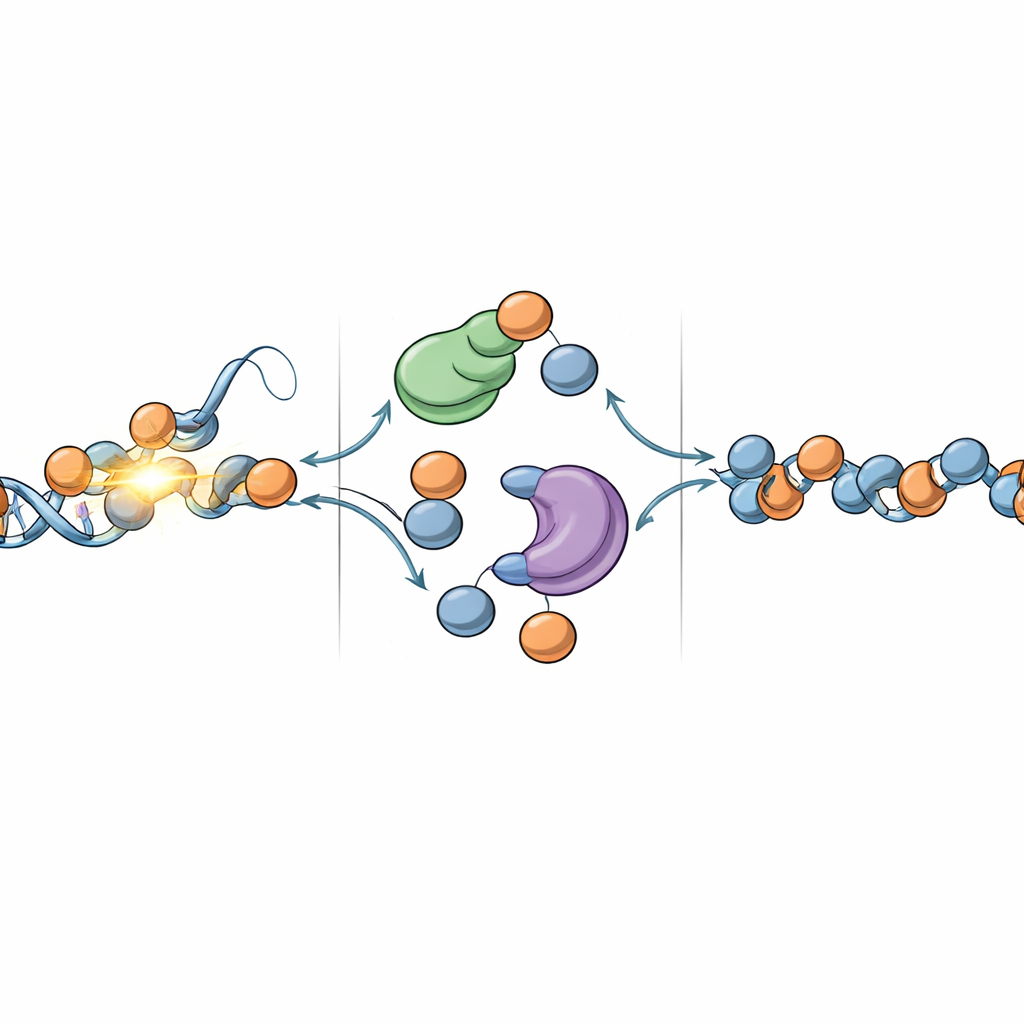
Warum das für Zellidentität und Krankheit wichtig ist
Die Arbeit zeichnet das Bild der Chromatinreparatur als einen doppelseitigen Vorgang: Beschädigte DNA wird repariert, während die umgebende Histonlandschaft mithilfe einer Mischung aus wiederverwendeten und frisch gelieferten Komponenten wiederaufgebaut wird. DNAJC9 und MCM2 stehen an einer Schnittstelle dieses Prozesses und koordinieren den Fluss von alten und neuen Histonen, sodass Zellen nach UV‑Schäden nicht nur den genetischen Code, sondern auch die epigenetischen Muster wiederherstellen können, die ihre Identität ausmachen. Da ähnliche Herausforderungen bei vielen Arten von DNA‑Schäden auftreten, liefert dieses Konzept eine Grundlage dafür, zu verstehen, wie Zellen ein stabiles Epigenom unter Stress bewahren—ein Thema, das zentral ist für Alterung, Krebs und andere Erkrankungen, bei denen die Chromatinregulation gestört ist.
Zitation: Plessier, A., Chansard, A., Petit, E. et al. Proteomic profiling of UV damage repair patches uncovers histone chaperones with central functions in chromatin repair. Nat Commun 17, 2127 (2026). https://doi.org/10.1038/s41467-026-68781-x
Schlüsselwörter: DNA-Schadensreparatur, Chromatin, Histon-Chaperone, UV-Strahlung, Epigenom-Stabilität