Clear Sky Science · de
Stereoselektive Cyan-Verschiebungsreaktion ermöglicht durch photoenzymatische Katalyse
Kleine Teile verschieben, große Wirkung erzielen
Chemiker möchten oft ein Molekül so anpassen, wie ein Ingenieur ein Zahnrad in einer Maschine versetzt—ein kleines Bauteil bewegen, ohne alles neu aufzubauen. Diese Arbeit zeigt, wie Wissenschaftler eine Cyano-Gruppe, ein kleines aber wirkungsvolles chemisches Griffstück, behutsam von einer Position im Molekül zur anderen verschieben können, mithilfe von Licht und spezialisierten Enzymen. Das Ergebnis ist ein präziserer und nachhaltigerer Weg, Moleküle zu konstruieren, die in Arzneimitteln und fortschrittlichen Materialien verwendet werden.
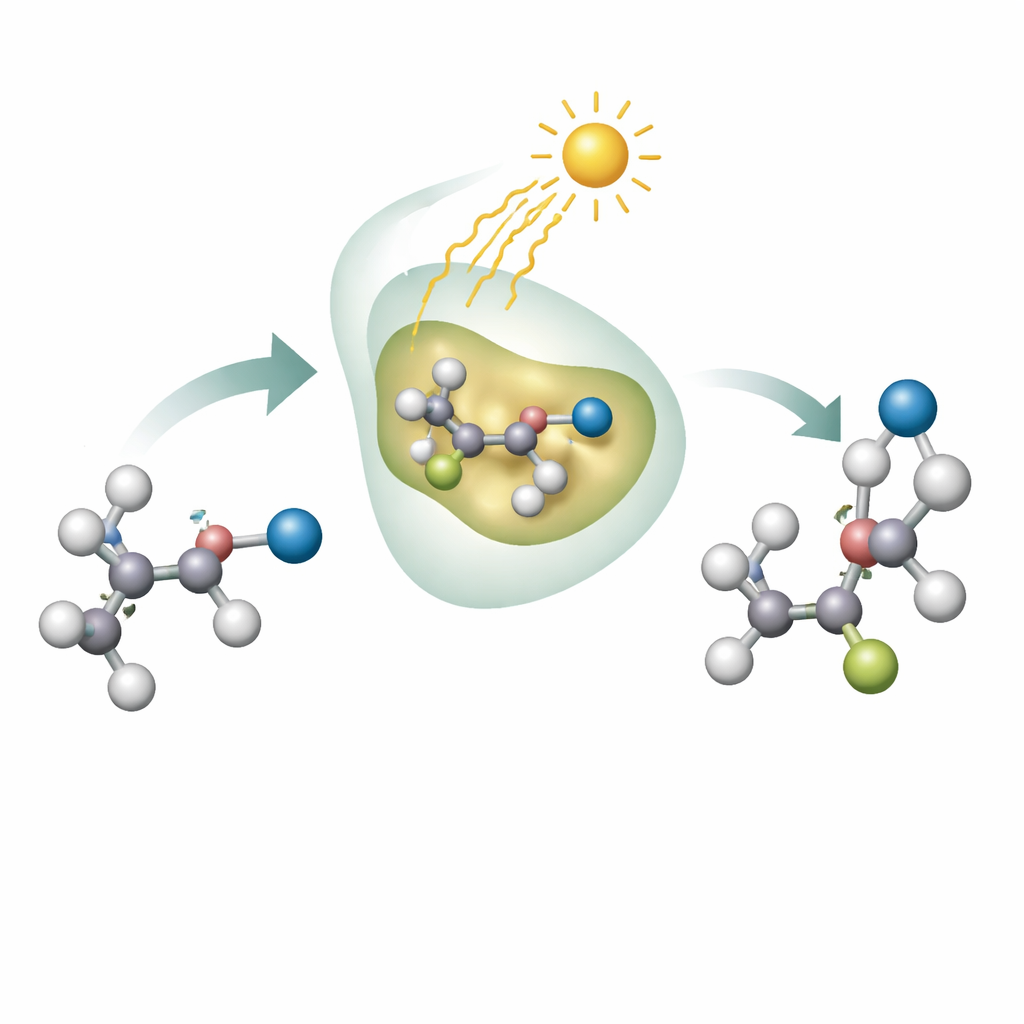
Warum die Verschiebung einer kleinen Gruppe zählt
Das Verhalten eines organischen Moleküls wird maßgeblich durch seine funktionellen Gruppen bestimmt—die kleinen Atomgruppen, die wie Schalter wirken. Das Verschieben einer solchen Gruppe selbst um kurze Strecken entlang einer Kohlenstoffkette kann das Verhalten des Moleküls im Körper oder in einem Material dramatisch verändern. Chemiker wissen, wie man solche Wanderungen herbeiführt, besonders mittels Radikalreaktionen, doch fällt es ihnen häufig schwer, die „Händigkeit“ des Produkts zu kontrollieren. Wie linke und rechte Hände kommen viele Moleküle in spiegelbildlichen Formen vor, und oft ist nur eine davon nützlich oder sicher. Bis jetzt war es sehr schwierig, die bevorzugte Händigkeit während dieser gruppenverschiebenden Reaktionen zu erhalten.
Enzyme und Licht gemeinsam nutzen
Die Autoren kombinieren die Stärken von Enzymen und Licht, um dieses Problem zu lösen. Sie konzentrieren sich darauf, eine Cyano-Gruppe (die CN-Einheit) entlang einer Kohlenstoffkette in sogenannten alkylischen Nitrilen zu verschieben, die wichtige Bausteine sind und in viele andere nützliche Funktionen überführt werden können. Das Team verwendet flavinabhängige Enzyme, eine verbreitete Klasse von Proteinen, die in lebenden Zellen natürlicherweise Redoxchemie betreiben. Wenn der Flavin-Kofaktor in diesen Enzymen blaues Licht absorbiert, gelangt er in einen angeregten Zustand, der stark genug ist, ein Iodatom von einem Ausgangsmolekül abzutrennen und so ein hochreaktives Radikal zu erzeugen. Im engen Inneren der Enzymtasche greift dieses Radikal zur Cyano-Gruppe, löst eine Umlagerung aus, die sie versetzt, und wird anschließend sorgfältig durch Übertragung eines Wasserstoffatoms vom Flavin „abgeschaltet“.
Auf Abruf eine einzige Spiegelbildform herstellen
Eine zentrale Leistung dieser Arbeit ist, dass die Enzyme die Cyano-Gruppe nicht nur verschieben, sondern dies mit ausgezeichneter Kontrolle über die Händigkeit tun. Durch das Screening natürlicher Enzyme und deren anschließende Verfeinerung identifizieren die Forschenden Systeme, die ein Produkt mit sehr hoher Reinheit in einer Spiegelbildform liefern, und andere, die die entgegengesetzte Form bevorzugen. Sie zeigen, dass eine breite Palette von Ausgangsmolekülen mit unterschiedlichen aromatischen Ringen und Seitenketten diese lichtgetriebene Cyano-Verschiebung durchlaufen kann, während eine starke Präferenz für eine einzelne Händigkeit erhalten bleibt. Elektronische Feinabstimmung der Ausgangsmaterialien—das Hinzufügen von Gruppen, die Elektronen spenden oder entziehen—beeinflusst zusätzlich, wie sauber die bevorzugte Händigkeit gebildet wird, und offenbart, wie empfindlich das zugrunde liegende Gleichgewicht der Reaktivität ist.
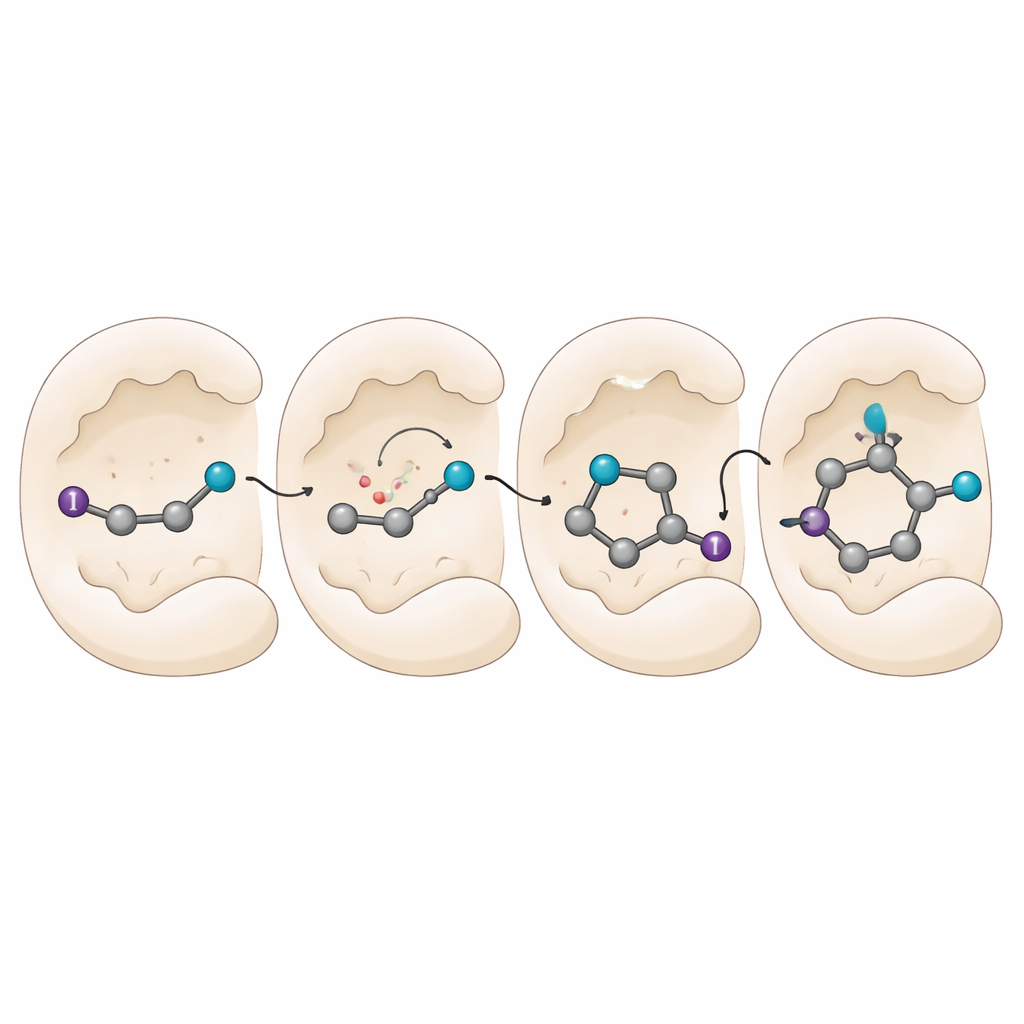
Blick ins molekulare Getriebe
Um zu verstehen, wie die Enzyme eine derart präzise Kontrolle ausüben, führen die Forschenden mechanistische Experimente und Computersimulationen durch. Radikal-Fangtests bestätigen, dass der Prozess tatsächlich über Radikalzwischenstufen verläuft, doch ein Großteil der Chemie ist im Enzym abgeschirmt, sodass äußere Fallen nur schwer eingreifen können. Optische Messungen zeigen, dass Enzym und Substrat einen speziellen lichtabsorbierenden Komplex bilden, der hilft, die Reaktion zu initiieren. Simulationen des Enzym–Radikal-Komplexes zeigen, dass die Cyano-Gruppe durch bestimmte Aminosäuren verankert wird, während der Rest des Moleküls in bevorzugte Orientierungen rotieren kann. Subtile Stapelwechselwirkungen zwischen dem aromatischen Ring des Substrats und bestimmten Aminosäuren neigen das Gleichgewicht zugunsten einer Seite des Radikals, wenn das finale Wasserstoffatom übertragen wird, und fixieren so, welches Spiegelbild entsteht.
Ein neues Werkzeug zum Bau besserer Moleküle
Schließlich führt diese Studie einen neuen Weg ein, Moleküle mit bemerkenswerter Feinheit umzuordnen. Durch den Einsatz photoaktivierter Enzyme, die eine radikalbasierte Cyano-Verschiebung lenken, zeigen die Autoren, dass es möglich ist, eine funktionelle Gruppe zu versetzen und gleichzeitig genau zu bestimmen, welche Spiegelbildform das Produkt annimmt. Für die Arzneimittelentwicklung und die Materialwissenschaft bietet dies eine flexible und umweltfreundlichere Route zu fein abgestimmten Molekülstrukturen und erweitert das Repertoire, das Chemiker nutzen können, um sicherere Medikamente und intelligentere Materialien zu entwerfen.
Zitation: Duan, X., Xu, J., Bai, R. et al. Stereoselective cyano translocation reaction enabled by photoenzymatic catalysis. Nat Commun 17, 2133 (2026). https://doi.org/10.1038/s41467-026-68776-8
Schlüsselwörter: photoenzymatische Katalyse, Wanderung von funktionellen Gruppen, Cyano-Translokation, enzymatische Stereokontrolle, alkylische Nitrile