Clear Sky Science · de
Einzelzell-Exon-Deletion-Profile enthüllen Spleißereignisse, die Genexpression und Zellzustandsdynamik formen
Wie winzige Änderungen an RNA das Verhalten von Zellen verändern können
Unsere Zellen lesen und spleißen ständig RNA-Anweisungen, um zu entscheiden, welche Proteine sie herstellen und wie sie auf Stress reagieren, wachsen oder sich teilen. Diese Studie zeigt, dass das Verändern sehr kleiner Abschnitte dieser RNA-Nachrichten — einzelner Segmente, Exons genannt — die Genaktivität stark umformen und sogar beeinflussen kann, wie Zellen durch den Zellzyklus laufen. Die Arbeit stellt ein leistungsfähiges Werkzeug vor, mit dem Wissenschaftler viele dieser kleinen RNA‑Entscheidungen gleichzeitig, Zelle für Zelle, untersuchen können, und eröffnet neue Wege, Krankheit zu verstehen und Wirkstoffziele zu finden.
Ausgewählte Worte aus dem genetischen Drehbuch herausnehmen
Gene sind als lange DNA-Streifen geschrieben, aber Zellen lesen sie nicht einfach durch. Stattdessen schneiden und kleben sie kleinere Bausteine, Exons genannt, zusammen, um eine RNA-Botschaft zu bilden. Indem sie wählen, welche Exons verbleiben, können Zellen mehrere Proteinversionen aus einem einzigen Gen herstellen, ähnlich wie verschiedene Filmschnitte aus demselben Rohmaterial entstehen. Viele Krankheiten, darunter Krebs und Autismus, stehen im Zusammenhang mit Fehlern in diesem Prozess, doch für die meisten Exon‑Entscheidungen wissen wir noch nicht, welche Funktion sie tatsächlich haben. Die Autoren wollten das ändern, indem sie ein groß angelegtes System bauten, das spezifische Exons aus vielen Genen entfernen kann und dann in Tausenden einzelner Zellen zugleich beobachtet, wie diese Änderungen die interne Verschaltung der Zellen beeinflussen.
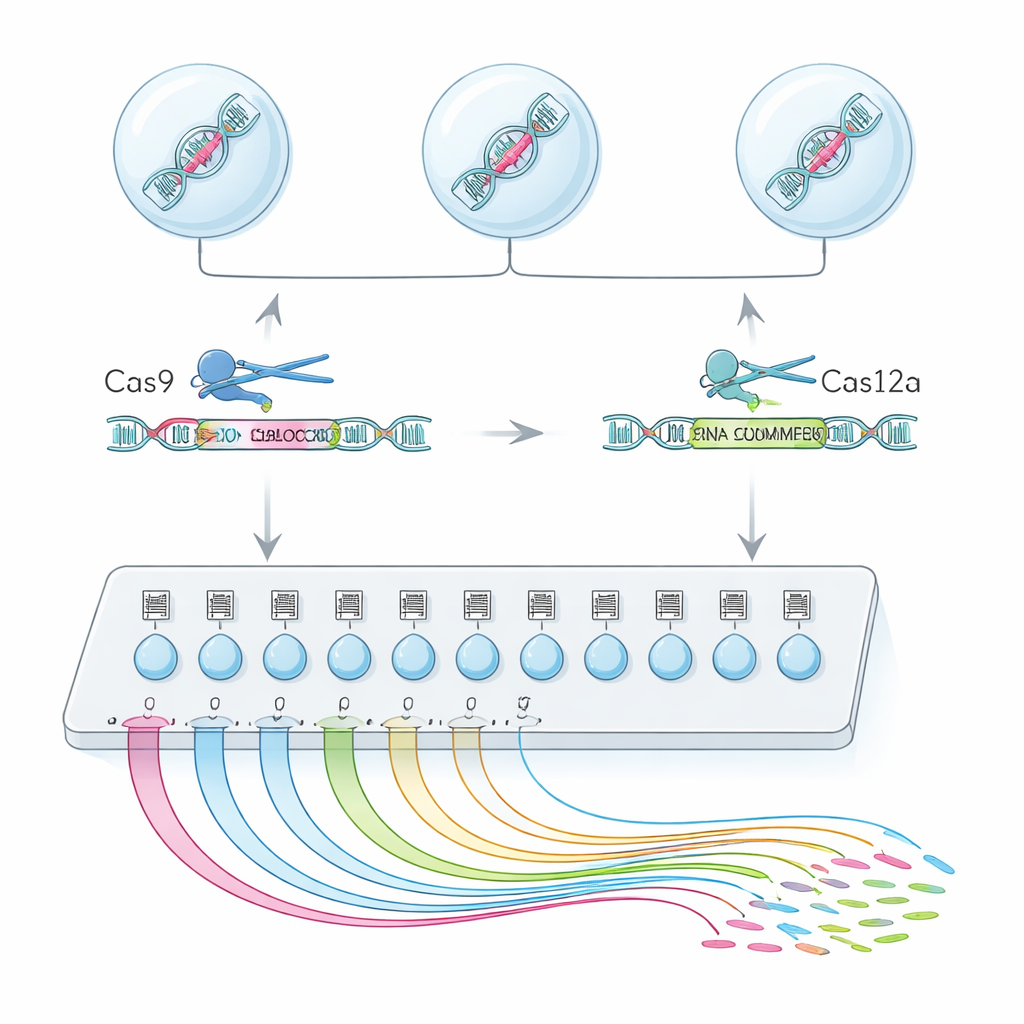
Eine Einzelzell‑„Suchmaschine“ für Exon‑Funktion
Um dies zu erreichen, kombinierte das Team zwei Genom‑Editier‑Enzyme, Cas9 und Cas12a, zu einer Hybridplattform namens CHyMErA. Jedes Enzym wird durch kurze RNA‑„Adressen“ zur DNA geführt. Durch das gezielte Anleiten beider Enzyme, knapp vor und knapp nach einem gewählten Exon zu schneiden, können sie dieses Segment sauber entfernen, während der Rest des Gens intakt bleibt. Die neue Methode, scCHyMErA‑Seq, koppelt dieses präzise Schneiden mit Einzelzell‑RNA‑Sequenzierung. Die RNA jeder Zelle wird in einem Tröpfchen zusammen mit einem Barcode und den Guide‑RNAs, die angeben, welches Exon entfernt wurde, eingefangen. Die Sequenzierung zeigt dann für Zehntausende Zellen sowohl die jeweilige Editierung als auch das detaillierte Muster der aktivierten oder ausgeschalteten Gene.
Das Werkzeug so entwickeln, dass man beide »Klingen« der Schere sieht
Eine zentrale Herausforderung war, die Cas12a‑Guides zuverlässig neben den Cas9‑Guides im selben Einzelzellexperiment zu detektieren. Erste Entwürfe erfassten entweder die Cas12a‑Guide‑RNAs nicht oder beeinträchtigten die Editier‑Effizienz. Die Forscher lösten das, indem sie die Cas12a‑Handle‑Sequenz sorgfältig neu gestalteten, um Abschnitte zu entfernen, die die Transkription vorzeitig abbrachen, und indem sie ein kleines stabilisierendes RNA‑Element sowie einen gezielten Amplifikationsschritt hinzufügten. Diese Anpassungen steigerten die Fähigkeit, beide Guides in etwa 90 Prozent der Zellen zu sehen, bei gleichzeitiger Erhaltung starker Exon‑Deletionen. Mit diesem optimierten Setup screente das Team 224 alternative Exons in 161 menschlichen Genen und profilierte mehr als 200.000 hochwertige Einzelzellen.
Exons entdecken, die Genprogramme und Zellzyklen steuern
Im Vergleich der Genaktivität editierter Zellen mit Kontrollen führten nahezu die Hälfte der getesteten Exons zu erheblichen Verschiebungen in der Expression von Hunderten anderer Gene. Exons aus Genen, die an RNA‑Verarbeitung und Transkription beteiligt sind, neigten dazu, sich zu clustern und ähnliche Expressionsfingerabdrücke zu erzeugen, wodurch gemeinsame biologische Wege wie Ribosomenaufbau oder RNA‑Abbau sichtbar wurden. In einigen Fällen hatte das Entfernen eines einzelnen Exons einen klaren und interpretierbaren Effekt: Das Entfernen eines Exons in den Genen TAF5 oder LSM11 störte die korrekte Verarbeitung von Histon‑RNAs und führte zu einer ungewöhnlichen Anhäufung polyadenylierter Histon‑Botschaften. Der Datensatz hob zudem Dutzende Exons hervor, deren Verlust veränderte, wie viele Zellen in verschiedenen Stadien des Zellzyklus zu finden waren, und verband damit spezifische Spleißereignisse direkt mit Entscheidungen darüber, wann eine Zelle pausiert, ihre DNA kopiert oder sich zur Teilung vorbereitet.
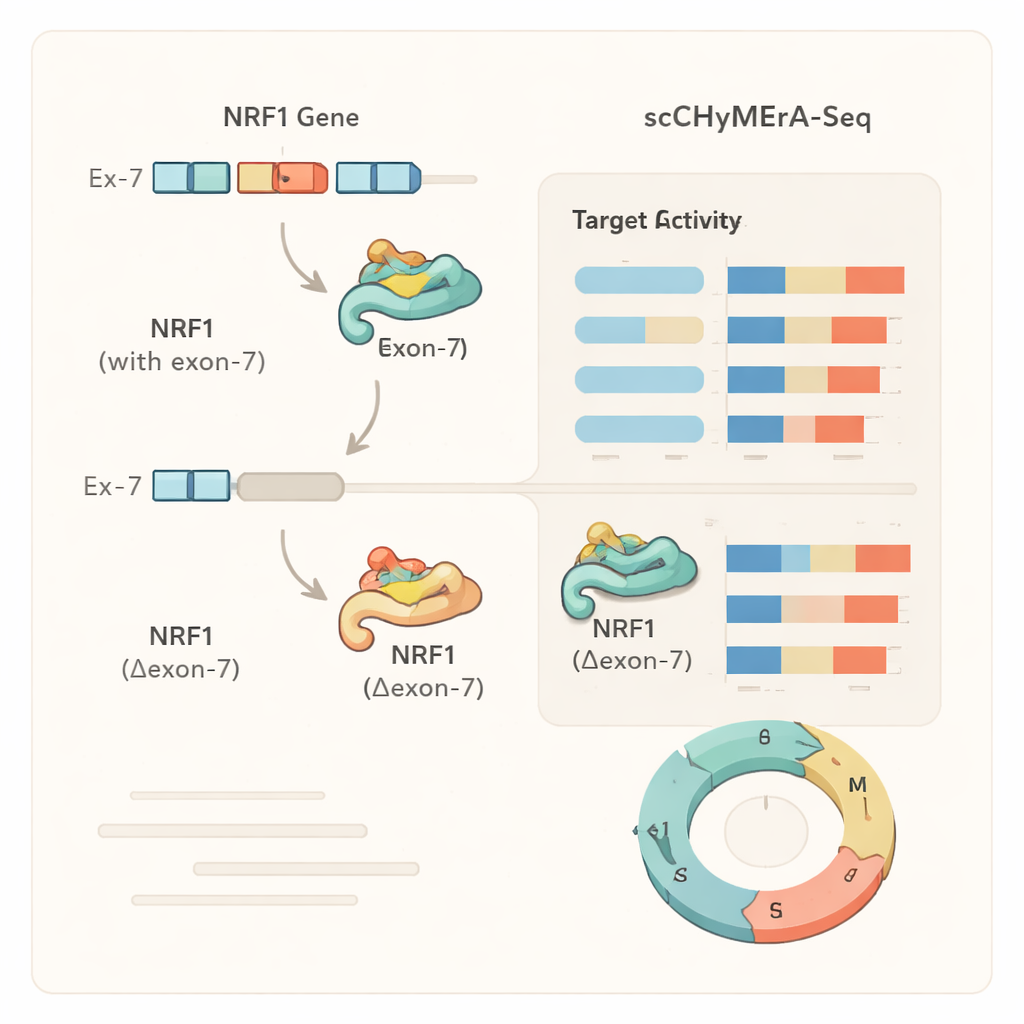
Eine Fallstudie: ein Exon, das einen Masterregulator abstimmt
Ein auffälliges Beispiel war Exon 7 im Gen NRF1, einem Transkriptionsfaktor, der viele Gene der zellulären Energieproduktion kontrolliert. Dieses Exon überlappt teilweise NRF1s DNA‑Bindedomäne. Nach dem Entfernen von Exon 7 veränderte sich die Aktivität von Hunderten NRF1‑kontrollierter Gene, und detaillierte Experimente zeigten, dass das verkürzte NRF1‑Protein deutlich schlechter in der Lage war, seine Zielpromotoren im Genom zu binden. Die Autoren identifizierten außerdem einen spezifischen Spleißregulator, SRSF3, der die Einbeziehung dieses Exons fördert, wodurch sich eine Kette vom Spleißfaktor über eine Exon‑Entscheidung in NRF1 zu umfassenden Änderungen in zellulären Genprogrammen und dem Stoffwechsel ergab. Ähnliche Analysen zeigten, dass bei einigen Genen die Exon‑Deletion einem vollständigen Gen‑Knockout ähnelte, während sie bei anderen eine feinabgestimmte, zustandsabhängige Änderung hervorrief — was darauf hindeutet, dass alternative Exons Proteinverhalten subtil modulieren können, anstatt es einfach an- oder auszuschalten.
Warum das für Gesundheit und künftige Therapien wichtig ist
Für Nicht‑Spezialisten lautet die Kernbotschaft: Zellen verlassen sich auf die Einfügung oder das Überspringen sehr kurzer RNA‑Segmente, um die Funktionsweise von Genen fein abzustimmen, und diese feinen Anpassungen können große Eigenschaften wie Zellteilung oder Stressreaktion verschieben. Die Plattform scCHyMErA‑Seq wirkt wie ein Hochdurchsatz‑Labortest für diese Spleißentscheidungen, indem sie aufzeigt, welche Exons echte funktionelle Auswirkungen haben und wie sie zelluläre Zustände umgestalten. Da viele Krebsarten und neurologische Erkrankungen fehlgespleißte Exons oder veränderte Transkriptionsfaktoren aufweisen, könnte dieser Ansatz helfen, Splice‑Varianten für zukünftige Wirkstoffe oder RNA‑Therapien zu priorisieren und eine Landkarte liefern, wie kleine Änderungen im genetischen Drehbuch zu großen Veränderungen im Zellverhalten führen.
Zitation: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Schlüsselwörter: alternatives Spleißen, Einzelzell-RNA-Sequenzierung, CRISPR-Screening, Genregulation, Zellzyklus