Clear Sky Science · de
Granzyme‑B‑mimetisches Nanozym für zielgerichtete nanovesikuläre Krebsanwendungen
Die körpereigenen Krebskiller neu denken
Unser Immunsystem verfügt über spezialisierte Zellen, die Krebs aufspüren und vernichten können, doch in vielen soliden Tumoren haben sie Schwierigkeiten, einzudringen, ermüden schnell oder richten sich gegen falsche Ziele. Diese Studie beschreibt ein vollständig künstliches, nanoskaliges System, das eine der stärksten Waffen des Immunsystems nachahmt und sie direkt in Tumorzellen liefert. Bedeutsam ist die Arbeit, weil sie auf Behandlungen hinweist, die sich wie lebende Immunzellen verhalten, aber aus stabilen, kontrollierbaren Materialien bestehen statt aus empfindlichen menschlichen Zellen.
Einen natürlichen Assassinen als Vorlage nutzen
Zytotoxische T‑Zellen, eine Art weißer Blutzellen, töten gefährliche Zellen mithilfe eines Enzyms namens Granzyme B. Sobald sie ein Ziel erkennen, machen sie kleine Löcher in dessen Membran und injizieren Granzyme B, das innerhalb der Zelle Selbstmordprogramme aktiviert. Diese Strategie ist die Grundlage moderner Therapien wie CAR‑T‑Zellen, die einige Blutkrebserkrankungen heilen können. In soliden Tumoren versagen CAR‑T‑Zellen jedoch oft, weil sie nicht alle Tumorregionen erreichen, erschöpfen oder versehentlich gesundes Gewebe angreifen. Die Autoren fragten, ob sich ein unbelebtes, nanoskaliges Gerät bauen lässt, das die Schlüsselfunktion von Granzyme B reproduziert — das Auslösen der Selbstzerstörungsmaschinerie der Zelle — ohne auf lebende T‑Zellen angewiesen zu sein.
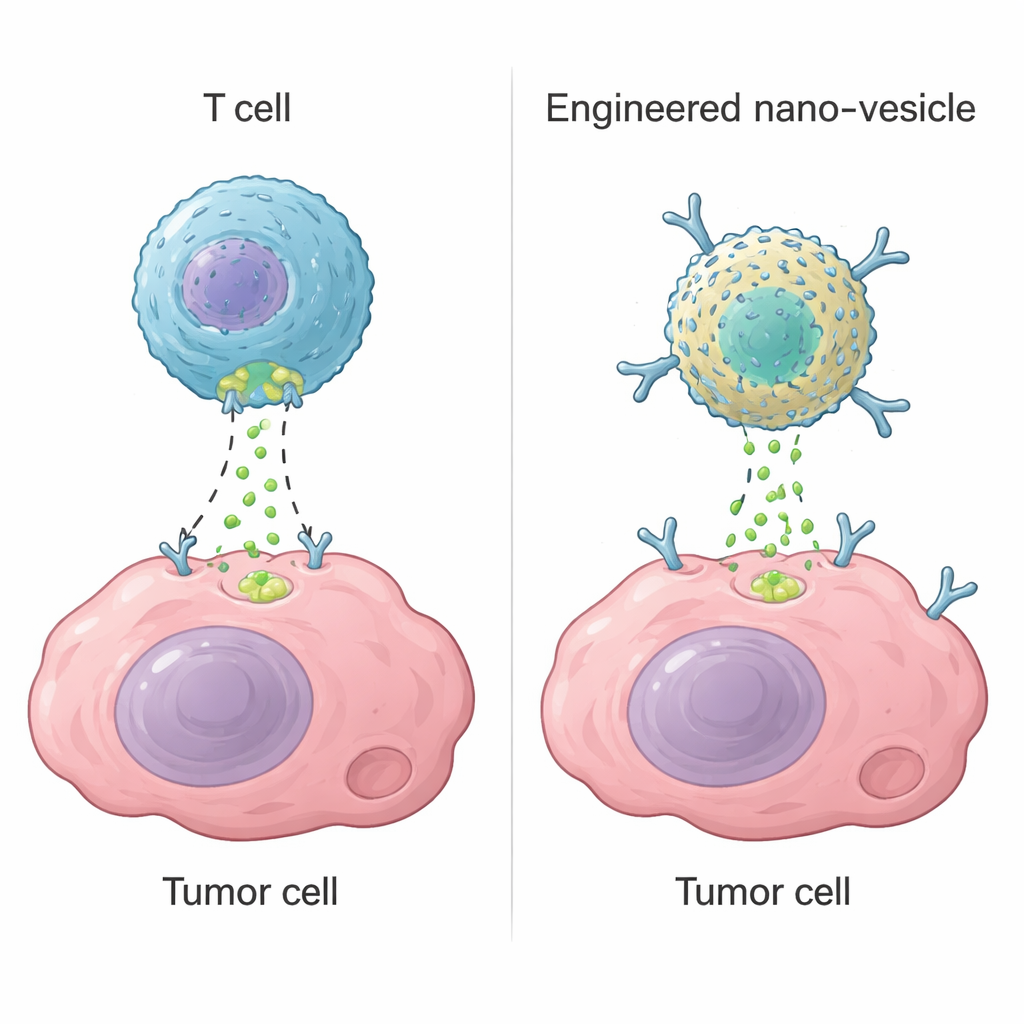
Entwurf eines winzigen künstlichen Enzyms
Das Team startete mit Ferritin, einem natürlichen Protein, das hohle Nanokäfige bildet und sich leicht in großen Mengen herstellen lässt. Durch die Bindung von Palladiumionen an humanes Ferritin schufen sie ein „Nanozym“ mit enzymähnlichem Verhalten. Sorgfältige Strukturstudien zeigten, dass zwei Palladiumatome in eine spezifische Tasche an der Proteinoberfläche eingebettet sind, gehalten von schwefel‑ und stickstoffhaltigen Aminosäuren sowie Wassermolekülen. Dieses binukleare Metallzentrum wirkt als künstliche Schnittstelle, die dieselbe kurze Sequenz erkennt, die auch Granzyme B an einem wichtigen Ziel namens Caspase‑3 verwendet. In Labortests schnitt das Nanozym Caspase‑3 an der richtigen Stelle und aktivierte es, während eng verwandte Proteine ignoriert wurden. Das künstliche Enzym war etwas weniger effizient als das natürliche Granzyme B, zeigte sich jedoch deutlich stabiler über einen weiten Bereich von Temperaturen und pH‑Werten.
Das Nanozym in Tumorzellen einschleusen
Enzyme wie Granzyme B wirken nur, wenn sie ins Innere von Tumorzellen gelangen. Um dies zu erreichen, verpackten die Forschenden ihr Palladium‑Ferritin‑Nanozym in lipidale Nanovesikel — kleine, weiche Bläschen aus fettähnlichen Molekülen. Anschließend beschichteten sie diese Vesikel mit Antikörperfragmenten, die HER2 erkennen, ein Protein, das bei Brust‑ und Blasenkrebs häufig überexprimiert ist. Treffen diese getarnten Vesikel auf HER2‑reiche Zellen, binden sie fest und verschmelzen mit der Zellmembran, sodass die Nanozym‑Fracht direkt in das Zytoplasma gelangt, statt in zelluläre Recycling‑Kompartimente eingeschlossen und verdaut zu werden. Mikroskopische Aufnahmen zeigten die Vesikel, die an der Zelloberfläche verweilten, während das Nanozym in das Zellinnere diffundierte und so die Voraussetzungen für kontrollierte Selbstzerstörung von innen schuf.
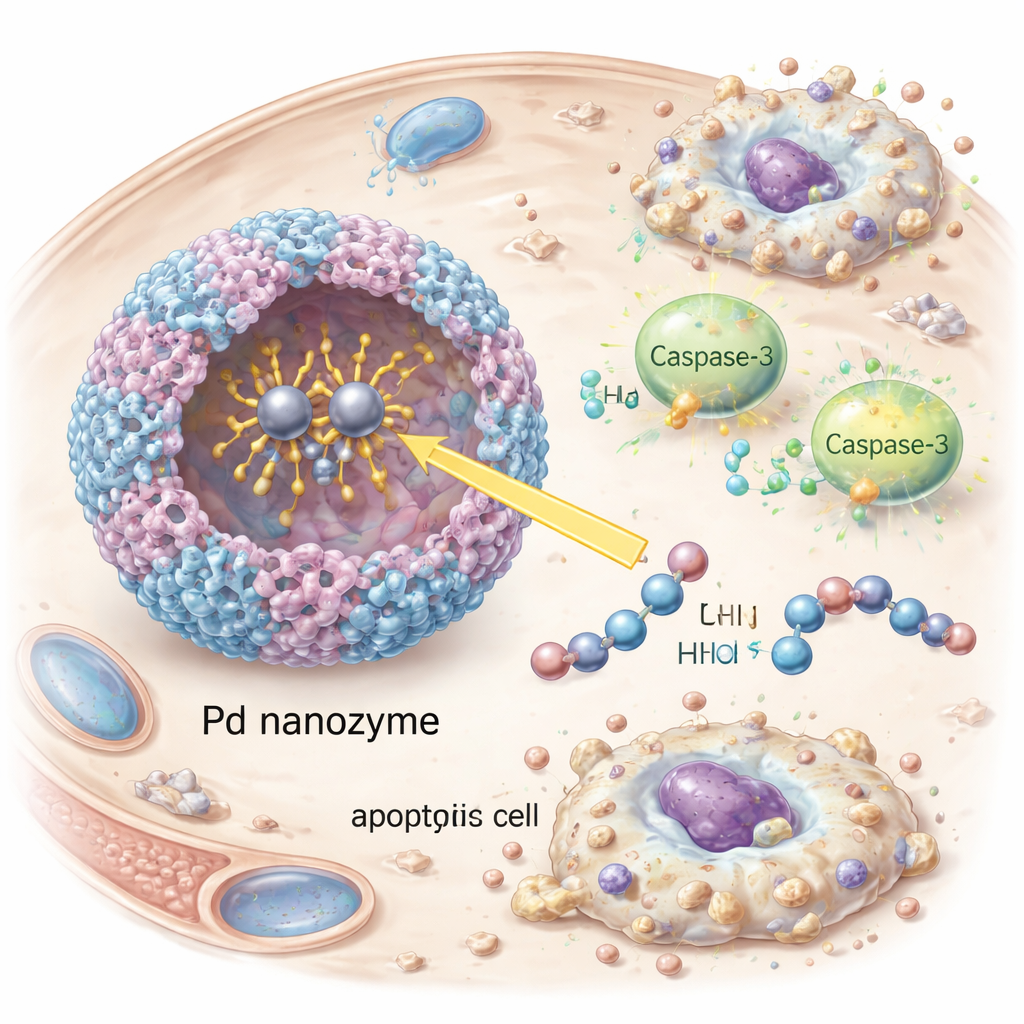
Präzises Auslösen des Zelltods
Einmal in den Krebszellen, schaltete das Nanozym Caspase‑3 ein, eine zentrale Ausführerprotease des programmierten Zelltods. Die Forschenden beobachteten das Auftreten aktivierten Caspase‑3 und seines nachgeschalteten Targets PARP sowie deutliche Anzeichen von Apoptose — Schrumpfen und Fragmentieren der Zellen — in kultivierten HER2‑positiven Tumorzellen. Das Stilllegen von Caspase‑3 mittels RNA‑Interferenz verringerte den Zelltod deutlich, was bestätigte, dass die Wirkung von diesem Signalweg und nicht von unspezifischen Schäden abhängt. In Mäusen mit HER2‑positiven Tumoren zirkulierten die mit Antikörpern dekorierten Vesikel länger im Blut, reichten stärker in die Tumoren hinein und verlangsamten das Tumorwachstum wirksamer als Vesikel ohne zielgerichtende Antikörper oder ohne Nanozym‑Fracht. Wichtig ist, dass die behandelten Tiere in diesen frühen Tests keinen auffälligen Gewichtsverlust, keine Blutauffälligkeiten oder Gewebeschäden in wichtigen Organen zeigten, was auf ein vorteilhaftes Sicherheitsprofil hindeutet.
Was das für die künftige Krebsbehandlung bedeuten könnte
Für Nichtfachleute ist die zentrale Botschaft, dass die Forschenden ein winziges, unbelebtes Gerät gebaut haben, das wie ein wichtiger Teil der krebsbekämpfenden Maschinerie unseres Immunsystems wirkt. Statt lebende T‑Zellen zu konstruieren, gestalteten sie ein stabiles Nanozym, das denselben Selbstzerstörungsschalter in Tumorzellen aktiviert und es in eine intelligente Lieferhülle packte, die bestimmte Krebsarten ansteuert. Obwohl vor einer Anwendung am Menschen noch viel Arbeit nötig ist, bietet der Ansatz eine flexible Plattform: Die Antikörperbeschichtung ließe sich prinzipiell austauschen, um andere Tumormarker anzusteuern, und das künstliche Enzym könnte weiter optimiert werden. Die Studie demonstriert einen vielversprechenden Weg zu zellfreier Immuntherapie, bei der sorgfältig entworfene Nanomaterialien statt lebender Immunzellen zur Jagd auf und Zerstörung solider Tumoren eingesetzt werden.
Zitation: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Schlüsselwörter: Krebsnanomedizin, Immuntherapie, Granzyme B, Nanozym, HER2‑positive Tumoren