Clear Sky Science · de
Durch reaktive Sauerstoffspezies aktivierte bioortogonale Chemie in lebenden Systemen ermöglicht durch boronat‑geschützte Dihydrotetrazine
Stress der Zelle als präziser Schalter
Viele Krankheiten, von Krebs bis zu Herzleiden, zeichnen sich durch Zellen unter oxidativem Stress aus, die hohe Mengen reaktiver Sauerstoffspezies wie Wasserstoffperoxid produzieren. Diese Studie zeigt, wie Chemiker genau diesen Stress als eingebauten Schalter nutzen können, um starke Therapien nur dort zu aktivieren, wo sie gebraucht werden. Indem Wirkstoffkomponenten so entworfen werden, dass sie nur in diesen gestressten Umgebungen reagieren, wollen die Forschenden Tumorzellen abtöten oder schädliche Proteine zerstören und dabei gesundes Gewebe schonen.
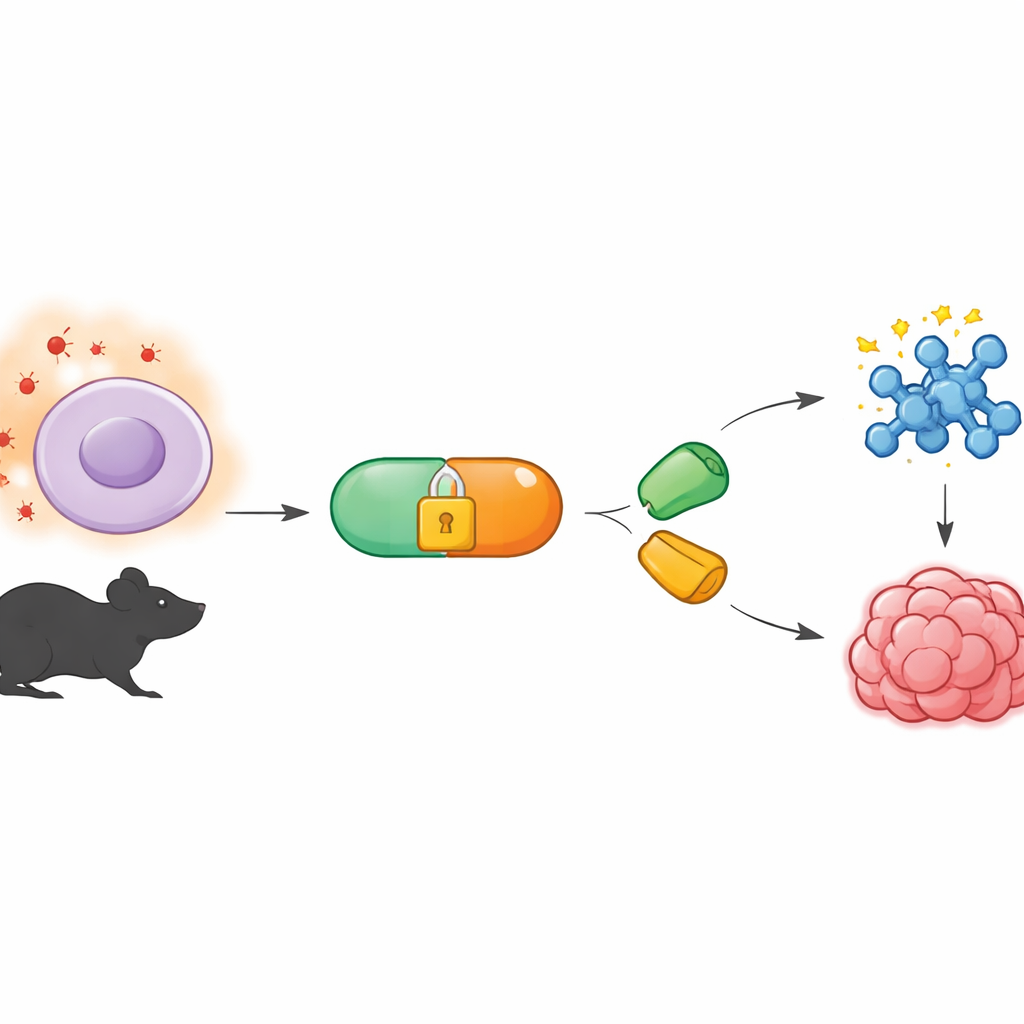
Ein chemisches Werkzeug, das still im Hintergrund wirkt
Die Arbeit baut auf einem Gebiet namens bioortogonale Chemie auf, das Reaktionen entwickelt, die in lebenden Organismen ablaufen können, ohne die normale Biologie zu stören. Eine verbreitete Variante nutzt spezielle Molekülpaare, die wie Puzzleteile schnell zusammenschnappen, selbst im dichten Inneren einer Zelle. Ein Partner, das Tetrazin, reagiert sehr schnell mit einem passenden „Ring“-Partner, dem Dienophil. Bislang wurden viele dieser Reaktionen durch Beleuchtung oder Zugabe von Enzymen gesteuert. Die Autorinnen und Autoren wollten stattdessen ein System, das auf die körpereigenen chemischen Signale hört – konkret auf die ungewöhnlich hohen Konzentrationen reaktiver Sauerstoffspezies, wie sie in Tumoren und anderem erkrankten Gewebe vorkommen.
Aufbau eines ROS‑sensitiven chemischen Triggers
Zu diesem Zweck entwickelte das Team Tetrazin‑Vorläufer, die sie BTz nennen und chemisch „verkleidet“ sind, sodass sie in normalem Gewebe inaktiv bleiben. Die „Verpackung“ besteht aus einer Boronatgruppe, die an eine reduzierte Form des Tetrazins gebunden ist. Wenn Wasserstoffperoxid knapp ist, ist BTz über viele Stunden in Wasser und in Zellkulturen stabil. Ist jedoch Wasserstoffperoxid reichlich vorhanden – in Konzentrationen ähnlich denen in Tumoren – wird die Boronatgruppe oxidiert und durchläuft eine Selbstzerstörungssequenz, die das aktive Tetrazin freilegt. In Reagenzglasexperimenten führte stufenweises Erhöhen der Wasserstoffperoxidkonzentration zu einem entsprechenden Anstieg der Bildung aktiven Tetrazins, was bestätigt, dass die Reaktion selektiv und stark dosisabhängig ist.
Zellstress nutzen, um ein krebsförderndes Protein zu zerstören
Die Forschenden nutzten ihren Schalter zunächst, um eine moderne Wirkstoffstrategie namens gezielte Proteinabbaukontrolle zu steuern. Sie banden BTz an Thalidomid, ein kleines Molekül, das einen Enzymkomplex anwerben kann, der Proteine zur Entsorgung markiert. In Krebszellen blieb dieses BTz–Thalidomid inaktiv, bis die Wasserstoffperoxidkonzentration erhöht wurde; dann öffnete sich die Hülle und bildete ein aktives Tetrazin. Dieses Tetrazin reagierte anschließend mit einem passenden Partner, der an ein BRD4‑bindendes Wirkstoffmolekül gekoppelt war, und assemblierte ein größeres „Chimär“, das das krebsassoziierte Protein BRD4 zur zellulären Abfallmaschinerie zieht. In Lungen‑ und Zervixkarzinom‑Zelllinien sanken die BRD4‑Spiegel stark nur dann, wenn alle Komponenten vorhanden waren und Wasserstoffperoxid verfügbar war; die Blockade reaktiver Sauerstoffspezies verhinderte den Abbau und unterstreicht, dass der Prozess tatsächlich stressaktiviert ist.
Ein toxisches Medikament nur dort freisetzen, wo es gebraucht wird
Anschließend nutzte das Team dieselbe Chemie als präzises Abgabesystem für Doxorubicin, ein wirksames, aber herzschädigendes Chemotherapeutikum. Sie verbanden Doxorubicin mit einem gespanntem Ringpartner, sodass es in einer inaktiven Prodrug‑Form eingeschlossen war. Trifft diese Prodrug in einer wasserstoffperoxidreichen Umgebung auf BTz, reagiert das neu gebildete Tetrazin mit dem Ring in einem „Click‑to‑Release“-Prozess, verbindet die Teile und setzt freies Doxorubicin frei. In in Kultur gezüchteten kolonkarzinomzellen tötete dieses zweistufige System die Zellen fast ebenso effektiv wie das freie Medikament, jedoch nur bei Präsenz von Wasserstoffperoxid; ohne dieses blieben die Zellen größtenteils unversehrt. Eine einfachere, allein auf Wasserstoffperoxid ansprechende Doxorubicin‑Prodrug war in diesen Tests weniger effektiv und weniger selektiv, was den Vorteil der Trennung von Sensorik und Freisetzung in zwei koordinierten Schritten hervorhebt.
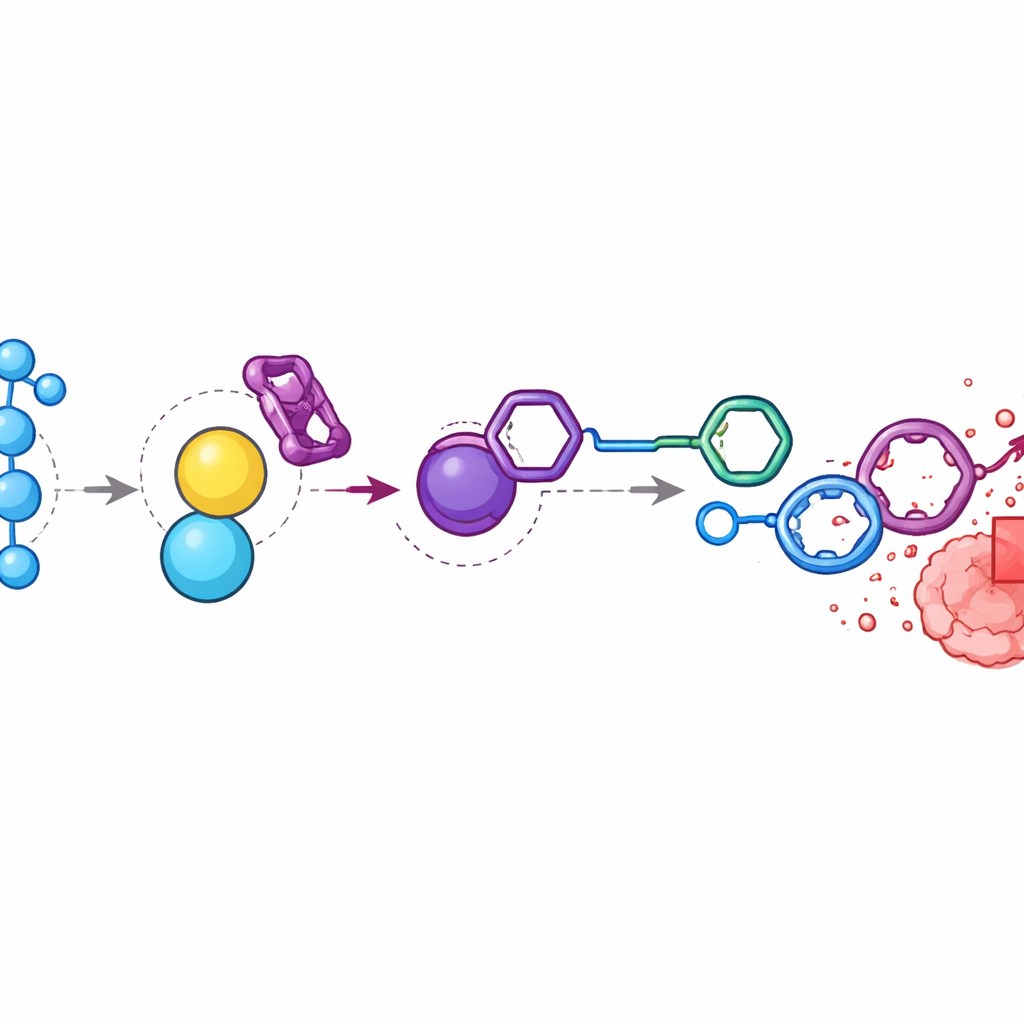
Chemotherapie innerhalb von Tumoren fokussieren
Bei Mäusen mit Kolontumoren fanden die Forschenden, dass die Wasserstoffperoxidspiegel in Tumoren fast neunmal höher waren als im umliegenden Muskelgewebe. Sie injizierten die Doxorubicin‑Prodrug und BTz in einer zeitlich abgestimmten Abfolge, sodass sich beide Komponenten in der Nähe des Tumors ansammelten. Chemische Analysen zeigten, dass die Komponenten im Blutkreislauf und in Organen weitgehend verschwanden, aber innerhalb der Tumoren hohe Mengen freien Doxorubicins entstanden. Im Vergleich zu Tieren, die Standard‑Doxorubicin erhielten, zeigten die mit dem aktivierten System behandelten Tiere ähnliche oder bessere Tumorschrumpfungen, behielten aber ein stabiles Körpergewicht und vermieden die schwere Toxizität, die bei höheren Medikamentendosen auftrat. Als das Team das Wasserstoffperoxid‑Signal durch Injektion von Katalase – einem Enzym, das Wasserstoffperoxid abbaut – unterbrach, wurden Wirkstofffreisetzung und tumorselektive Anreicherung stark reduziert, was bestätigt, dass oxidativer Stress am Tumorort der entscheidende Treiber ist.
Vom Stresssignal zur Präzisionstherapie
Insgesamt zeigt diese Studie eine vielseitige chemische Plattform, die ein Kennzeichen von Krankheit – überschüssige reaktive Sauerstoffspezies – in einen präzisen Steuerknopf für mächtige Reaktionen in lebenden Systemen verwandelt. Indem der reaktive Tetrazin‑Handgriff verschlossen bleibt, bis er auf Wasserstoffperoxid trifft, erlaubt der Ansatz, komplexe Therapien nur dort im Körper aufzubauen, wo sie gebraucht werden, sei es um ein krebsförderndes Protein zu demontieren oder ein toxisches Medikament innerhalb eines Tumors freizusetzen. Da oxidativer Stress auch bei Altern, Entzündungen, Diabetes und neurodegenerativen Erkrankungen eine Rolle spielt, könnten ähnliche stressreaktive Reaktionen schließlich für viele Erkrankungen angepasst werden, bei denen Präzision und Sicherheit oberste Priorität haben.
Zitation: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Schlüsselwörter: bioortogonale Chemie, reaktive Sauerstoffspezies, Tetrazin‑Ligation, gezielte Wirkstofffreisetzung, PROTAC