Clear Sky Science · de
Homotypische, membrangesteuerte elektrochemische mikrofluidische Analyse extrazellulärer Vesikel für präzise Krebsdiagnostik
Die eigene Panzerung des Krebses in ein Diagnostikinstrument verwandeln
Die Membranen, die Krebszellen umgeben, sind mit charakteristischen molekularen „Fahnen“ gespickt. Diese Studie zeigt, wie Forschende diese Panzerung abnehmen, auf winzige Goldchips aufbringen und damit aussagekräftige Partikel aus Blut herausfangen können. Das Ergebnis ist ein hochsensitiver Bluttest, der nicht nur anzeigt, ob Brustkrebs vorliegt, sondern auch, welcher Subtyp—eine Information, die für die Wahl der richtigen Behandlung entscheidend ist.
Warum der Subtyp von Brustkrebs wichtig ist
Brustkrebs ist keine einheitliche Erkrankung. Tumoren werden in Subtypen wie Östrogenrezeptor-positiv (ER+), HER2-positiv und triple-negativ eingeteilt, die unterschiedlich auf Hormontherapie, zielgerichtete Medikamente oder Chemotherapie ansprechen. Heute bestimmen Ärztinnen und Ärzte den Subtyp in der Regel anhand einer Gewebeprobe direkt aus dem Tumor. Dieser Eingriff ist invasiv, kann nicht häufig wiederholt werden und kann Veränderungen übersehen, die im Verlauf der Erkrankung auftreten. Ein blutbasierter Test, der diese Subtyp-Signaturen im Zeitverlauf verfolgen kann, würde es ermöglichen, Therapien früher und gezielter anzupassen.
Winzige Botenstoffe, die im Blut schwimmen
Krebszellen geben ständig nanoskalige Bläschen, sogenannte extrazelluläre Vesikel (EVs), in den Blutkreislauf ab. EVs tragen Proteine, Lipide und genetisches Material, die denen ihrer Mutterzellen sehr ähneln, und sind daher attraktive Kandidaten für „Liquid Biopsies“. Es gibt jedoch eine Herausforderung: EVs verschiedener Brustkrebs-Subtypen können sehr ähnlich erscheinen, wenn man sich nur auf ein oder zwei Proteine konzentriert. Bestehende Tests zielen entweder auf gemeinsame Marker ab—was die Unterscheidung der Subtypen erschwert—or verlassen sich auf komplexe genetische Assays, die langsam sind und irreführende Ergebnisse liefern können. Die Autorinnen und Autoren wollten den umfassenderen molekularen Fingerabdruck auf EV-Oberflächen auf einfache, robuste Weise ablesen.
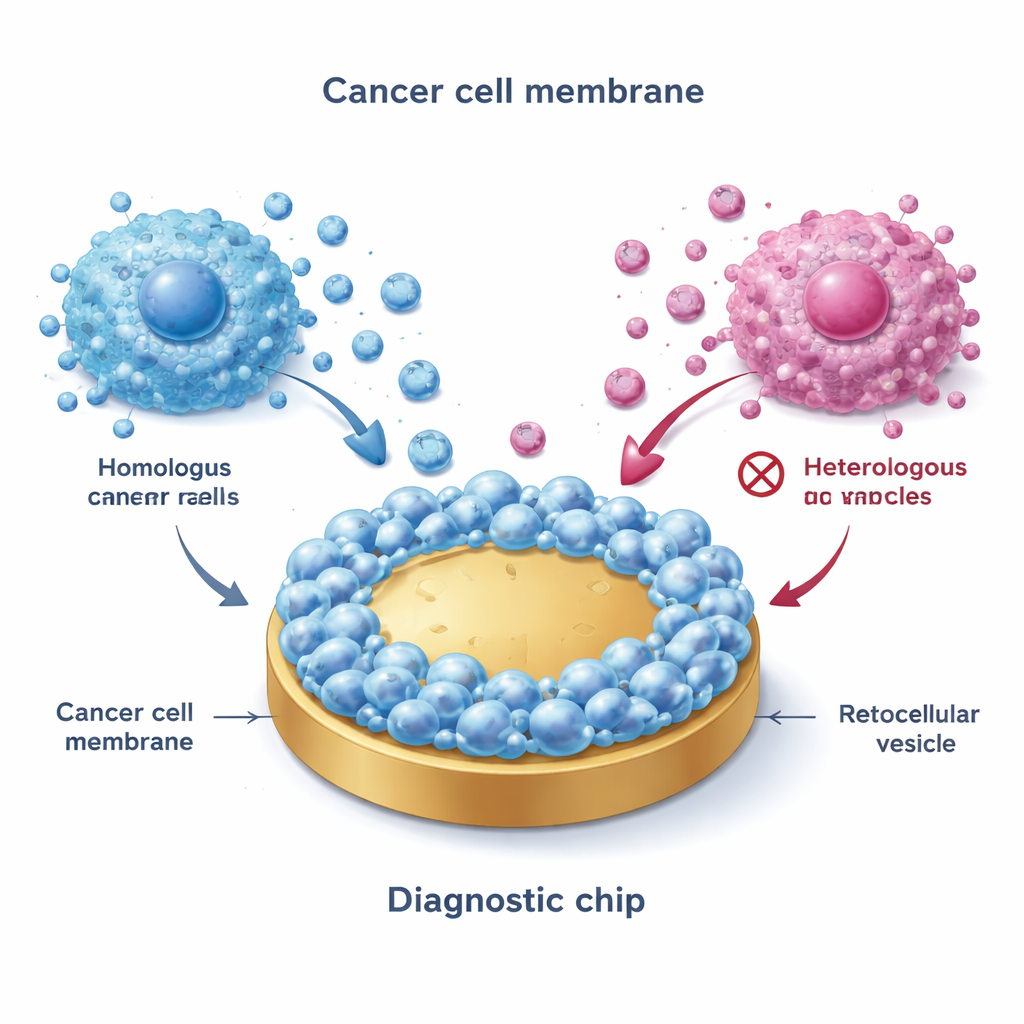
Ein biomimetisches Fangnetz bauen
Das Team begann damit, Membranen aus kultivierten Brustkrebszellen zu gewinnen, die die wichtigsten Subtypen repräsentieren: ER+ (wie MCF-7), HER2-positiv und triple-negativ. Mittels Gefrier–Auftau-Zyklen eröffneten sie die Zellen, isolierten die äußeren Membranen und verschmolzen diese Membranen anschließend mit flachen Goldoberflächen. So entstand eine „biomimetische Schnittstelle“, die die Außenseite der ursprünglichen Krebszellen eng nachahmt. Bemerkenswerterweise haften, wenn EVs über diese beschichteten Oberflächen fließen, nur Vesikel von passenden oder eng verwandten Krebs-Subtypen besonders stark—ein Phänomen, das als homotypische Bindung bezeichnet wird. Fortgeschrittene Bildgebung und elektrische Messungen bestätigten, dass die membranbeschichteten Oberflächen rauer, hydrophiler und deutlich weniger anfällig für unspezifische Adsorption sind als blankes Gold, was sie für saubere Messungen in komplexen Flüssigkeiten wie Blut gut geeignet macht.
Vesikel-Fangen in ein elektrisches Signal verwandeln
Um die Bindung in ein auslesbares Signal zu verwandeln, zielten die Forschenden auf ein reichlich vorhandenes Protein namens CD47 auf der EV-Oberfläche. Sie koppelten CD47-Antikörper über eine kurze DNA-Brücke an Silbernanopartikel und schufen so winzige elektroaktive Marker. Nachdem die membranbeschichtete Oberfläche ihre bevorzugten EVs eingefangen hatte, hefteten sich diese Marker an CD47 auf den gebundenen Vesikeln. Wenn die Probe einer Säurelösung ausgesetzt und anschließend elektrochemisch gemessen wurde, erzeugte das Silber einen scharfen, leicht quantifizierbaren Strom. Die Signalstärke stieg über einen weiten Bereich von EV-Konzentrationen linear an, bis hinab zu nur wenigen Hundert Vesikeln pro Milliliter—deutlich empfindlicher als gebräuchliche Methoden wie ELISA-Kits oder Nanopartikel-Tracking. Jeder Typ von Krebsmembran erzeugte ein starkes Signal nur mit seinen passenden EVs, selbst in Gegenwart von Vesikeln anderer Subtypen, Blutplättchen oder nichtverwandter Zellen.
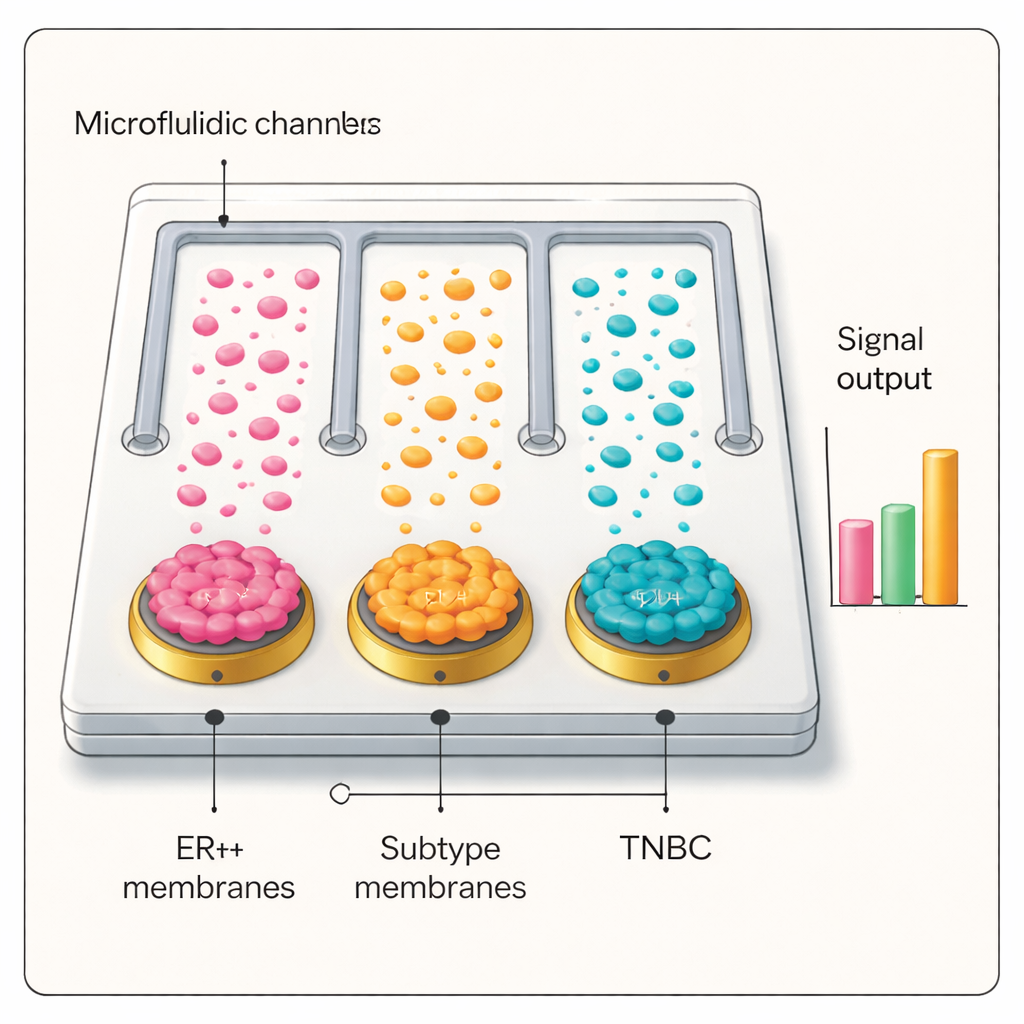
Vom Labortisch zu Patientenproben
Mit dieser selektiven und sensitiven Schnittstelle baute das Team einen mikrofluidischen Chip mit parallelen Kanälen, von denen jeder mit einer anderen Brustkrebszellmembran beschichtet war, plus einer unbeschichteten Kontrolle. Wenn Plasma von Patientinnen und Patienten durch den Chip geleitet und mit den Silber‑Antikörper-Markern geprüft wurde, lieferte nur der Kanal, dessen Membran dem Tumor-Subtyp der Patientin/des Patienten entsprach, ein hohes elektrisches Signal. In verblindeten Tests mit Dutzenden von Personen—darunter ER+- und triple-negativen Brustkrebspatientinnen/-patienten, Personen mit benignen Brustveränderungen, Lungenkrebspatienten und gesunde Freiwillige—untersuchte die Plattform zuverlässig Krebs von Nicht‑Krebs und identifizierte korrekt Brustkrebs-Subtypen. Die diagnostische Leistung entsprach in vielen Fällen der Standardpathologie oder übertraf sie und zeigte Potenzial für die Stadieneinteilung der Erkrankung und die Verfolgung ihres Verlaufs.
Was das für die künftige Krebsversorgung bedeuten könnte
Einfach ausgedrückt haben die Forschenden die äußere Hülle des Krebses in einen hochselektiven Köder für die winzigen Partikel verwandelt, die Tumore ins Blut freisetzen. Indem man das elektrische Signaturprofil des Kanals abliest, der „aufleuchtet“, könnten Ärztinnen und Ärzte eines Tages nicht nur feststellen, ob Krebs vorhanden ist, sondern welcher Typ—und das allein anhand einer Blutprobe. Zwar bedarf das System noch weiterer Verfeinerung—etwa durch Hinzufügen weiterer Marker und Membrantypen sowie die Integration intelligenter Datenanalyse—, doch es weist in die Richtung einer Zukunft, in der routinemäßige, minimalinvasive Bluttests die personalisierte Krebsbehandlung steuern und die Veränderung von Tumoren im Zeitverlauf überwachen.
Zitation: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Schlüsselwörter: Brustkrebs-Subtypen, Liquid Biopsy, extrazelluläre Vesikel, mikrofluidische Diagnostik, Zellmembran-Sensoren