Clear Sky Science · de
Zyklische molekulare Assemblierungen für Golgi‑Bildgebung und -Störung
Das Versandzentrum der Zelle als strategisches Ziel
Im Inneren jeder tierischen Zelle befindet sich der Golgi‑Apparat, eine geschäftige Sortierstation, die Tausende von Proteinen und Lipiden fertigstellt, verpackt und verschickt. Viele Krebszellen sind stark von diesem Knotenpunkt abhängig, um Wachstums‑signale zu modifizieren und Faktoren auszuschütten, die ihr Umfeld formen. Diese Arbeit stellt winzige Designer‑Moleküle vor, die den Golgi gezielt ansteuern, ihn für schnelle Bildgebung sichtbar machen und — bei Umgestaltung — gezielt seine Funktion stören können, um Krebszellen zu schwächen, während bestimmte gesunde Zellen geschont werden.
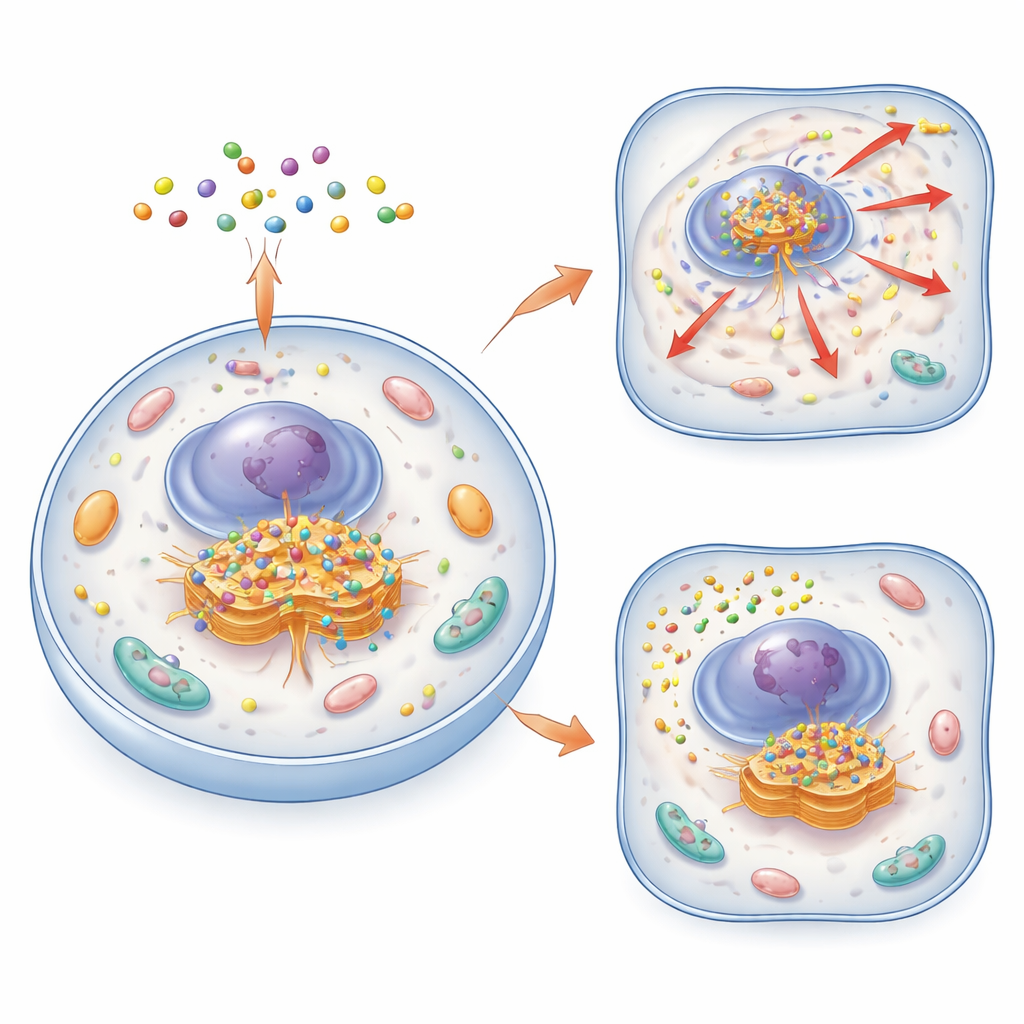
Eine neue Methode, den Golgi zu finden und zu beobachten
Die Autoren entwickelten eine Familie kleiner, intelligenter Moleküle, genannt zyklische molekulare Assemblierungen oder CyMA. Diese Moleküle bestehen aus kurzen Peptiden, die sowohl Zellmembranen passieren als auch zu winzigen Clustern zusammenhaften können. In ihrer „Bildgebungs“‑Variante (CyMA‑i) tragen die Peptide einen fluoreszenten Farbstoff, der hell aufleuchtet, wenn die Moleküle assembliert sind. Einmal in der Zelle schneiden Enzyme eine Schutzkappe vom CyMA‑Vorläufer ab und legen dabei ein reaktives Handle frei. Golgi‑ansässige Enzyme befestigen dann eine Fettsäurekette an diesem Handle, wodurch die Moleküle deutlich klebriger werden und sich genau am Golgi selbst zusammenlagern. Weil dieser Prozess schnell abläuft und die natürliche zelluläre Maschinerie nutzt, können die Forschenden die Form des Golgi in lebenden Zellen innerhalb von Minuten und bei sehr niedrigen Sondenkonzentrationen darstellen.
Ein sinnloser Zyklus, der Moleküle am Golgi fixiert
CyMA sind nicht nur Markierungen; sie sind so entworfen, dass sie an einem „futile cycle“ (sinnloser Zyklus) am Golgi teilnehmen. Eine Enzymgruppe hängt Fettsäureketten an das Peptid, während eine andere Gruppe diese wieder entfernt. Während die Zelle wiederholt diese Ketten an- und abhängt, setzen sich die modifizierten Peptide lokal immer wieder zusammen und bauen sich wieder ab. Dieses ständige Hin und Her fängt einen festen Kern von Assemblierungen auf Golgi‑Membranen ein, lässt aber einzelne Moleküle durchzirkulieren. Die Zelle muss beständig eigene Fettsäure‑Bausteine aufwenden, um diesen Kreislauf aufrechtzuerhalten, wodurch die Assemblierungen quasi „gefüttert“ werden und persistieren. Gleichzeitig können andere Enzyme langsam eine besondere Esterbindung innerhalb der CyMA kappen und sie in wasserfreundlichere Fragmente umwandeln, die wegdiffundieren. Weil einige gesunde Zellen, etwa Leberzellen und bestimmte Immunzellen, reich an solchen Esterasen sind, bauen sie CyMA natürlicherweise besser ab und sind dadurch weniger beeinträchtigt.
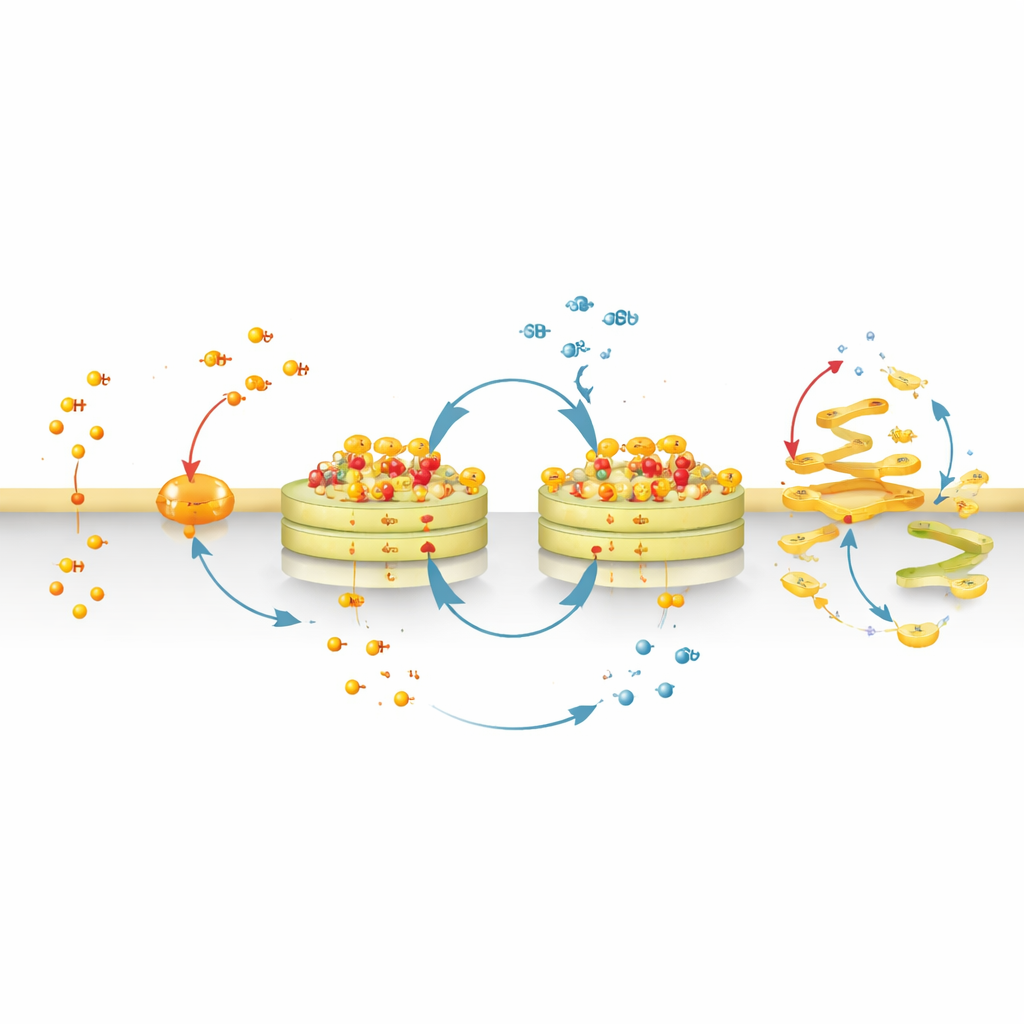
Vom sanften Bildgebungswerkzeug zum Golgi‑Störer
Durch den Austausch des fluoreszenten Farbstoffs gegen eine stärker membranaffine chemische Gruppe wandelte das Team CyMA‑i in CyMA‑d um, eine störende Variante, die nicht mehr leuchtet, aber weiterhin am Golgi zyklisiert und assembliert. Diese Assemblierungen stören physikalisch die Struktur des Golgi und den ständigen Vesikel‑Verkehr zu und von ihm. Proteine, die normalerweise vom endoplasmatischen Retikulum zum Golgi und weiter an die Zelloberfläche transportiert werden, bleiben stecken oder werden fehlgeleitet. Eingangswege — von der Zelloberfläche zurück zum Golgi oder vom Golgi zu anderen Organellen — werden ebenfalls blockiert. Infolgedessen erreichen wichtige Oberflächenrezeptoren und Signalproteine entweder nicht ihre Bestimmungsorte oder sammeln sich an falschen Stellen innerhalb der Zelle an.
Verwirrung von Zell‑Signalen und sekretorischen Nachrichten
Im Golgi erhalten viele Proteine entscheidende Fertigstellungen, wie Zuckerketten und Lipidanhänge. CyMA‑d‑Assemblierungen reduzieren die korrekte Lipidierung und Glycosylierung zahlreicher Proteine, darunter bekannte Krebs‑Treiber wie Ras und wichtige Rezeptor‑Tyrosinkinasen. Diese Veränderungen entgleisen wachstumsfördernde Signalwege wie AKT und mTOR. Gleichzeitig wird die sekretorische Leistung der Zelle gedämpft: Wichtige Faktoren wie TGF‑β1 und VEGF, die Tumoren nutzen, um Immunreaktionen zu unterdrücken und Blutgefäßwachstum zu fördern, werden nicht mehr effizient freigesetzt. Der Stress dieses Zusammenbruchs führt zu verdrehten Netzwerken des endoplasmatischen Retikulums, veränderten Mitochondrien, gestauter Autophagie (dem Recycling‑System der Zelle) und einer Zunahme beschädigter, ubiquitinierter Proteine, was zusammen Krebszellen in Richtung Zelltod treibt.
Selektiver Druck auf Tumoren und therapeutische Perspektiven
Da CyMA‑d auf einem gemeinsamen Satz von Enzymen und Metaboliten beruhen, die viele Krebszellen überbeanspruchen, können sie eine breite Palette von Tumortypen abtöten, einschließlich medikamentenresistenter Ovarialkrebsmodelle, und das bei sehr niedrigen Dosen. Zellen mit hohen Pegeln bestimmter Esterasen bauen CyMA‑d jedoch schneller ab und werden weniger geschädigt, was eine eingebaute Selektivität bietet. In dreidimensionalen Tumorsphäroiden, patientenabgeleiteten Kulturen und Mausmodellen verkleinern CyMA‑d Tumoren, reduzieren Metastasen und verringern Flüssigkeitsansammlungen im Bauchraum. In Kombination mit Immun‑Checkpoint‑Therapien verstärken sie die Tumorkontrolle und das Überleben weiter. Im Kern zeigt diese Arbeit, dass das Aufbauen dynamischer Materialien innerhalb des Golgi — statt das Anvisieren eines einzelnen Proteins — mehrere krebsrelevante Prozesse gleichzeitig lahmlegen kann.
Was das für künftige Behandlungen bedeutet
Für Nicht‑Spezialisten ist die Kernidee, dass die Autoren den Golgi vom passiven Beobachter in ein aktives therapeutisches Ziel verwandelt haben. Indem sie die zelleigenen Enzyme nutzen, um winzige Moleküle an diesem zentralen Knoten zu assemblieren und zu recyclen, können sie ihn entweder harmlos hervorheben oder seine Funktion allmählich überlasten. Diese doppelt nutzbare Plattform deutet auf eine neue Art von Therapie hin: Statt ein Medikament gegen ein einzelnes Protein zu entwerfen, könnten wir kleine Vorläufer konstruieren, die Zellen in selbstorganisierende Materialien verwandeln, die gesamte Kommunikations‑ und Transportnetzwerke stören, von denen Tumoren zum Wachsen und Ausbreiten abhängen.
Zitation: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Schlüsselwörter: Golgi‑Apparat, molekulare Assemblierungen, Proteintransport, Krebstherapie, Organelzielsteuerung