Clear Sky Science · de
Endotheliales PDLIM5 fördert die Filopodienbildung von Spitzt-Zellen und die Tumorangiogenese durch Regulierung der ACTN1/ACTN4-abhängigen Aktinbündelung
Wie Krebs Blutgefäße kapert
Krebs kann nicht über eine winzige Zellansammlung hinauswachsen, ohne die umliegenden Blutgefäße dazu zu bringen, Sauerstoff und Nährstoffe zu liefern. Diese Studie zeigt, wie ein wenig untersuchtes Protein in der inneren Auskleidung von Blutgefäßen Tumoren dabei hilft, neue, abnorme Gefäßverzweigungen zu bilden. Das Verständnis dieses Prozesses könnte Wege für gezieltere Therapien öffnen, die Tumoren nicht nur aushungern, sondern auch die Wirksamkeit der Immuntherapie verbessern.
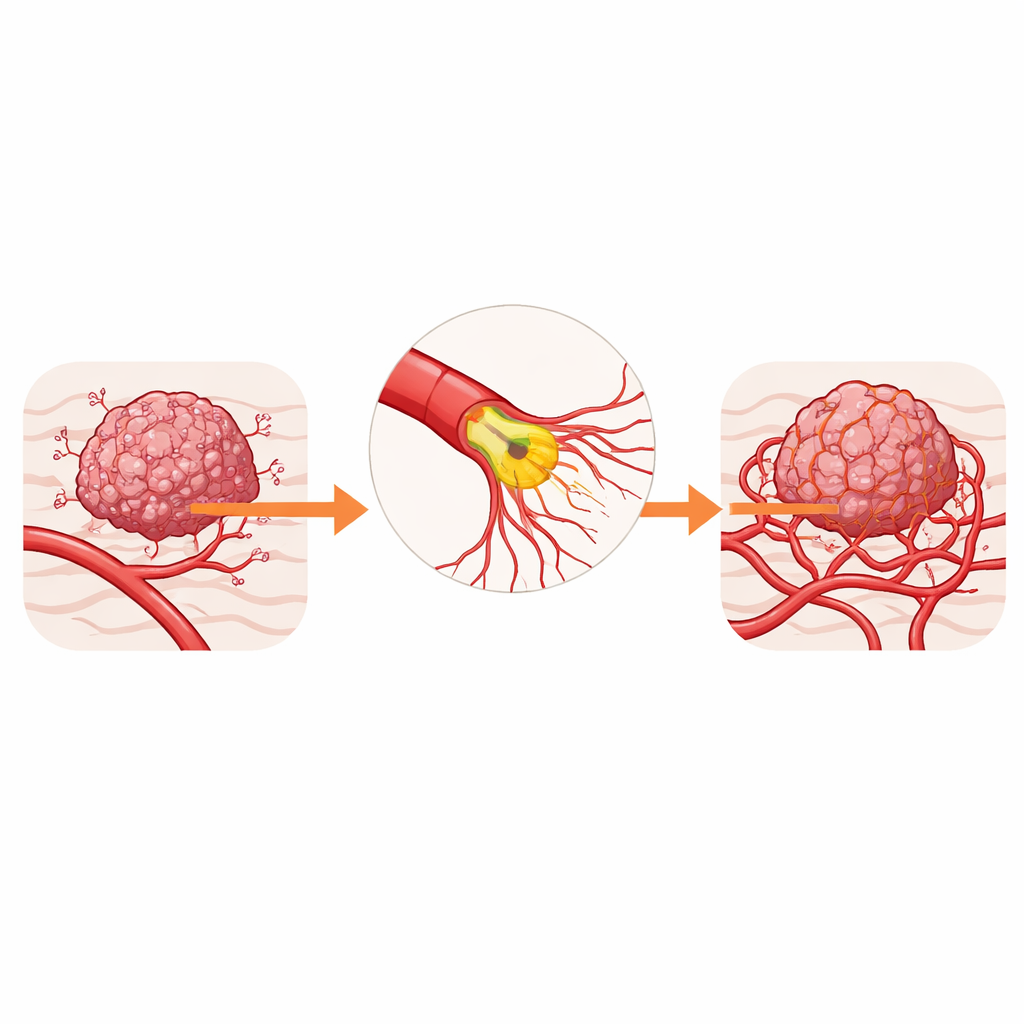
Die verborgenen Architekten der Tumorblutzufuhr
Die Gefäße, die Tumoren versorgen, bestehen aus spezialisierten Zellen, den Endothelzellen, die das Innere der Gefäße auskleiden. An der vordersten Spitze jedes neuen Gefäßastes sitzt eine »Spitzt-Zelle«, die lange, fingerartige Fortsätze aussendet, sogenannte Filopodien. Diese Fortsätze nehmen chemische Signale aus dem Tumor wahr und lenken das Wachstum der neuen Sprosse in sauerstoffarme Bereiche. Bei vielen Krebsarten gerät dieses Sprosswachstum außer Kontrolle, wodurch undichte, verdrehte Gefäße entstehen, die die Hypoxie verschärfen und es für Medikamente und Immunzellen schwieriger machen, den Tumor zu erreichen.
Ein Protein, das das Sprossen verstärkt
Beim Untersuchen einzelner Zellen aus menschlichen Lungenkarzinomen stellten die Forscher fest, dass tumornahes Endothel einen Satz von Genen stark aktiviert, die das innere Gerüst der Zelle steuern, insbesondere ein Protein namens PDLIM5. PDLIM5 war in Tumorgefäßen stärker vorhanden als in normalen Gefäßen, und Patienten, deren Tumorgefäße mehr PDLIM5 exprimierten, hatten tendenziell eine kürzere Überlebenszeit. In Mausmodellen mehrerer Krebsarten beschleunigte eine Erhöhung von PDLIM5 in der Gefäßauskleidung das Tumorwachstum und führte zu dichteren Gefäßnetzen, was darauf hindeutet, dass dieses Protein ein starker Treiber des Wachstums von Tumorblutgefäßen ist.
Wie PDLIM5 zelluläre »Fühler« aufbaut
Um zu untersuchen, wie PDLIM5 das Verhalten von Gefäßen beeinflusst, nutzte das Team experimentelle Modelle, in denen neues Sprosswachstum detailliert beobachtet werden kann, zum Beispiel wachsende Gefäße in der Mausretina und dreidimensionale Kulturen von Endothelzellen. Wurde PDLIM5 gezielt aus Endothelzellen entfernt, gingen die Sprosse langsamer voran, es gab weniger Spitzt-Zellen und deutlich weniger Filopodien. Auf mikroskopischer Ebene stellte sich heraus, dass PDLIM5 zwei wichtige aktinbündelnde Proteine, ACTN1 und ACTN4, mit langen Aktinsträngen verbindet, die das innere Gerüst der Zelle bilden. Diese Brückenfunktion hilft, Aktinstränge zu steifen Bündeln zu packen, die die Filopodien stützen. Mutationen an zwei kritischen Stellen von PDLIM5 (S593 und F596) unterbrachen diese Verbindung, schwächten die Aktinbündelung und verhinderten, dass PDLIM5 das normale Sprosswachstum wiederherstellen konnte, womit gezeigt wurde, dass dieser molekulare Kontakt für den Aufbau der »Fühler« der Spitzt-Zelle unerlässlich ist.
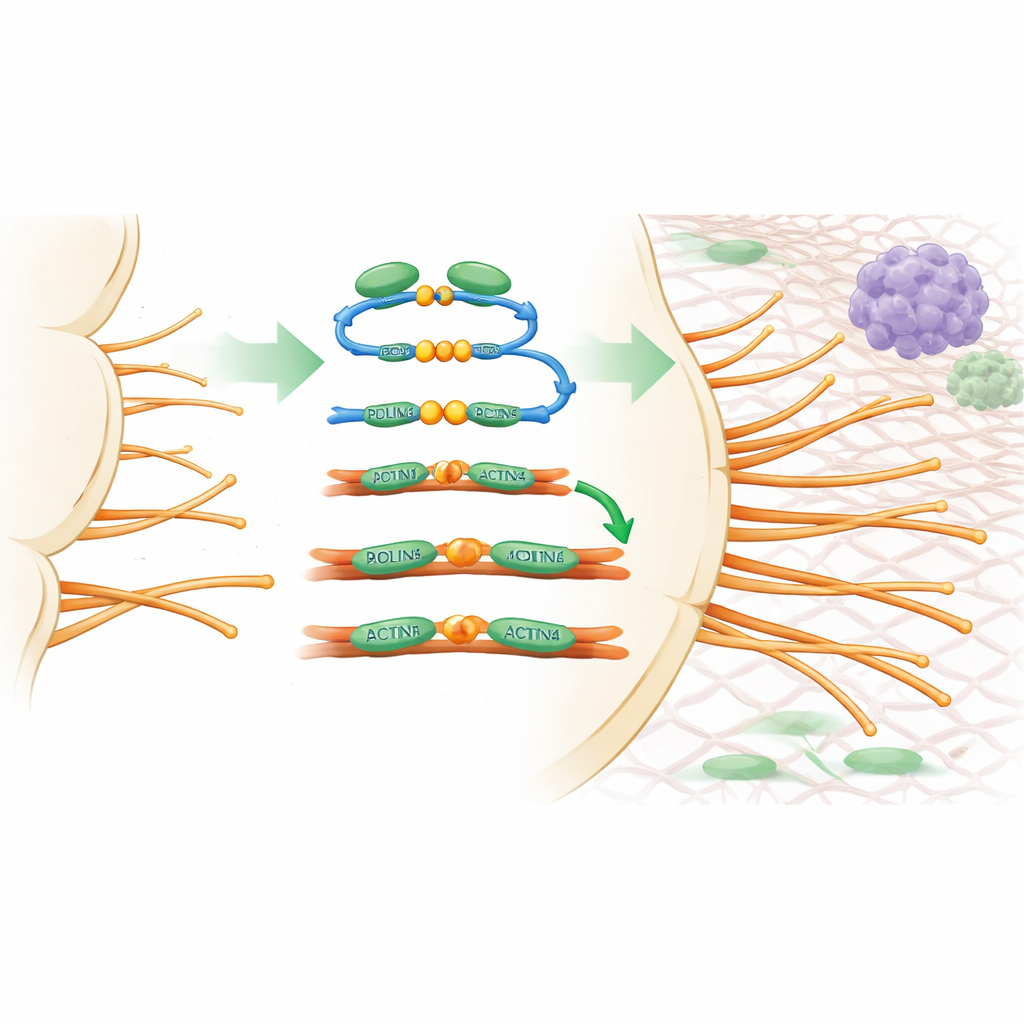
Umstrukturierung von Tumorgefäßen zugunsten des Immunsystems
Überraschenderweise bewirkte das Blockieren von PDLIM5 in der Gefäßauskleidung mehr als nur eine Verlangsamung des Tumorwachstums. Tumorgefäße wurden regelmäßiger geformt, weniger durchlässig und besser von stabilisierenden Stütz-Zellen bedeckt. Dadurch verbesserte sich die Sauerstoffzufuhr und die Bereiche mit starker Hypoxie schrumpften. Diese »normalisierteren« Gefäße ermöglichten einen stärkeren Eintritt von T-Zellen in den Tumor. Der Verlust von PDLIM5 veränderte außerdem die Anordnung von Adhäsionsmolekülen auf Endothelzellen, sodass T-Zellen leichter an Gefäßwände andocken und in das Tumorgewebe eindringen konnten. In Maus-Tumoren, die normalerweise gegen Immun-Checkpoint-Medikamente resistent sind, machte die Deletion von PDLIM5 die Behandlung mit einem Anti–PD-L1-Antikörper deutlich wirksamer und verkleinerte die Tumoren, während sowohl Helfer- als auch Killer-T-Zellen in ihnen zunahmen.
Warum das für künftige Krebstherapien wichtig ist
Insgesamt zeigen die Ergebnisse, dass PDLIM5 als zentraler Organisator des Aktingerüsts der Spitzt-Zelle wirkt, was eine robuste Filopodienbildung und ein schnelles Sprosswachstum in Richtung Tumor ermöglicht. Das Entfernen oder Deaktivieren von PDLIM5 in Endothelzellen verlangsamt die Ausbreitung der Tumorblutzufuhr, begradigt und stabilisiert verbleibende Gefäße, lindert Sauerstoffmangel und ermöglicht das Eindringen von Immunzellen in den Tumor. Für Patientinnen und Patienten deutet dies darauf hin, dass Medikamente, die die PDLIM5–ACTN1/ACTN4-Partnerschaft stören, Tumoren einerseits neue Gefäße entziehen und andererseits chaotische Tumorgefäßsysteme in Netzwerke verwandeln könnten, die Chemotherapie und Immuntherapie besser unterstützen.
Zitation: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
Schlüsselwörter: Tumorangiogenese, endotheliale Spitzt-Zellen, PDLIM5, Aktin-Zytoskelett, Krebsimmuntherapie