Clear Sky Science · de
Eine stabilisierte Tandem‑Antigenchimäre, die starke malariaübertragungsreduzierende Aktivität hervorruft
Warum es wichtig ist, die Übertragung durch Mücken zu stoppen
Die derzeit eingesetzten Malariavakzinen können schwere Erkrankungen und Todesfälle bei Kleinkindern deutlich verringern, lassen aber eine große Lücke: Personen, die sich nicht krank fühlen, können dennoch Parasiten tragen, die Mücken infizieren und die Übertragung aufrechterhalten. Diese Studie stellt ein Impfstoffdesign der nächsten Generation vor, das nicht nur eine einzelne Person schützen soll, sondern die Infektionskette zwischen Mensch und Mücke unterbrechen will. Indem die Forscher genau steuern, wie Schlüsselfragmente von Parasitenproteinen dem Immunsystem präsentiert werden, zielen sie darauf ab, Antikörper zu erzeugen, die Mücken als Wirte für Malaria unattraktiv machen und so Gemeinschaften der Eliminierung näherbringen.
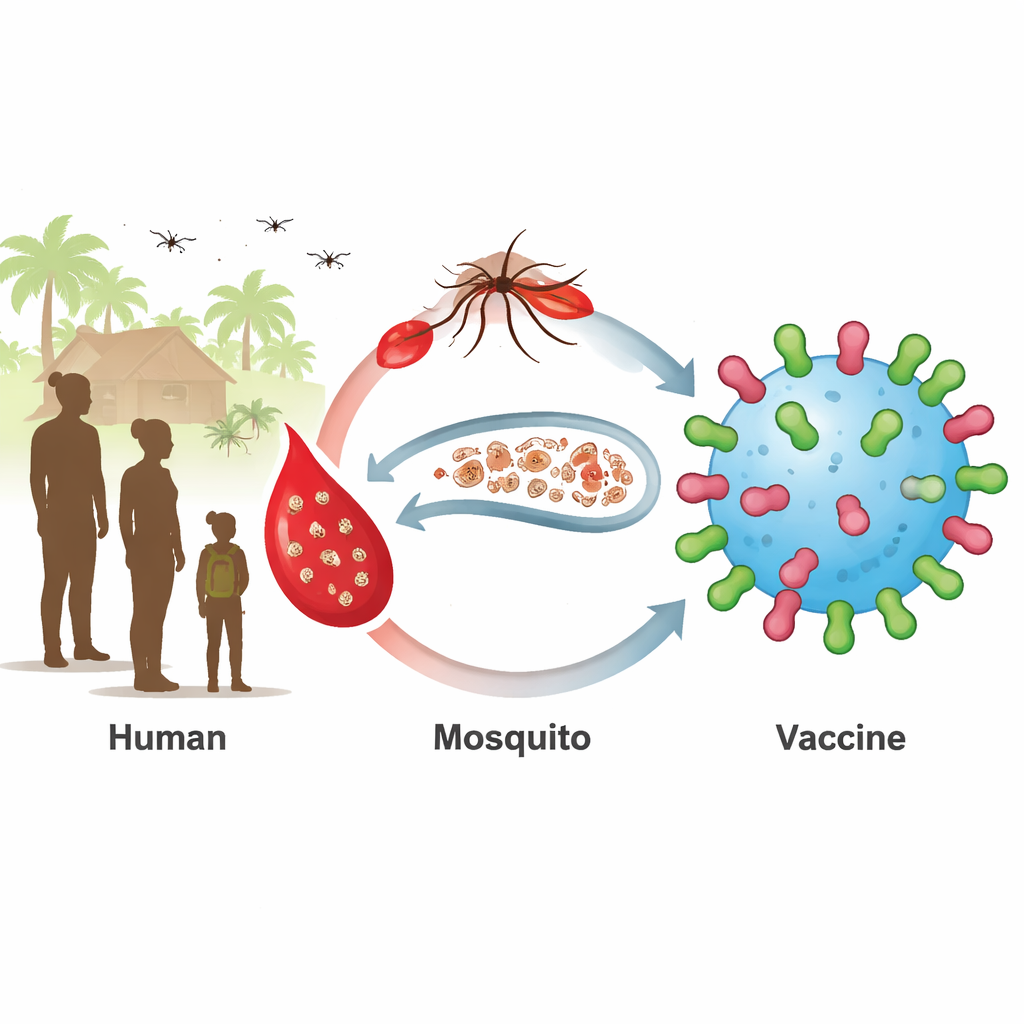
Ein verstecktes Reservoir, das Malaria am Leben hält
Aktuelle Malariavakzine konzentrieren sich auf frühe Infektionsstadien in Leber und Blut. Sie wirken am besten bei Kleinkindern, ältere Kinder und Erwachsene tragen jedoch oft reife sexuelle Parasitenstadien, so genannte Gametozyten, ohne Symptome zu zeigen. Wenn Mücken diese Personen stechen, nehmen sie die Parasiten auf und verbreiten sie weiter. Zwei Parasitenoberflächenproteine, bekannt als Pfs230 und Pfs48/45, sitzen auf diesen sexuellen Stadien und sind attraktive Ziele für sogenannte Übertragungsblockierende Impfstoffe. Impfstoffe gegen Fragmente dieser Proteine sind bereits in klinischen Studien, hatten aber Schwierigkeiten, in allen Empfängern starke und langlebige Antikörperantworten zu erzeugen.
Ein schlauerer Köder für das Immunsystem
Um frühere Designs zu verbessern, verfolgten die Autoren einen Strukturbiologieansatz und untersuchten im atomaren Detail, wie potente humane Antikörper an Pfs230 und Pfs48/45 binden. Sie identifizierten kleine Regionen, sogenannte Epitope, die besonders wirksam darin sind, die Entwicklung der Parasiten in Mücken zu blockieren. Ebenso wichtig war die Kartierung „nicht‑funktionaler“ Epitope, die Antikörper anziehen, die zwar binden, die Übertragung aber nicht stoppen – und damit Immunressourcen vergeuden. Mit Computer‑Modellierung und Proteinengineering verbanden sie die stärkste Region von Pfs230 (sein erstes Domäne) mit der Schlüsselregion von Pfs48/45 (seiner dritten Domäne) zu einem einzigen, sorgfältig arrangierten Protein, das sie eine stabilisierte Tandem‑Antigenchimäre, oder STAC, nennen.
Die nutzlosen Ziele verbergen, die nützlichen zeigen
Die Herausforderung bestand darin, diese beiden Domänen so zusammen darzustellen, dass sie die Anordnung auf dem Parasiten nachahmen, während die nicht‑funktionalen Oberflächen physisch verborgen werden, die sonst im intakten Protein vergraben sind. Das Team überarbeitete iterativ den kurzen Linker und die Schnittstelle zwischen den beiden Domänen und testete jede Version auf Stabilität, korrektes Falten und darauf, ob sie weiterhin an eine Reihe gut charakterisierter Antikörper bindet. Fortschrittliche Design‑Software schlug Mutationen vor, die die Schnittstelle strafften und die Expression in kultivierten Zellen verbesserten. Strukturelle Studien mittels Röntgenkristallographie, Kleinwinkel‑Röntgenstreuung und Kryo‑Elektronenmikroskopie bestätigten, dass in der finalen STAC‑Konstruktion die gewünschten Epitope hochtreu dargestellt werden, während die bekannten unwirksamen Stellen sterisch blockiert sind.
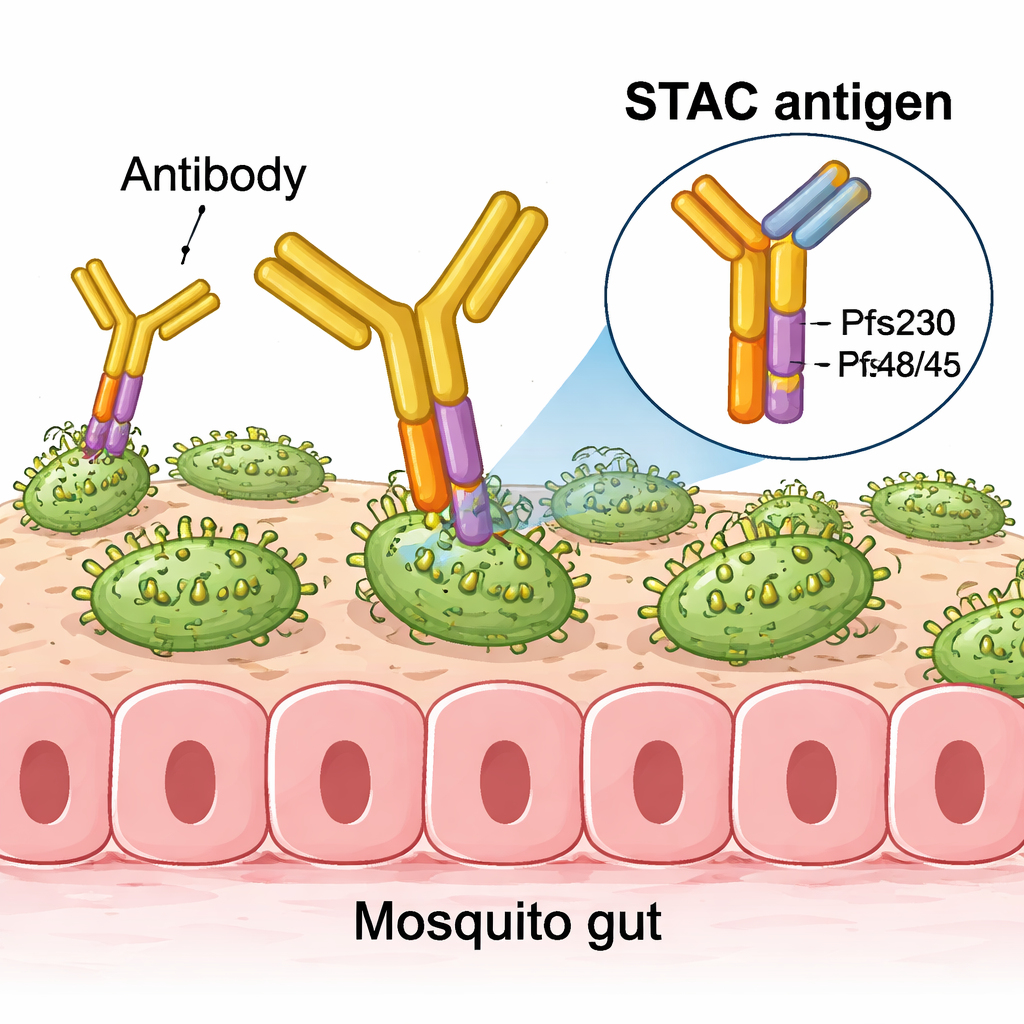
Von Einzelmolekülen zu leistungsstarken Nanopartikeln
Tests an Mäusen zeigten, dass, wenn STAC an spezialisierte Liposomen oder an sich selbst assemblierende Proteinnanopartikel gebunden wurde, starke Antikörperantworten ausgelöst wurden, die die Parasitenentwicklung in standardisierten Mückenfütterungsassays deutlich reduzierten. Bei gleichen oder geringeren Dosen übertraf STAC häufig Vakzine, die Pfs230‑ und Pfs48/45‑Fragmente getrennt verwendeten, sei es allein verabreicht, gemischt oder gemeinsam auf demselben Partikel dargestellt. In sehr sensitiven Tests, bei denen Mausserum vielfach verdünnt wurde, behielten die durch STAC‑dekorierte Nanopartikel ausgelösten Antikörper die Übertragungsreduzierende Aktivität besser bei als die anderer Formulierungen, was besonders potente und fokussierte Antworten anzeigt.
Was das für die Malariabekämpfung bedeuten könnte
Für Nicht‑Spezialisten ist die Kernidee, dass STAC ein maßgeschneiderter Köder ist, der dem Immunsystem genau jene Teile des Malariaparasiten zeigt, die für die Blockade der Ausbreitung am wichtigsten sind, während ablenkende Regionen, die nicht helfen, verborgen bleiben. In Tiermodellen führt dieses Design zu Antikörpern, die es den Parasiten erschweren, ihren Lebenszyklus in Mücken zu vollenden, selbst wenn die Antikörperspiegel relativ niedrig sind. Sollten ähnliche Ergebnisse beim Menschen erzielt werden, könnte STAC ein starker Partner zu bestehenden Malariavakzinen werden: Geimpfte Individuen vor Krankheit schützen und gleichzeitig das infektiöse Reservoir in der Gemeinschaft verkleinern. Darüber hinaus zeigt die Arbeit, wie detaillierte strukturelle Einsichten und Proteinengineering genutzt werden können, um mehrkomponentige Vakzine zu entwerfen, die potent, stabil und potenziell kostengünstiger herzustellen sind.
Zitation: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Schlüsselwörter: Malariavakzine, Übertragungsblockierung, Pfs230, Pfs48/45, Nanopartikel‑Immunogen