Clear Sky Science · de
Wesentliche Rolle der NONO–HOXA1–Wnt‑Achse bei der Differenzierung von Kardiomyozyten
Warum winzige Herz‑Zellen für uns alle wichtig sind
Jeder Herzschlag beruht auf Milliarden spezialisierter Muskelzellen, die sich während der Schwangerschaft bilden. Wenn dieser Prozess schiefgeht, können Neugeborene mit schweren Herzfehlern zur Welt kommen. Diese Studie verwendet humane Stammzellen, um ein entscheidendes Kontrollsystem zu enthüllen — aufgebaut aus den Molekülen NONO und HOXA1 sowie einem bekannten Signalweg namens Wnt — das frühe Zellen darin bestärkt, zu gesundem Herzmuskel zu werden. Das Verständnis dieser verborgenen Schaltkreise könnte langfristig zu besseren Diagnosen und Therapien für angeborene Herzfehler führen.
Vom unbeschriebenen Zustand zu den frühen Herzbauern
Die Forschenden begannen mit humanen induzierten pluripotenten Stammzellen — vielseitigen Zellen, die sich zu nahezu jedem Zelltyp entwickeln lassen. Mit einem standardisierten Protokoll leiteten sie diese Zellen zur Bildung von Kardiomyozyten, den schlagenden Zellen des Herzens. Wurde das NONO‑Gen entfernt, nahmen deutlich weniger Zellen erfolgreich eine Herzidentität an. Wesentliche frühe Marker, die normalerweise beim Verlassen des primitiven Zustands und beim Übergang in die Herzlinie auftauchen, waren stark reduziert. Einzelzell‑RNA‑Sequenzierung zeigte, dass viele NONO‑defiziente Zellen steckenblieben — halbwegs in einem unreifen, mesendoderm‑ähnlichen Zustand, anstatt sich zu vollentwickeltem Herzmuskel weiterzuentwickeln.
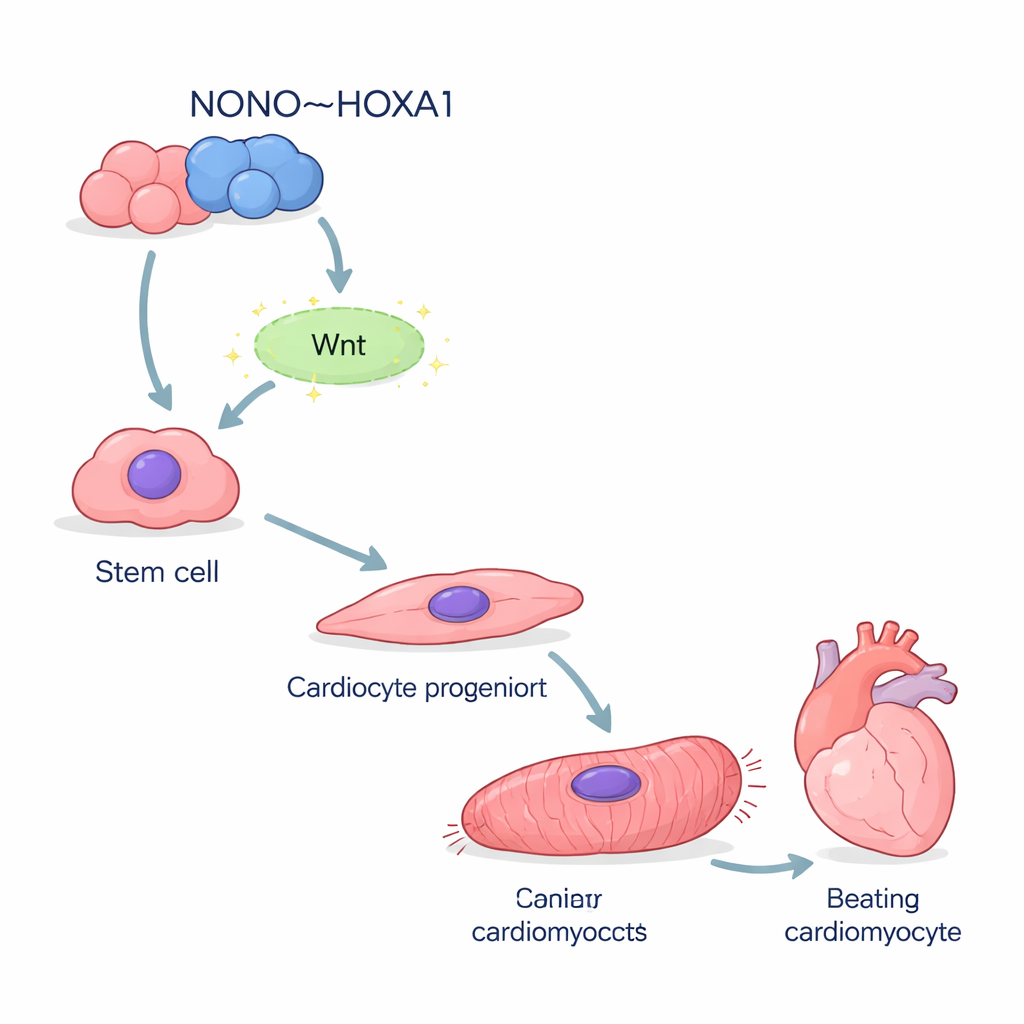
Wenn das Gerüst fehlt, versagen Herz‑Zellen
Die Zellen, die ohne NONO dennoch zu Kardiomyozyten wurden, waren weit davon entfernt, gesund zu sein. Sie exprimierten deutlich niedrigere Mengen an Strukturproteinen, die das Sarkomer bilden — die mikroskopische Maschinerie, die die Kontraktion antreibt. Unter dem Mikroskop zeigten die meisten Mutanten verworfene, fragmentierte kontraktile Fasern statt der ordentlichen Streifen normaler Zellen. Elektronenmikroskopie bestätigte, dass die üblichen Z‑Scheiben, die „Sprossen“ der kontraktilen Leiter, fehlten oder missgestaltet waren. Funktionell schlugen diese Zellen langsamer und unregelmäßiger. Messungen der Calcium‑Surges — elektrische Ereignisse, die jeden Herzschlag auslösen — zeigten unregelmäßige Verläufe mit verzögerten Spitzen und langsamer Erholung, was den Genexpressionsdefekten in Calcium‑Regulationskanälen entspricht.
Entwicklung retten und die NONO–HOXA1‑Partnerschaft offenlegen
Um zu prüfen, ob diese Probleme wirklich vom Verlust von NONO herrühren, führte das Team NONO in kontrollierter, medikamenteninduzierbarer Weise in den ersten zwei Tagen der Differenzierung wieder ein. Dieser kurze NONO‑Impuls stellte weitgehend das Ansteigen früher kardialer Gene wieder her, erhöhte den Anteil schlagender Herzzellen und baute organisierte Sarkomere und Z‑Scheiben wieder auf. Die Analyse der Genexpression bestätigte, dass viele Gene für Muskelkontraktion und Herzentwicklung in Richtung Normalwerte zurückkehrten. Im Gegensatz dazu konnten patientenabgeleitete, mutierte Versionen von NONO nicht retten, was die Idee stützt, dass solche Varianten die Krankheit durch Störung dieses frühen Programms verursachen. Protein‑Interaktionsversuche zeigten anschließend, dass NONO physisch an den Transkriptionsfaktor HOXA1 bindet und dass dieser Kontakt HOXA1 stabilisiert und dessen Dimerbildung fördert, die zum Ergreifen der DNA nötig ist.
Das Wnt‑Signal einschalten, um die Herz‑Fate zu verpflichten
Kartierungen, wo diese Proteine im Genom liegen, zeigten, dass NONO und HOXA1 häufig dieselben Regulationsregionen besetzen, inklusive solcher, die wichtige frühe Herz‑ und Wnt‑Weg‑Gene steuern. Fehlt NONO, schwächte sich HOXA1s Bindung an viele dieser Stellen ab, besonders an Genen, die das präkardiale Mesoderm — das früheste herzbildende Gewebe — antreiben. Der nachgeschaltete Wnt/β‑Catenin‑Weg, der normalerweise die Ausbildung von Mesoderm und Herzentwicklung unterstützt, war ebenfalls abgeschwächt: Es akkumulierte weniger β‑Catenin im Zellkern und Wnt‑antwortfähige Reporter zeigten geringere Aktivität. Eine Verstärkung der Wnt‑Signale durch eine höhere Dosis eines Wnt‑aktivierenden Wirkstoffs in den frühesten Differenzierungstagen konnte das Fehlen von NONO teilweise kompensieren, mehr Herz‑Zellen wiederherstellen und die kardiale Genexpression steigern.
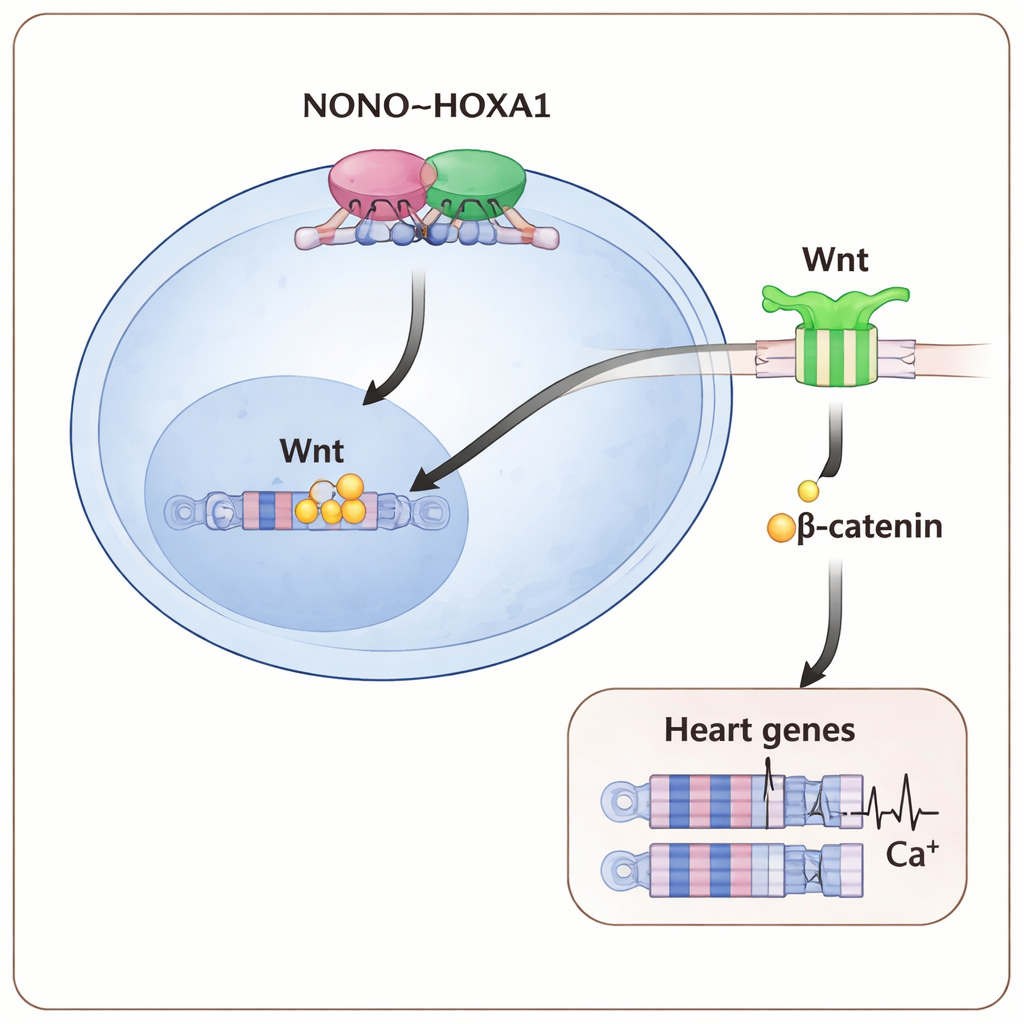
Was das für das Verständnis von Fehlbildungen bedeutet
Für Nicht‑Spezialisten lautet die zentrale Botschaft: Ein kleines molekulares Team — NONO, das Hand in Hand mit HOXA1 Wnt‑Signale feinjustiert — wirkt als früher „Verkehrsleiter“, der jungen Zellen sagt, Herzmuskel zu werden, und sie dafür ausstattet, richtig zu schlagen. Wird ein Teil dieser NONO–HOXA1–Wnt‑Achse gestört, zögern die Zellen, bleiben wichtige Herzgene aus und die resultierenden Kardiomyozyten sind strukturell und elektrisch fragil. Diese Erkenntnisse liefern eine klarere molekulare Erklärung dafür, warum Mutationen in NONO mit angeborenen Herzfehlern assoziiert sind, und weisen Wege auf, diese Bahn in Stammzellmodellen — oder eines Tages in Therapien zur Vorbeugung oder Reparatur von Herzmissbildungen — zu manipulieren.
Zitation: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Schlüsselwörter: angeborener Herzfehler, Differenzierung von Kardiomyozyten, Wnt‑Signalwirkung, Herzmodelle aus Stammzellen, Genregulation