Clear Sky Science · de
Asymmetrische Pt1C3–Pt1O1C3-katalytische Paare für effiziente Transferhydrierung von Azobenzol
Clevere Katalysatoren für sauberere Chemie
Chemiker suchen ständig nach Wegen, wichtige Chemikalien mit weniger Energie, weniger Materialeinsatz und saubereren Verfahren herzustellen. Diese Studie stellt einen neuen Typ hocheffizienter Katalysatoren vor, der aus einzelnen Platinatomen besteht, die in sorgfältig positionierten Paaren auf einer Kohlenstoffschicht angeordnet sind. Diese winzigen Strukturen beschleunigen eine Schlüsselreaktion, die das industrienahe Farbstoffmolekül Azobenzol in ein nützlicheres Produkt überführt, erheblich und weist zugleich den Weg zu grüneren Herstellungsverfahren feiner Chemikalien.
Warum winzige Metallpaare wichtig sind
Katalysatoren sind Substanzen, die chemische Reaktionen beschleunigen, ohne verbraucht zu werden, und sie sind zentral für alles von Brennstoffzellen bis zur Arzneimittelherstellung. In den letzten Jahren haben Forschende gelernt, Edelmetalle wie Platin als einzelne Atome auf Trägern zu verteilen, um aus jedem teuren Atom maximale Leistung herauszuholen. Viele reale Reaktionen sind jedoch zu komplex, als dass ein einzelnes Atom sie effizient bewältigen könnte; sie funktionieren am besten, wenn zwei benachbarte Stellen zusammenarbeiten. Das Team dieser Arbeit konzentriert sich auf solche „katalytischen Paare“: zwei Metallatome, die nahe genug beieinander liegen, um die Aufgaben zu teilen, aber mit atomarer Präzision so angeordnet sind, dass sie besser funktionieren als größere Partikel oder isolierte Atome.
Entwurf eines atomaren Doppelakts
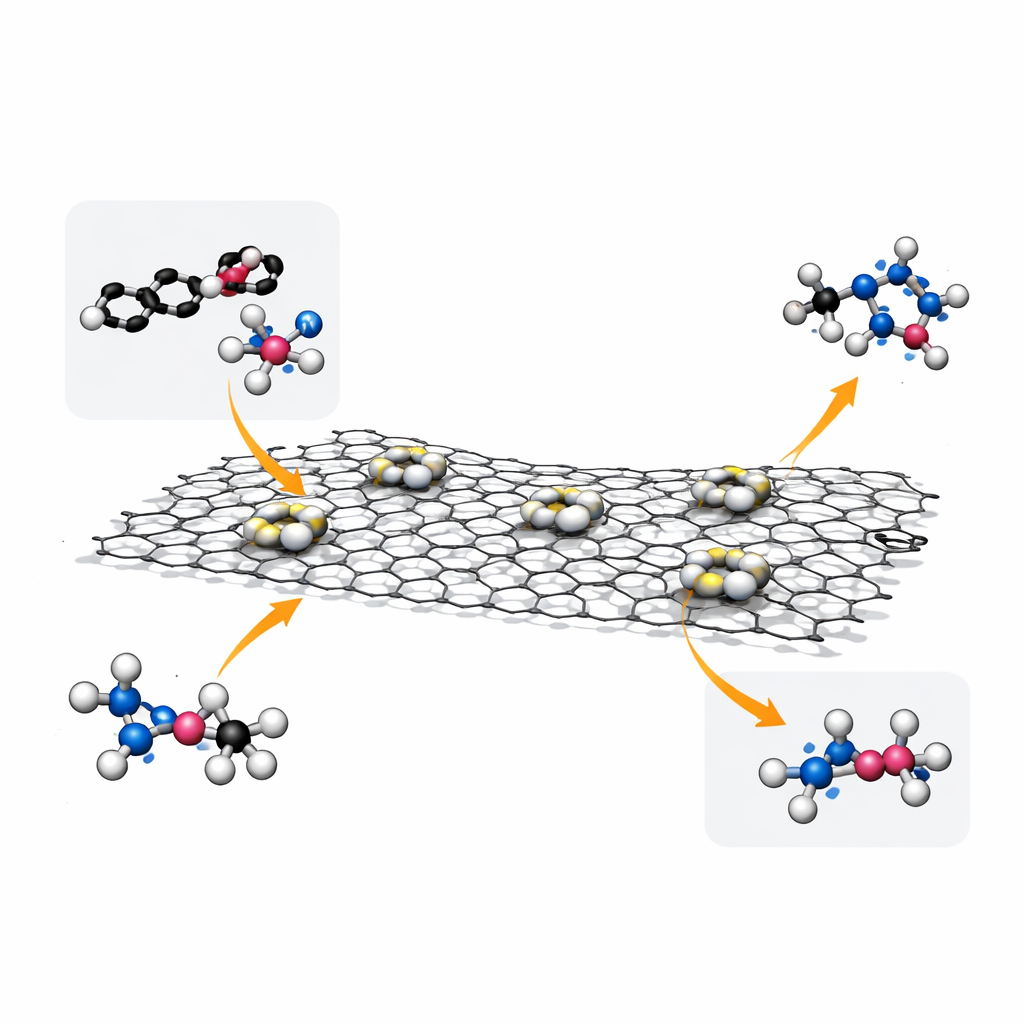
In der Studie bauten die Forschenden Paare von Platinatomen auf reduziertem Graphenoxid auf, einer dünnen, leitfähigen Kohlenstoffschicht. Jedes Paar ist asymmetrisch: Ein Platinatom ist an drei Kohlenstoffatome gebunden, während sein Partner an drei Kohlenstoffe und ein Sauerstoffatom gebunden ist. Dieser subtile Unterschied verändert, wie jedes Platinatom mit den reagierenden Molekülen interagiert. Mit spezialisierten Synthesemethoden kontrollierte das Team, wie dicht diese Paare auf der Oberfläche verteilt sind und – entscheidend – wie weit benachbarte Paare voneinander entfernt liegen. Hochauflösende Elektronenmikroskopie und fortgeschrittene spektroskopische Techniken bestätigten, dass die Platinatome einzeln dispergiert sind, echte Paare und keine Klumpen bilden und während des Betriebs einen stabilen chemischen Zustand beibehalten.
Das optimale Verhältnis für Geschwindigkeit finden
Der Katalysator wurde bei der Transferhydrierung von Azobenzol getestet, einer Reaktion, bei der Wasserstoff indirekt von einem festen Reagenz, Ammoniak–Borane, in Gegenwart von Wasser bereitgestellt wird. Indem die Gesamtmenge an Platin konstant gehalten, aber die Menge auf dem Kohlenstoffträger variiert wurde, veränderten die Forschenden den Abstand zwischen benachbarten Platinpaaren. Sie entdeckten, dass die katalytische Aktivität nicht einfach mit mehr Metall anstieg: Die Leistung erreichte ein Maximum, wenn der durchschnittliche Abstand zwischen den Paaren etwa 5,3 Å betrug (etwa eine halbe Milliardstel Meter). Bei diesem Abstand erzielte der Katalysator eine außergewöhnlich hohe Umsatzfrequenz—über eine Größenordnung besser als vergleichbare Platin-Nanopartikel- oder Einzelatomsysteme—und blieb über viele Reaktionszyklen stabil. Er funktionierte außerdem gut für verschiedene Azobenzolderivate, was zeigt, dass das Design breit einsetzbar ist und nicht nur auf ein einzelnes Molekül zugeschnitten wurde.
Wie Form und Abstand die Reaktion steuern
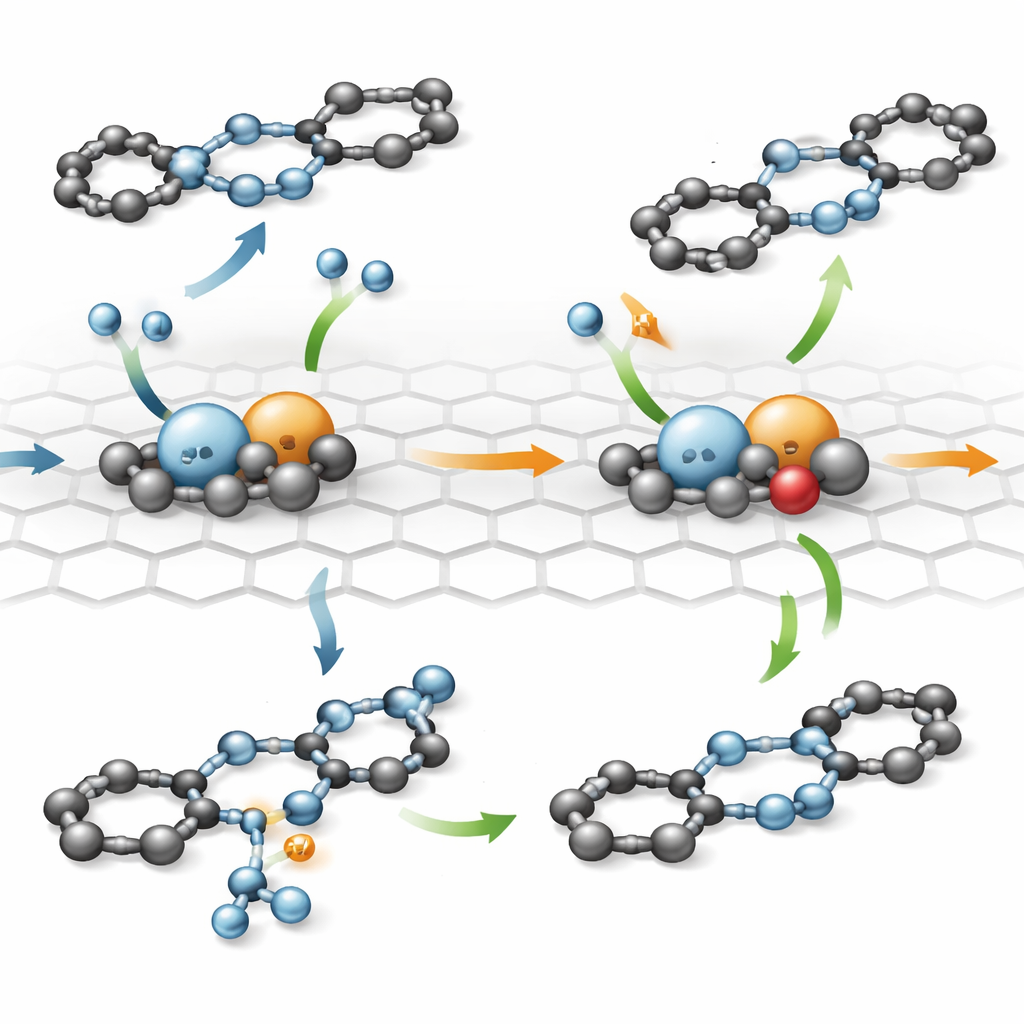
Um zu verstehen, warum diese präzise Anordnung so gut wirkt, nutzte das Team quantenmechanische Simulationen, um zu modellieren, wie Elektronen und Atome während der Reaktion bewegen. Das asymmetrische Platinpaar in Kombination mit dem optimalen Abstand zwischen benachbarten Paaren stimmt die elektronische Struktur der Metallatome so ab, dass sowohl Azobenzol als auch Ammoniak–Borane gleichzeitig bequem auf der Oberfläche Platz finden, ohne zu stark zu haften. Die Rechnungen zeigen einen schrittweisen Pfad, in dem Wasserstoff vom Ammoniak–Borane über das Platinpaar sowie benachbarte Kohlenstoff- und Sauerstoffatome weitergeleitet und schließlich auf die Stickstoff–Stickstoff-Bindung im Azobenzol übertragen wird. Wenn beide Platinatome vom gleichen Typ sind oder wenn sie zu dicht bzw. zu weit auseinander liegen, haftet Wasserstoff entweder zu fest, kann sich nicht effizient bewegen oder die Reaktanten adsorbieren nicht richtig—alles Ursachen, die die Reaktion verlangsamen.
Was das für zukünftige grüne Chemie bedeutet
Die Arbeit zeigt, dass nicht nur die Wahl des Metalls, sondern die genaue lokale Umgebung und der Abstand atomgenauer Paare die Leistung eines Katalysators entscheidend bestimmen können. Durch die gezielte Gestaltung eines ungleichen Platin-Duos bei genau der richtigen Trennung erzielten die Forschenden eine schnelle, selektive und robuste Hydrierung von Azobenzol unter Verwendung einer praktischen Wasserstoffquelle. Für Nichtfachleute lautet die Kernbotschaft: Die Kontrolle von Materie auf der Ebene einzelner Atome wird zu einem praktikablen Werkzeug für sauberere, effizientere chemische Herstellungsprozesse, was potenziell Abfall und Energieverbrauch bei der Produktion von Farbstoffen, Pharmazeutika und anderen Feinchemikalien reduzieren kann.
Zitation: Fang, Y., Zhao, W., Xing, Z. et al. Asymmetric Pt1C3-Pt1O1C3 catalytic pairs for efficient transfer hydrogenation of azobenzene. Nat Commun 17, 2239 (2026). https://doi.org/10.1038/s41467-026-68759-9
Schlüsselwörter: atomare Katalysatoren, Platinpaare, grüne Chemie, Hydrierung, auf Graphen gestützte Katalysatoren