Clear Sky Science · de
Elektrographische Cue-Reaktivität koexistiert mit tiefer Hirnstimulation im Nucleus accumbens in einem Fall von Opioidgebrauchsstörung
Warum diese Geschichte wichtig ist
Die Opioidabhängigkeit bleibt eine tödliche Epidemie, und viele Menschen kämpfen trotz Medikation und Beratung weiterhin mit starken Drogenverlangen. Dieser Artikel erzählt die Geschichte eines jungen Mannes, dessen Behandlungsteam ein Hirnimplantat nicht nur zur Stimulation, sondern auch zum Abhören seines Gehirns nutzte. Indem sie ein spezifisches elektrisches Signal identifizierten, das mit seinen Opioidverlangen verknüpft war, konnten sie seine tiefe Hirnstimulation so feinabstimmen, dass sie besser wirkte, mit weniger Energieaufwand, und ihm half, drogenfrei zu bleiben.
Dem Verlangen auf die Spur kommen
Der Patient war ein 25-jähriger Mann mit einer langjährigen schweren Opioidabhängigkeit, beginnend in der frühen Adoleszenz, begleitet von Depressionen, Angststörungen und weiteren Komplikationen. Standardbehandlungen, einschließlich sehr hoher Methadon-Dosen, hatten seine Verlangen nicht unter Kontrolle halten können. Jahre zuvor hatte er eine tiefe Hirnstimulation (DBS) in einer tiefen Hirnregion, dem Nucleus accumbens, erhalten – einem zentralen Knotenpunkt für Motivation und Belohnung. Mit aktivierter Stimulation sanken seine Verlangen, und er blieb mehrere Jahre von Opioiden abstinent. Als jedoch eine chirurgische Komplikation die Ärzte zwang, seine Batterie zu entfernen, kehrten die Verlangen innerhalb von Wochen zurück und sein Rückfallrisiko stieg deutlich an. Dadurch ergab sich eine seltene Gelegenheit: Elektrode und Anschluss konnten vorübergehend an externe Aufzeichnungsgeräte gekoppelt werden, sodass Forscher die Gehirnaktivität direkt messen konnten, während er Verlangen erlebte.
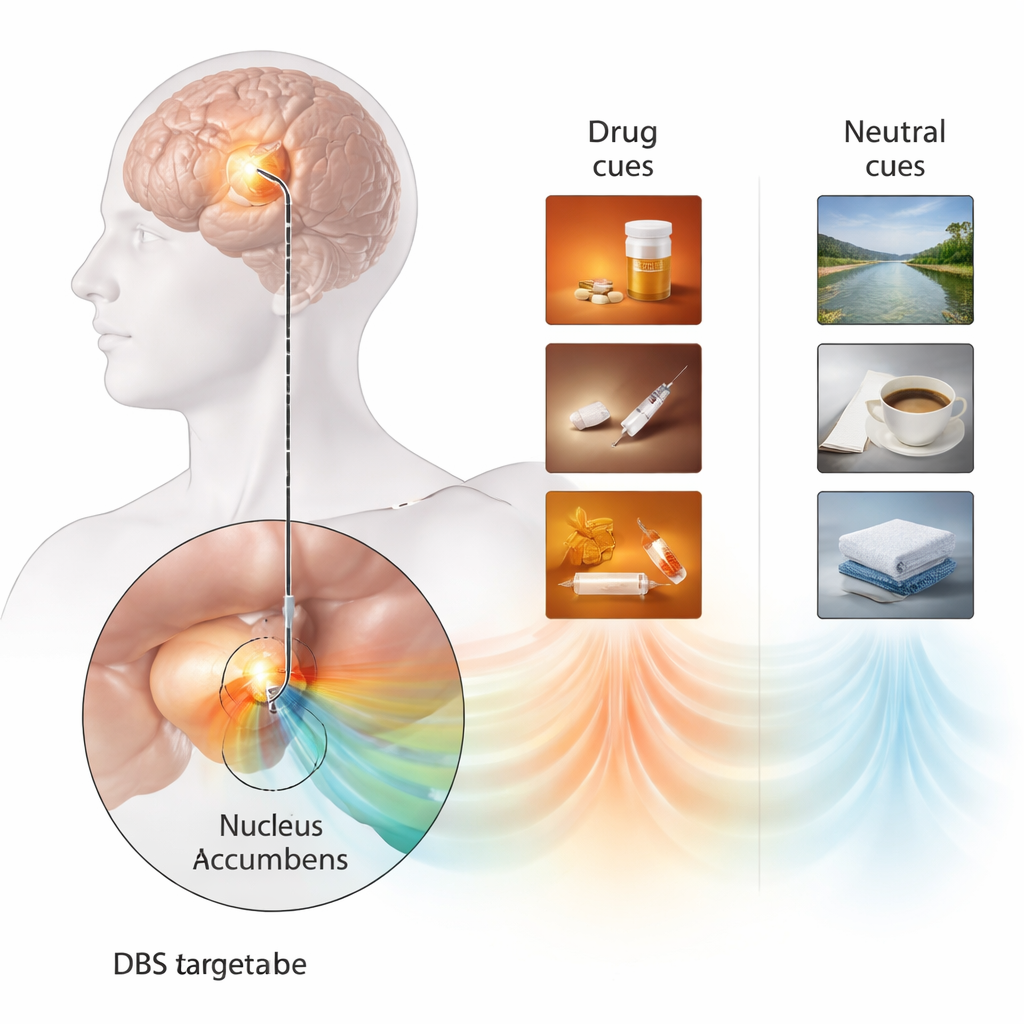
Personalisierte Auslöser enthüllen ein Hirnsignal
Um abzubilden, wie Verlangen im Gehirn aussieht, entwickelte das Team eine stark personalisierte Cue‑Reaktivitäts-Aufgabe. Statt generischer Drogenbilder erstellten sie kurze Videos, die sein früheres Drogenverhalten genau widerspiegelten – sein bevorzugtes Opioid, Spritzutensilien und Vorbereitungsrituale – und setzten diese zu ruhigen Naturszenen in Kontrast. Nach jedem sechssekündigen Clip bewertete er, wie stark sein Drang, Opioide zu konsumieren, war. Gleichzeitig wurde der DBS-Leitungsdraht im Nucleus accumbens wie ein winziges Mikrofon verwendet, um lokale elektrische Rhythmen seines Gehirns aufzuzeichnen. Wenn die Drogenvideos liefen, erschien ein charakteristischer Niedrigfrequenzrhythmus (im Bereich von 1–6 Hz) im ventralen Teil des Nucleus accumbens, einem Bereich, der vermutlich der sogenannten „Shell“-Subregion entspricht. Dieses Signal war bei neutralen Videos deutlich schwächer und in anderen Elektrodenbereichen nicht zu sehen. Wichtig war, dass höhere Leistung in diesem Rhythmus mit stärkeren selbstberichteten Verlangen korrelierte, was nahelegt, dass es sich um einen direkten Hirnmarker für Drogen-Cue-Reaktivität handelte und nicht um ein allgemeines Signal für Erregung oder Aufmerksamkeit.
Stimulation als gezieltes Instrument
Die entscheidende nächste Frage war, ob Stimulation an genau dieser Stelle den verlangensbezogenen Hirnrhythmus und das damit verbundene Verlangen dämpfen könnte. Das Team testete systematisch verschiedene Elektrodenkombinationen, fragte in Echtzeit nach Verlangen, Stimmung und Nebenwirkungen und erhöhte schrittweise die Stimulationsstärke. Das ventrale Kontaktpaar im Nucleus accumbens‑Shell erwies sich als Sweet Spot: Es führte zu starker Verlangenslinderung und Stimmungsverbesserung bei relativ geringem Strom und minimalen Nebenwirkungen. Dorsalere Kontaktpaare, in einem benachbarten Faserbündel namens anteriorer Schenkel der inneren Kapsel, halfen ebenfalls, erforderten aber deutlich stärkere Stimulation und riefen unangenehme Empfindungen hervor. Gestützt auf diese Tests wiederholten die Forscher die Cue‑Reaktivitäts‑Aufgabe, während sie vor jedem Video kurze Phasen der Shell‑Stimulation applizierten. Unter dieser „stimulierten“ Bedingung wurde der zuvor erhöhte 1–6‑Hz‑Rhythmus während der Drogenreize in Richtung neutraler Werte gedrückt, und seine durchschnittlichen Verlangensbewertungen sanken um mehr als die Hälfte.
Dauerhafte Veränderung mit leichterer Belastung
Mit diesen konvergierenden Belegen – aus Anatomie, Hirnsignalen und Verhalten – programmierten die Kliniker sein implantiertes Gerät dauerhaft so um, dass es fokal innerhalb der Nucleus‑accumbens‑Shell mit deutlich geringerem Strom als zuvor stimulierte. In den folgenden sechs Monaten berichtete er über anhaltende Reduktionen sowohl in Häufigkeit als auch Intensität der Opioidverlangen, erhielt und hielt Abstinenz aufrecht und erfüllte Kriterien für eine frühe Remission, ohne größere Veränderungen in Stimmung, Angst oder Energie. Modellierungen des Hirnnetzwerks zeigten, dass die neuen Einstellungen ein kleineres, fokussierteres Gewebsvolumen aktivierten und gleichzeitig einen wichtigen Pfad zwischen dem Nucleus accumbens und einer unter den Frontallappen gelegenen Region, die an Emotion und Bewertung beteiligt ist, ansprachen. Da die Stimulation effizienter war, reduzierten sich auch die Batterienachforderungen deutlich – ein wichtiger Vorteil für einen jungen Patienten, der wahrscheinlich langfristige Therapie benötigen wird.
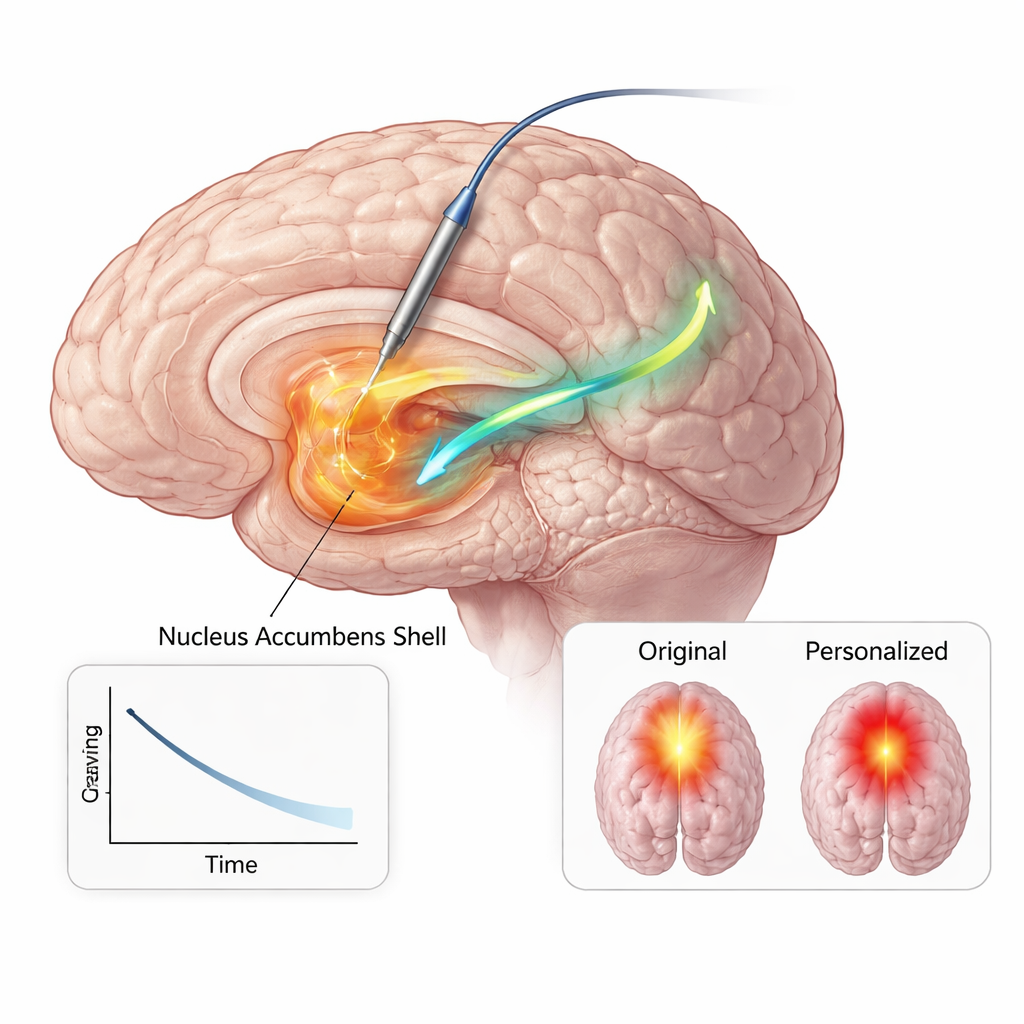
Was das für die zukünftige Versorgung bedeuten könnte
Dieser N‑of‑1‑Fall beweist nicht, dass derselbe Ansatz bei allen Menschen mit Opioidabhängigkeit wirken wird, aber er dient als Machbarkeitsnachweis. Er zeigt, dass bei mindestens einer Person ein spezifischer elektrischer Rhythmus in einem Belohnungsknoten des Gehirns Opioidverlangen eng verfolgte und durch präzise zielgerichtete Stimulation beruhigt werden konnte, was zu anhaltender Symptomlinderung bei niedrigerer elektrischer Dosis führte. Einfach ausgedrückt lernte das Team, den Stimulator auf das eigene Verlangenssignal des Patienten „abzustimmen“. Wenn ähnliche Hirnmarker bei mehr Personen gefunden und verfolgt werden können und Geräte, die sowohl messen als auch stimulieren, weiter verbreitet verfügbar werden, könnten künftige Behandlungen die Hirnstimulation für Suchterkrankungen personalisieren – indem sie eingreifen, wenn Verlangensschaltkreise aufflammen, und so Menschen helfen, einem Rückfall zuvorzukommen.
Zitation: Qiu, L., Nho, YH., Seilheimer, R.L. et al. Electrographic cue-reactivity co-localizes with accumbens deep brain stimulation in a case of opioid use disorder. Nat Commun 17, 1708 (2026). https://doi.org/10.1038/s41467-026-68758-w
Schlüsselwörter: Opioidabhängigkeit, tiefe Hirnstimulation, Nucleus accumbens, Hirnbiomarker, Drogenverlangen