Clear Sky Science · de
Strukturelle Grundlage für Gabelumkehr und RAD51-Regulation durch den SCF-Ubiquitin-Ligase-Komplex des F-Box-Helikase 1
Wie Zellen eine blockierte DNA-Kopie-Maschine retten
Jedes Mal, wenn sich eine Zelle teilt, muss sie Milliarden von DNA-Basen schnell und fehlerfrei kopieren. Doch diese Kopiermaschinerie gerät häufig ins Stocken – DNA-Schäden, schwer zu kopierende Sequenzen oder Arzneimittelbehandlungen können den Prozess unterbrechen. In solchen Fällen verlassen sich Zellen auf Notfallreparaturteams, die die Replikationsgabeln stabilisieren und wieder in Gang bringen. Diese Arbeit zeigt in noch nie dagewesenen strukturellen Details, wie ein solcher Teamleiter – ein Proteinkomplex rund um die Helikase FBH1 – blockierte DNA umformt und ein weiteres zentrales Reparaturprotein, RAD51, streng kontrolliert. Das Verständnis dieses Zusammenspiels erklärt, wie Zellen gefährliche Genombrüche vermeiden und warum Störungen dieser Faktoren mit Krebs in Verbindung stehen.
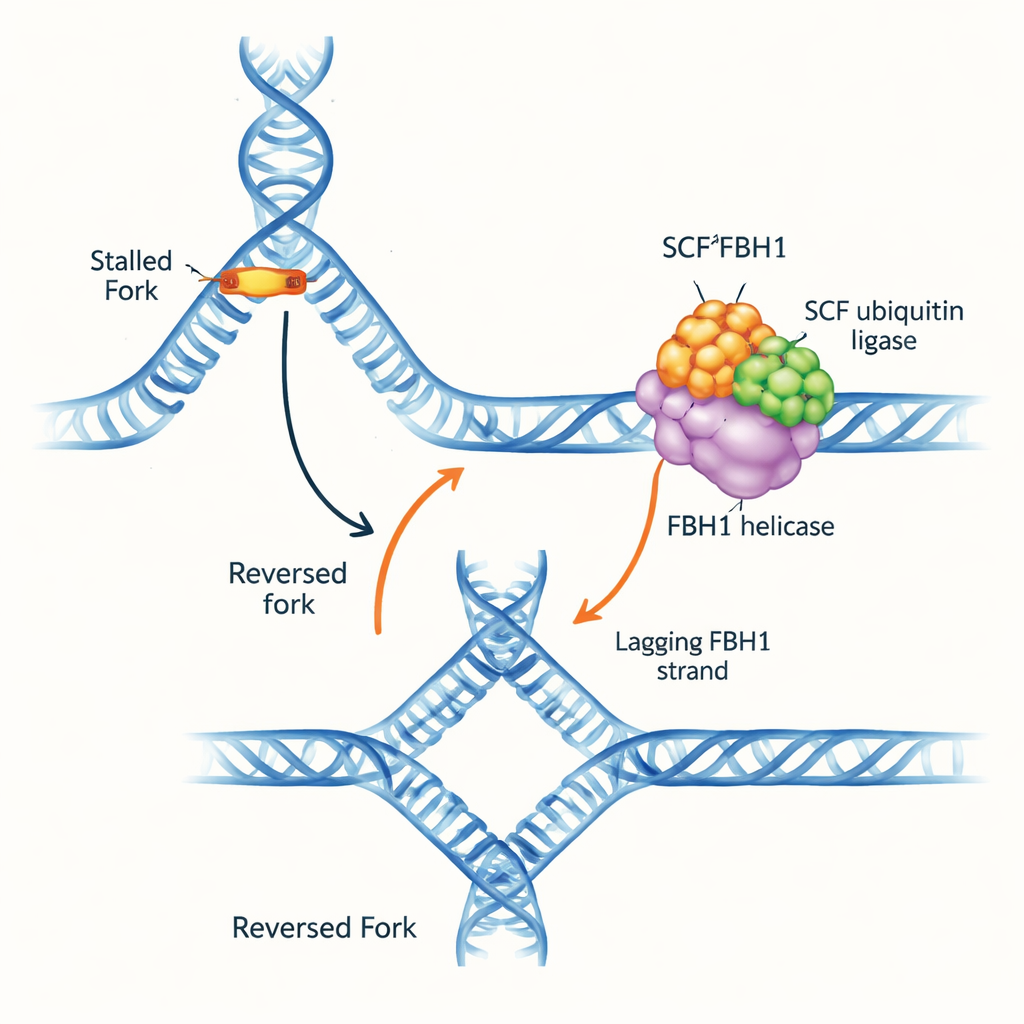
Ein Stau auf der DNA-Autobahn
Replikationsgabeln sind Y-förmige Strukturen, an denen die Doppelhelix aufgetrennt und kopiert wird. Trifft die Gabel auf Hindernisse, kann sie die Richtung umkehren: die Elternstränge zippen wieder zusammen und die neu synthetisierten Stränge paaren sich miteinander, wodurch eine vierarmige DNA-Verzweigung entsteht. Diese „Gabelumkehr“ kann Zeit verschaffen, um Schäden zu reparieren und die Replikation sicher neu zu starten, erzeugt aber bei Fehlsteuerung auch anfällige DNA, die brechen kann. Mehrere molekulare Motoren sind dafür bekannt, Gabeln rückwärts zu schieben, indem sie die doppelsträngige DNA vor der Gabel greifen. FBH1 zeichnet sich hingegen dadurch aus, dass es sich anders verhält und in Tumoren häufig verändert ist, was darauf hindeutet, dass es über einen eigenständigen und medizinisch relevanten Weg operiert.
Ein Gabelspezialist mit einer bevorzugten Seite
Die Autoren reinigten den humanen SCFFBH1-Komplex, der die FBH1-Helikase mit einem Ubiquitin-Anheftungsmodul (SCF) kombiniert. Zunächst fragten sie, welche DNA-Formen FBH1 bevorzugt. Mit Bindungs- und Aufwickel-Assays zeigten sie, dass SCFFBH1 echte gabelähnliche Strukturen stark bevorzugt, insbesondere dort, wo auf dem „lagging“-Vorlagstrang ein kurzer Abschnitt einzelsträngiger DNA vorhanden ist – die Seite, die in kurzen Fragmenten kopiert wird. An diesen Strukturen entwindet FBH1 DNA hunderte Male schneller als an einem einfachen losen Ende, was darauf hinweist, dass das richtige Einrasten an der Gabelverzweigung seine Motoraktivität enorm steigert. Einzelmolekulare Magnetschrauben bestätigten, dass der Komplex die DNA entwinden und dann entlang einzelsträngiger DNA über Tausende von Basen hinweg wandern kann, ohne zu dissoziieren – er wirkt als kräftiger, prozessiver Motor.
Die Gabel umkehren, indem man von hinten zieht
Um herauszufinden, wie dieser Motor Gabeln tatsächlich umkehrt, testete das Team künstliche Gabelsubstrate mit oder ohne einzelsträngige Lücken. Im Gegensatz zu anderen Gabelumbauern konnte SCFFBH1 nicht an einer vollständig gepaarten Gabel arbeiten; es benötigte eine Lücke auf dem lagging-Vorlagstrang und bewegte sich in 3′–5′-Richtung entlang dieses Einzelstrangs. Diese „Von-hinten-Zug“-Bewegung treibt das erneute Aneinanderlegen der Elternstränge voran, während das Enzym an der Gabelverzweigung fest eingespannt bleibt. Eine Kryo-Elektronenmikroskopie-Struktur von SCFFBH1 gebunden an eine gestoppte Gabel zeigt, wie: ein besonderes positiv geladenes Patch, ein „Junction-Binding-Motiv“ in einer Unterdomäne von FBH1, liegt genau an dem Verzweigungspunkt, wo die drei DNA-Äste zusammenkommen. Als die Forscher zwei entscheidende Aminosäuren in diesem Motiv mutierten, fiel die Gabelumkehr in vitro etwa 25-fach ab, während der grundlegende Entwindungsmotor noch recht gut funktionierte. In Zellen verhinderte die gleiche Mutation das normale Verlangsamen von Replikationsgabeln als Reaktion auf ein stressauslösendes Medikament – ein Kennzeichen fehlgeschlagener Gabelumkehr.
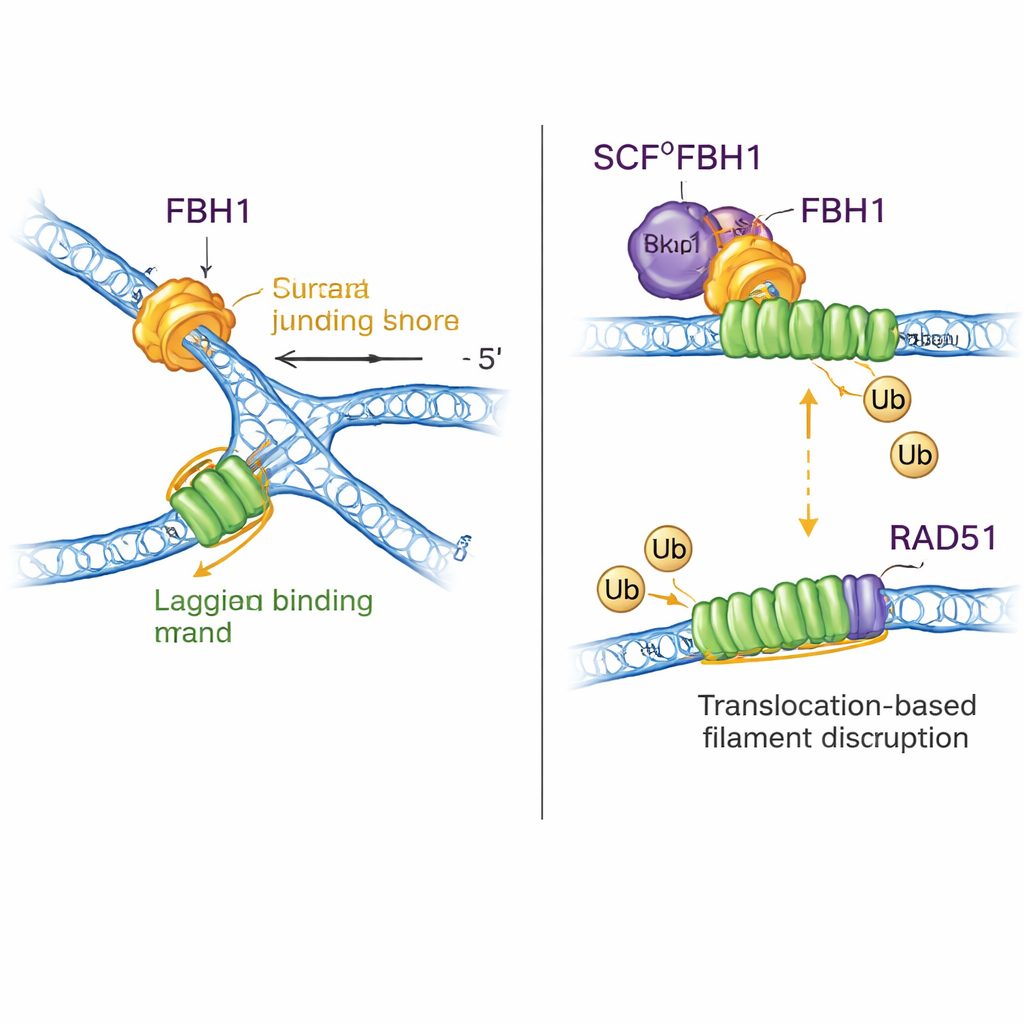
Doppelte Rolle: DNA umformen und RAD51 entfernen
FBH1 ist nicht nur ein Motor; über den SCF-Komplex hilft es auch, kleine Ubiquitin-Tags an Proteine zu hängen. Die neuen Strukturen fügen nahezu den gesamten SCFFBH1–DNA-Komplex zusammen und zeigen, dass der Ubiquitin-Transfer-„Kopf“ der Ligase weniger als 45 Å vom vom FBH1 ausgehenden lagging-Strang entfernt sitzt. Durch das Andocken bekannter Strukturen anderer Ubiquitin-Ligasen schlagen die Autoren vor, dass diese Geometrie RAD51 – ein Enzym, das Filamente auf DNA bildet, um Rekombination zu fördern – genau in die Schusslinie auf dem lagging-Strang einer gestoppten Gabel positioniert. Frühere Arbeiten zeigten, dass FBH1 RAD51 mechanisch von der DNA entfernen und es außerdem mit Ubiquitin markieren kann, sodass es sich nicht leicht wieder anlagert. Das neue Modell vereinheitlicht diese Ideen: Während FBH1 am lagging-Strang zieht, um die Gabel umzubauen, kann das nahegelegene SCF-Modul RAD51-Untereinheiten markieren und so helfen, übermäßige RAD51-Filamente abzubauen oder deren Neubildung zu verhindern, die sonst die korrekte Gabelverarbeitung blockieren würden.
Was das für Genomstabilität und Krebs bedeutet
Insgesamt zeigt die Studie, dass SCFFBH1 gestoppte DNA-Replikationsgabeln mit einem Mechanismus umkehrt, der sich von anderen bekannten Gabelumbauern unterscheidet: Es greift den Verzweigungspunkt fest und transloziert gleichzeitig entlang des lagging-Vorlagstrangs von hinten, wodurch das sichere Wiederzusammenziehen der Elternstränge gefördert wird, ohne eine langlebige, mobile vierarmige Verzweigung zu bilden. Zugleich ist seine eingebaute Ubiquitin-Ligase strategisch positioniert, um RAD51 vom selben Strang zu entfernen und so eine entfesselte Rekombination bei Replikationsstress zu verhindern. Da FBH1 in Krebsarten häufig verloren geht oder mutiert ist, helfen diese strukturellen und mechanistischen Einsichten zu erklären, wie solche Tumoren DNA-Schäden anhäufen und warum sie möglicherweise unterschiedlich auf Medikamente reagieren, die Replikationsstress hervorrufen oder verwandte Wege angreifen.
Zitation: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Schlüsselwörter: DNA-Replikationsstress, Gabelumkehr, FBH1-Helikase, RAD51-Regulation, Genomstabilität