Clear Sky Science · de
Automatisierte Kartierung des Fortschritts von DNA-Replikationsgabeln in menschlichen Zellen mit ForkML
Warum die Messung der DNA-Kopiergeschwindigkeit wichtig ist
Jedes Mal, wenn eine menschliche Zelle sich teilt, muss sie mehr als drei Milliarden DNA-Bausteine schnell und fehlerfrei kopieren. Verlangsamt oder blockiert sich dieser Vorgang, kann das das Genom schädigen und zu Krebs oder Entwicklungsstörungen beitragen. Bisher fehlte jedoch eine einfache Methode, um genau zu beobachten, wie schnell einzelne „Kopiermaschinen“ der DNA über bestimmte Abschnitte des menschlichen Genoms laufen. Dieser Artikel stellt ForkML vor, eine neue Technik, die Nanopore-DNA-Sequenzierung und maschinelles Lernen kombiniert, um diese Aufgabe in bisher unerreichter Größenordnung zu automatisieren.
Die Kopiermaschinen der Zelle indirekt beobachten
Die DNA wird von winzigen molekularen Maschinen, den Replikationsgabeln, entlang der Doppelhelix dupliziert, wobei neue Stränge entstehen. ForkML ermöglicht Forschern, diese Gabeln indirekt zu beobachten, indem ein harmloses chemisches Etikett, BrdU, während zweier sehr kurzer Pulse mit festem Zeitabstand in neu synthetisierte DNA eingebaut wird. Da BrdU in einzelnen DNA-Molekülen von Nanopore-Sequenzierern nachgewiesen werden kann, sind auf jedem DNA-Strang zwei markierte „Streifen“ sichtbar, an denen eine Gabel während der beiden Pulse vorbeigelaufen ist. Durch Messen des Abstands zwischen den Streifen und Division durch den bekannten Zeitabstand lässt sich die Geschwindigkeit jeder Gabel in dem betreffenden Genomabschnitt berechnen. 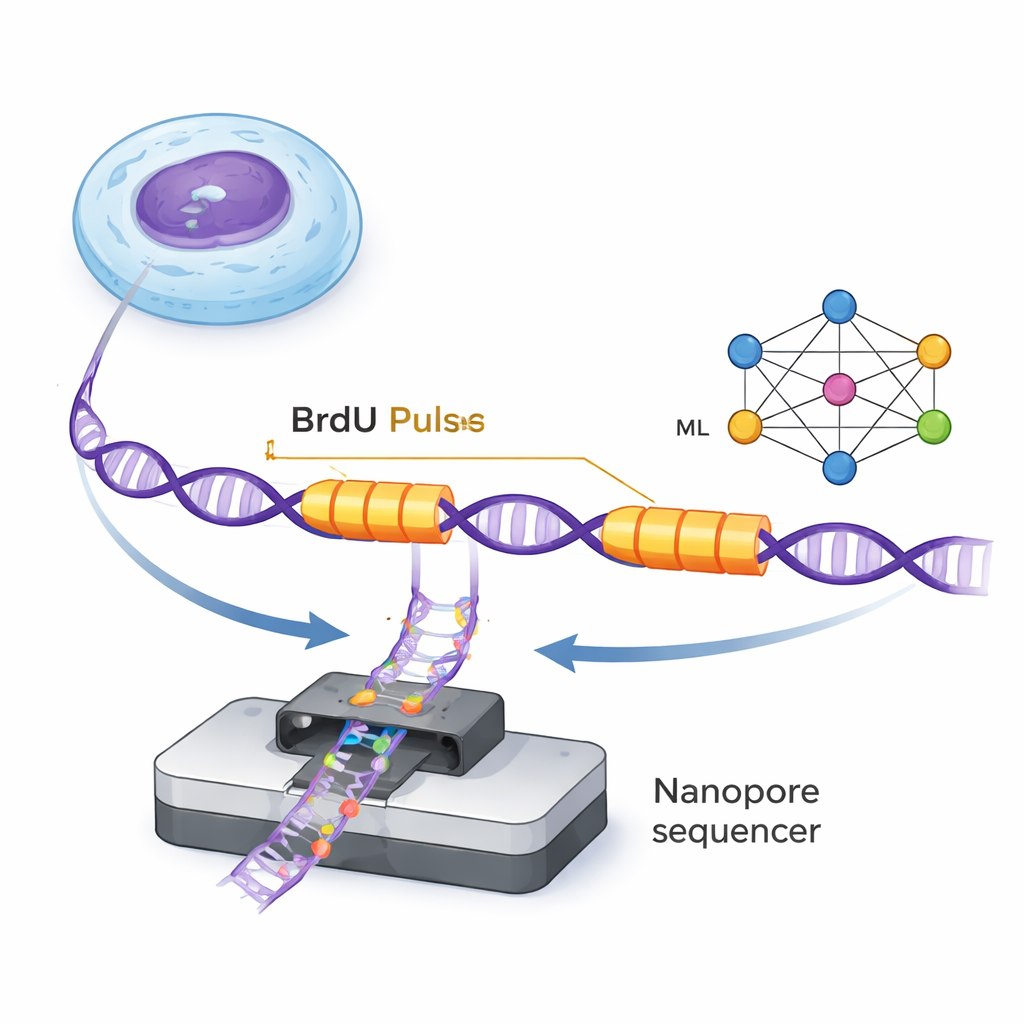
Ein Computer, der die chemischen Spuren liest
In früheren Arbeiten mit Hefe konnten die Autoren diese BrdU-Spuren mit einfachen Regeln erkennen, doch in menschlichen Zellen sind die Signale schwächer und komplexer. Menschliche Expertinnen und Experten können das charakteristische Muster – ein scharfer Anstieg von BrdU beim Pulsbeginn, gefolgt von einem langsamen Abfall nach dem Auswaschen – noch erkennen, aber das manuell für Millionen von DNA-Fragmenten zu tun, ist unmöglich. ForkML löst dieses Problem, indem es ein neuronales Netzwerk, eine Form des maschinellen Lernens, an Tausenden von manuell annotierten Beispielen trainiert. Das Modell lernt, jeden DNA-Abschnitt als Hintergrund oder als rechts- bzw. linkslaufende Gabel zu klassifizieren und den Beginn jedes BrdU-Pulses mit hoher Genauigkeit zu lokalisieren. Damit ist eine vollautomatische Kartierung von Tausenden individueller Gabelgeschwindigkeiten aus einem einzigen Sequenzierlauf möglich.
Stress messen und Unterschiede im Genom aufdecken
Beim Einsatz von ForkML in einer menschlichen Kolon-Krebszelllinie erzielte das Team über 2000 Gabelgeschwindigkeitsmessungen pro Experiment und fand, dass sich eine typische Gabel mit etwa 1,2 Kilobasen pro Minute bewegt — im Einklang mit früheren, niedrigdurchsatzigen Methoden. Behandelten sie die Zellen mit Wirkstoffen, die die DNA-Replikation verlangsamen, erkannte ForkML die Verlangsamung deutlich und zeigte damit, dass die Methode Replikationsstress sensibel messen kann. Da jede Gabel wieder auf ihre Position im Referenzgenom zurückgeführt wird, konnten die Autoren die Geschwindigkeit mit anderen Merkmalen in Beziehung setzen, etwa dem Zeitpunkt der Replikation im Zellzyklus, der Chromatinverdichtung und der Transkriptionsaktivität. 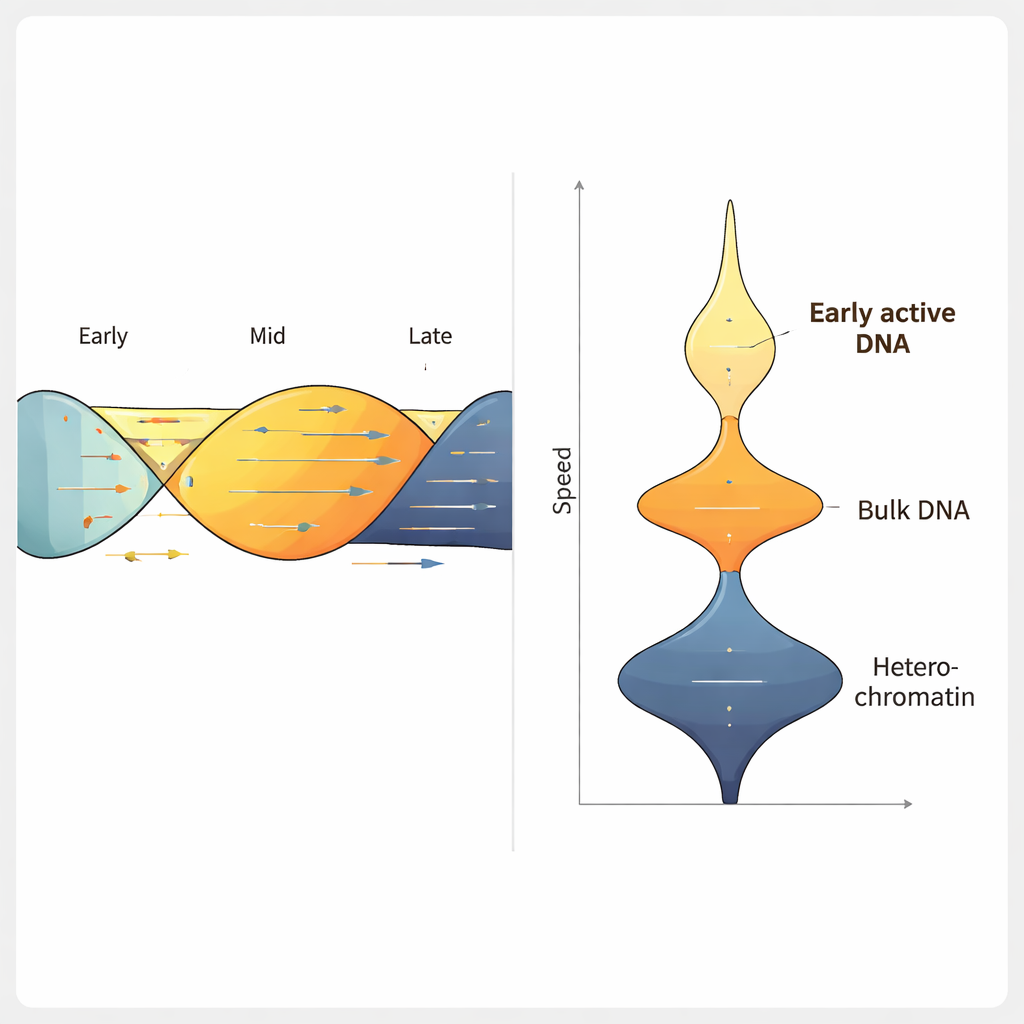
Aufdecken, wo die DNA-Replikation beginnt und wie sich Stränge unterscheiden
Neben der Geschwindigkeit identifiziert ForkML auch, wo die DNA-Replikation beginnt und endet, indem es Stellen erkennt, an denen Gabeln entlang desselben Moleküls auseinanderlaufen oder aufeinandertreffen. Bei der Kartierung von mehr als 20.000 solchen Startpunkten bestätigen die Autoren, dass menschliche Zellen eine gemischte Strategie verwenden: Einige Initiationen treten in klar definierten Startzonen auf, die meisten beginnen jedoch verstreut im Genom. Durch die Kombination der Gabelrichtung mit der Information, welcher DNA-Strang vom Sequenzierer gelesen wurde, kann ForkML außerdem die Raten der Leading- und Lagging-Strang-Synthese unterscheiden — etwas, das traditionelle Faser-Assays nicht leisten können. Tests in sechs verschiedenen humanen Zelllinien — sowohl normalen als auch krebsartigen — zeigen, dass dieselben einfachen BrdU-Markierungsbedingungen breit anwendbar sind und in jedem Fall robuste Geschwindigkeitsabschätzungen liefern.
Ein digitales Upgrade einer klassischen Methode
Für Nicht-Spezialisten lässt sich ForkML als moderne, digitale Version des klassischen DNA-Faser-Assays betrachten: Es verwendet ein ähnliches Markierungsschema, ersetzt jedoch manuelle Mikroskopie durch Langzeitsequenzierung und maschinelles Lernen. Das bringt eine deutlich höhere Durchsatzrate, die direkte Verortung jeder Messung im Genom und detailliertere Informationen darüber, wo und wie schnell DNA kopiert wird. Weil das Protokoll einfach, mit aktueller Nanopore-Hardware kompatibel und auf andere Organismen übertragbar ist, hat ForkML das Potenzial, ein Standardwerkzeug zur Untersuchung der DNA-Replikation zu werden. Praktisch bietet es Forschenden eine leistungsfähige Möglichkeit, lokale DNA-Kopiergeschwindigkeiten — normal oder unter Stress — mit Genaktivität, Chromatinzustand und krankheitsbedingten Veränderungen im Genom zu verknüpfen.
Zitation: Rojat, V., Ciardo, D., Tourancheau, A. et al. Automated mapping of DNA replication fork progression in human cells with ForkML. Nat Commun 17, 1975 (2026). https://doi.org/10.1038/s41467-026-68750-4
Schlüsselwörter: DNA-Replikation, Geschwindigkeit der Replikationsgabel, Nanopore-Sequenzierung, BrdU-Markierung, Maschinelles Lernen in der Genomik