Clear Sky Science · de
Ein proteogenomischer Atlas von 1.032 Hirnmetastasen identifiziert molekulare Subtypen, Immunlandschaften und therapeutische Verwundbarkeiten
Warum Krebs in der Hirnsubstanz streut
Da die Krebstherapie Fortschritte macht, leben mehr Menschen lange genug, damit ihre Tumoren in neue Organe streuen, einschließlich des Gehirns. Diese Hirnmetastasen sind inzwischen eine häufige und oft verheerende Komplikation; dennoch behandeln Ärztinnen und Ärzte sie meist danach, wo der Primärtumor entstanden ist—Lunge, Brust, Haut, Darm—instead of danach, wie sich der Krebs an das Leben im Gehirn angepasst hat. Diese Studie erstellte einen detaillierten „Atlas“ von mehr als tausend Hirnmetastasen, um deren verborgene Biologie zu verstehen, wie sie mit den eigenen Zellen und dem Immunsystem des Gehirns interagieren und welche neuen therapeutischen Ansatzpunkte sich daraus ergeben könnten.
Aufbau einer großen Landkarte von Hirntumoren
Die Forschenden sammelten Daten von 1.032 Hirnmetastasen, die aus verschiedenen Primärtumoren hervorgegangen waren, zusammen mit Dutzenden passender Primärtumoren und einigen aggressiven primären Hirntumoren zum Vergleich. Sie kombinierten mehrere moderne Methoden: DNA- und RNA-Sequenzierung, groß angelegte Messungen von Proteinen und Metaboliten, Einzelzell- und räumliche Kartierung von Tumor- und Immunzellen sowie patientenabgeleitete Mini-Organoide, die im Labor gezüchtet wurden. Durch die Integration all dieser Ebenen verfolgten sie nicht nur das Ziel, Gene aufzulisten, sondern zu verstehen, wie ganze biologische Systeme in Hirnmetastasen funktionieren.
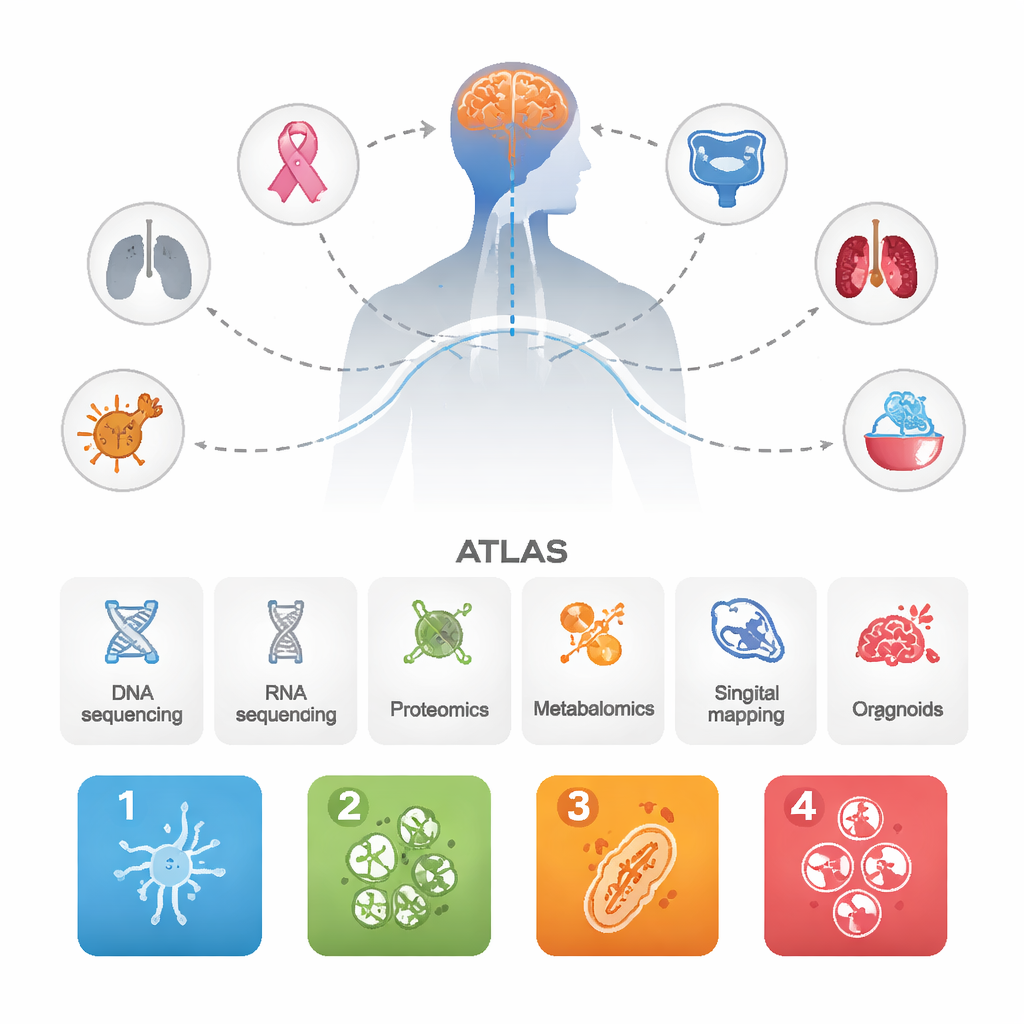
Vier wiederkehrende „Persönlichkeiten“ von Hirnmetastasen
Trotz unterschiedlicher Herkunftsorgane ließen sich die Hirnmetastasen immer wieder in vier große molekulare Subtypen einteilen. Einer, BrMS1 genannt, wirkt „neural-ähnlich“: Tumorzellen und das umliegende Gewebe exprimieren viele Programme von Gehirn- und Nervenzellen und zeigen relativ aktive immunologische Überwachung. BrMS2 ist „immun-infiltriert“, dicht bevölkert mit Immunzellen, insbesondere T‑Zellen, und zeigt ein Programm, das als epithelial‑mesenchymale Transition bekannt ist und Zellverbindungen lockert und die lokale Umgebung umgestaltet. BrMS3 ist „metabolisch“ und wird von hochaktiven Krebszellen dominiert, die ihre Energieverwendung umprogrammieren—etwa über Wege wie Fettsäurestoffwechsel und oxidative Phosphorylierung. BrMS4 ist „proliferativ“, gekennzeichnet durch schnelle Zellteilung, stammzellähnliche Merkmale und hohe genomische Instabilität, aber auffallend wenige Immunzellen.
Was die Mikroumgebung des Tumors offenbart
Durch die Betrachtung auf Einzelzell- und räumlicher Ebene zeigte das Team, dass jeder Subtyp in einer charakteristischen Nachbarschaft im Gehirn vorkommt. BrMS1-Läsionen sind reich an unterstützenden Gehirnzellen wie Astrozyten und Neuronen, was darauf hindeutet, dass der Tumor normales Hirngewebe nachahmt und kapert. BrMS2-Tumoren sind hingegen gesprenkelt mit dichten T‑Zell-Clustern, darunter viele „erschöpfte“ T‑Zellen, die Checkpoint-Moleküle wie PD‑1 exprimieren, und weisen aktivierte Blutgefäße sowie entzündliche Signale auf. BrMS3-Läsionen liegen in metabolisch aktiven Zonen, während BrMS4-Läsionen Inseln schnell teilender Zellen bilden, umgeben von relativ immunarmen Bereichen. Allgemein fand die Studie, dass in Hirnmetastasen—aber nicht in Primärtumoren—starke Aktivierung der epithelial‑mesenchymalen Transition tendenziell mit höherer T‑Zell-Infiltration einhergeht, was nahelegt, dass dieses Programm das Eindringen von Immunzellen erleichtern könnte.
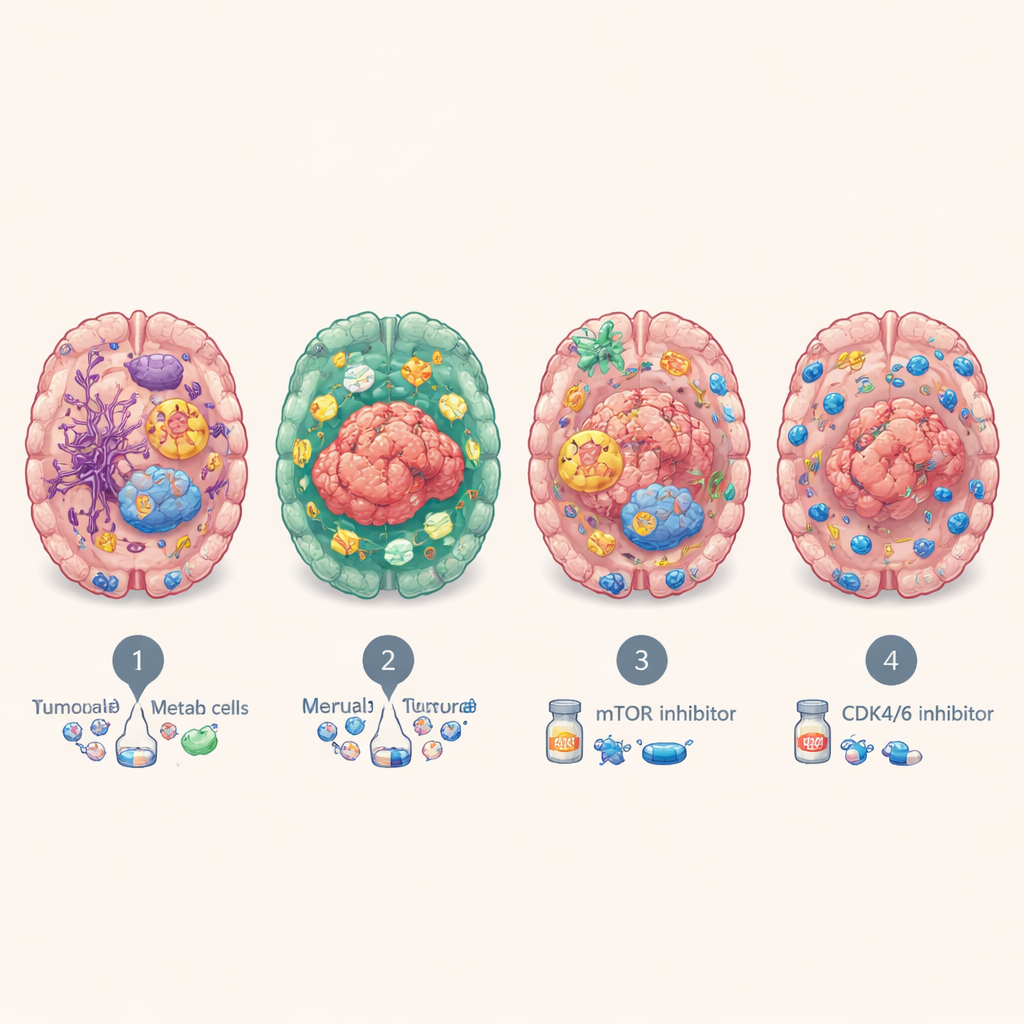
Anhaltspunkte für Behandlung und Patientenergebnisse
Diese molekularen Persönlichkeiten waren nicht nur akademisch relevant. Patientinnen und Patienten mit dem immun-infiltrierten BrMS2-Subtyp hatten tendenziell bessere Überlebenszeiten als diejenigen mit dem proliferativen BrMS4-Subtyp, der durchweg die schlechtesten Ergebnisse aufwies. Durch Wirkstofftests an patientenabgeleiteten Organoiden fanden die Forschenden heraus, dass die metabolischen BrMS3-Tumoren besonders empfindlich gegenüber der Hemmung des mTOR‑Signalwegs sind, der Zellwachstum und Stoffwechsel steuert, und dass die schnell teilenden BrMS4-Tumoren anfälliger für CDK4/6‑Inhibitoren sind, Medikamente, die den Zellzyklus verlangsamen. Separate Analysen deuteten darauf hin, dass BrMS1-Tumoren möglicherweise besser auf Strahlentherapie ansprechen, während die entzündete, checkpointreiche Umgebung von BrMS2 ein größeres Potenzial für Immuntherapien haben könnte, die erschöpfte T‑Zellen wiederbeleben—wobei dies noch durch direkte Studien an Patientinnen und Patienten mit Hirnmetastasen bestätigt werden muss.
Was das für Menschen mit Hirnmetastasen bedeutet
Dieser Atlas zeigt, dass sich Krebszellen, sobald sie das Gehirn erreicht haben, dazu neigen, in einige wenige gemeinsame biologische Zustände zu konvergieren, die die ursprüngliche Herkunft überschneiden. Zu wissen, ob eine Hirnmetastase neural-ähnlich, immunreich, metabolisch oder hochproliferativ ist, könnte künftig helfen, Behandlungen gezielter zu wählen—etwa zwischen Strahlentherapie, Immuntherapie oder Medikamenten, die Stoffwechsel oder Zellteilung angreifen. Obwohl die Arbeit die Standardversorgung noch nicht verändert, liefert sie eine detaillierte Roadmap für zukünftige Forschung und klinische Studien, mit dem Ziel, diese molekularen Verwundbarkeiten in bessere, präzisere Therapien für Patientinnen und Patienten mit Hirnmetastasen zu übersetzen.
Zitation: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Schlüsselwörter: Hirnmetastase, Tumorsubtypen, Tumormikroumgebung, Krebsimmuntherapie, Krebsstoffwechsel