Clear Sky Science · de
Tiefsee‑hydrothermale Umwandlung treibt die Entwicklung von einfachen Alkanen zu präbiotischer molekularer Komplexität
Heiße Quellen am Meeresgrund
Tief unter der Meeresoberfläche, wo nie Sonnenlicht hinkommt, sprudeln heiße Flüssigkeiten aus felsigen Schloten auf dem Meeresboden. Diese Tiefsee‑Heißwasserquellen, oder hydrothermalen Schlote, sind nicht nur geologische Kuriositäten – sie könnten die chemischen Motoren gewesen sein, die einfache Kohlenstoffmoleküle in den reichhaltigen organischen „Eintopf“ verwandelten, aus dem das Leben hervorging. Diese Studie untersucht, wie solche natürlichen Reaktoren grundlegende Zutaten wie einfache Kohlenwasserstoffe schrittweise in weit komplexere, lebensnahe Moleküle umwandeln können.
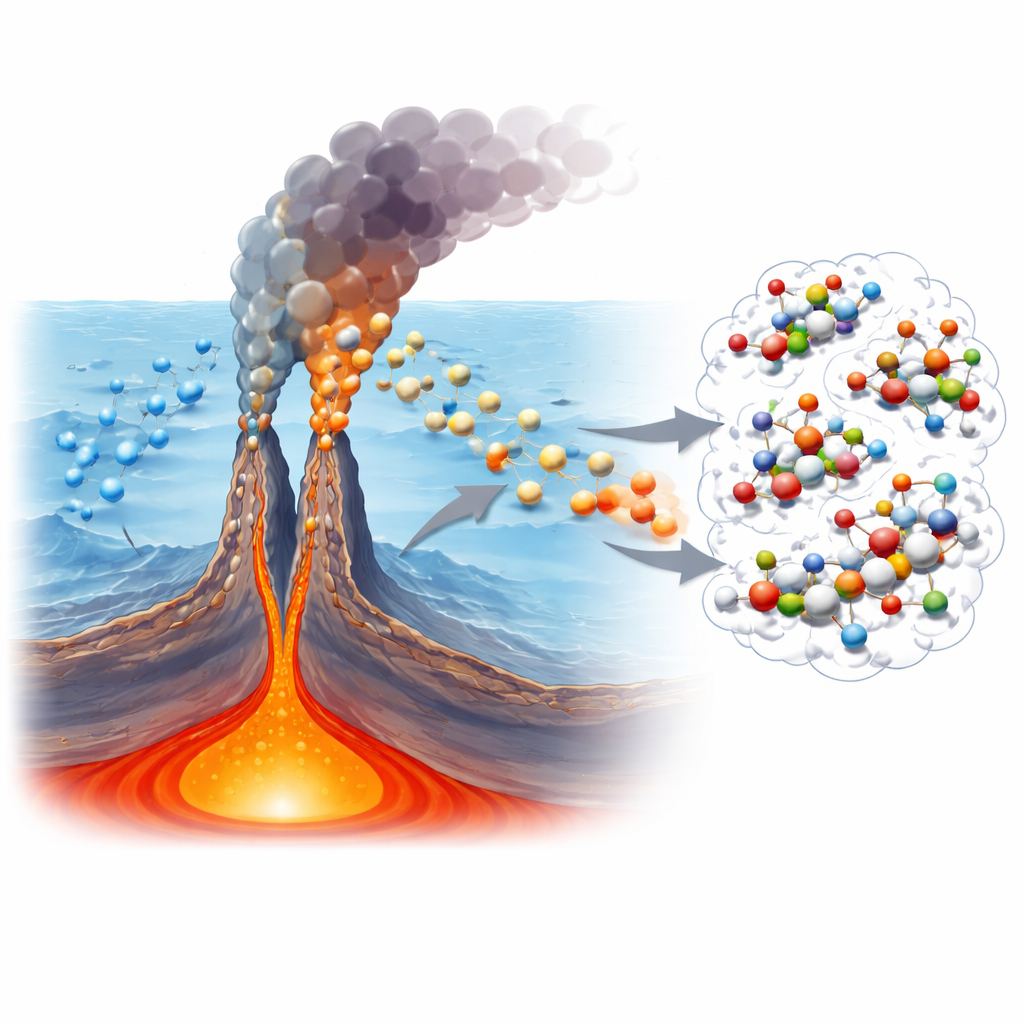
Wo Feuer auf Ozean trifft
Die in dieser Arbeit untersuchten Schlote liegen entlang des ultralangsam spreizenden Indischen Rückens, einem tiefen Riss im Meeresboden, wo das Innere der Erde auf den Ozean trifft. Hier sickert Meerwasser in die Kruste, erhitzt sich auf Hunderte Grad Celsius, reagiert mit Gestein und Metallen und tritt dann durch schlotartige Strukturen wieder aus. Diese Flüssigkeiten transportieren reduzierte Kohlenstoffverbindungen wie Methan und einfache Alkane sowie Wasserstoff, Sulfid und Metalle – genau die Art chemischer Energie, von der viele Forscher denken, dass sie die frühesten Schritte hin zum Leben angetrieben hat. Bislang blieb jedoch ein großes Rätsel: Wie entwickeln sich diese Grundstoffe zu komplexeren, funktionalen Molekülen, die als Vorläufer von Aminosäuren, Nukleobasen und anderen Bausteinen der Biologie dienen könnten?
Den chemischen Stammbaum lesen
Um diese Frage anzugehen, entlehnten die Forscher Werkzeuge der modernen Metabolomik – der Untersuchung kleiner Moleküle in lebenden Systemen – und wandten sie auf Gesteine aus aktiven und inaktiven Schloten an drei Standorten an: Longqi, Edmond und Kairei. Mit hochauflösender Massenspektrometrie zerlegten sie komplexe Gemische in einzelne molekulare „Fingerabdrücke“ und nutzten anschließend rechnerische Methoden, um verwandte Strukturen zu clustern. Das Ergebnis ist eine Art chemischer Stammbaum, der abbildet, wie Moleküle strukturell zueinander in Beziehung stehen, ähnlich wie evolutionäre Bäume verwandte Arten verknüpfen. Statt biologische Abstammung nachzuzeichnen, verfolgt diese „geochemische Phylogenie“, wie Hitze, Minerale und sich ändernde Redoxbedingungen Kohlenstoffverbindungen im Laufe der Zeit umformen.
Von geraden Ketten zu komplexen Netzen
Der molekulare Baum zeigt einen eindrücklichen, geordneten Verlauf. An einem Ende dominieren in den Schlottproben einfache, gerade und verzweigte Alkane – grundlegende Ketten aus Kohlenstoff und Wasserstoff. Entlang des Baums weichen diese Ketten ringförmigen und fusionierten aromatischen Strukturen, die in heißeren, aktiven Schloten stärker auftreten. Weiter entlang nehmen die Moleküle Stickstoff, Schwefel und Sauerstoff auf und bilden heterocyclische Ringe, Amide, Säuren und andere polare Verbindungen, die stärker mit Wasser und Mineralien interagieren. Dieser Trend – von Kette zu Ring zu heteroatomreichen Strukturen – deutet darauf hin, dass hydrothermale Bedingungen Organika nicht einfach zerstören; sie treiben eine schrittweise Zunahme an Komplexität und chemischer Vielseitigkeit voran.
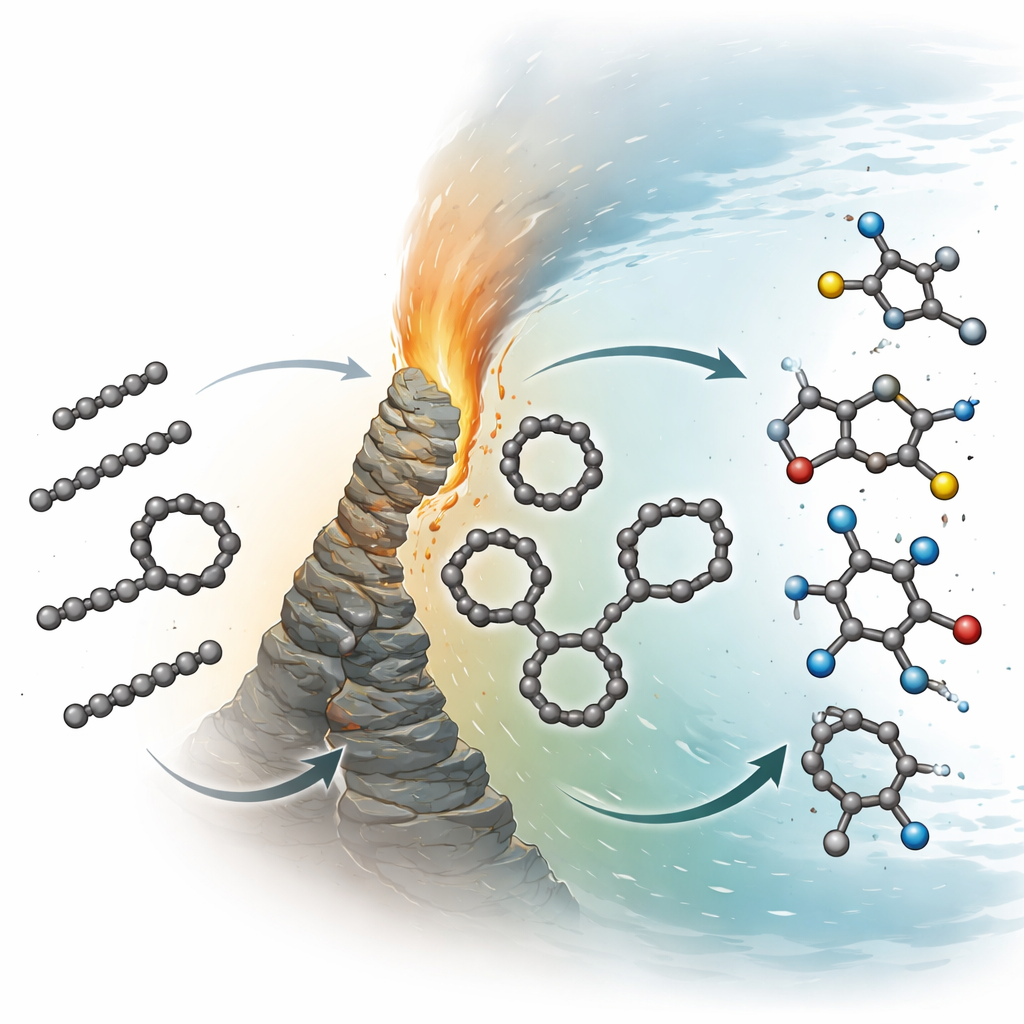
Wenn Schlote ruhen, zieht Stickstoff ein
Ein weiterer zentraler Befund ergibt sich beim Vergleich heißer, kräftig ausströmender Standorte mit nahegelegenen Schloten, die abgekühlt und verstummt sind. Ultrahochaufgelöste Messungen intakter Moleküle zeigen, dass aktive Schlote relativ arm an stickstoffhaltigen Organika sind, obwohl sie reich an reduziertem Kohlenstoff sind. Wenn Schlote abkühlen und inaktiv werden, nimmt die allgemeine Moleküldiversität zu, und stickstoffhaltige Verbindungen werden deutlich häufiger. Dieses Muster, das über mehrere Feldgebiete konsistent beobachtet wird, deutet darauf hin, dass das Erlöschen und die Abkühlung von Schloten Reaktionen begünstigt, die Stickstoff und zusätzliches Sauerstoff einbauen – etwa Aminierung und Nitrierung – wodurch stabilere, stickstoffreiche Moleküle in den Schlotwänden akkumulieren und bestehen bleiben können.
Warum das für Leben hier und anderswo wichtig ist
In der Gesamtschau zeichnen diese Ergebnisse Tiefsee‑Hydrothermalquellen als dynamische Reaktoren, die einfache Kohlenstoffketten in zunehmend funktionale und polare Moleküle umwandeln können, einschließlich stickstoffreicher Spezies, die der Chemie von Aminosäuren und Nukleobasen näherkommen. Statt eines chaotischen Durcheinanders folgt die Chemie erkennbaren Pfaden, geformt von Temperatur, Mineraloberflächen und Redoxgradienten: Heiße, aktive Schlote begünstigen anfängliche Kohlenstoffreduktion und Ringbildung, während kühlere, abklingende Schlote komplexere, stickstoffhaltige Strukturen fixieren. Diese progressive, reproduzierbare Entwicklung von einfachen Alkanen zu präbiotisch anmutender Komplexität schließt die Lücke zwischen Tiefen‑Kohlenstoff der Erde und den ersten Bausteinen des Lebens – und liefert einen Leitfaden dafür, wonach Wissenschaftler bei der Suche nach vergangenem oder gegenwärtigem Leben in hydrothermalen Umgebungen auf dem Mars und bei eisbedeckten Ozeanwelten suchen sollten.
Zitation: Liu, Q., Xu, H., Wang, J. et al. Abyssal hydrothermal alteration drives the evolution from simple alkanes to prebiotic molecular complexity. Nat Commun 17, 2415 (2026). https://doi.org/10.1038/s41467-026-68745-1
Schlüsselwörter: hydrothermale Schornsteine, Ursprung des Lebens, präbiotische Chemie, organische Moleküle, Tiefseengeologie