Clear Sky Science · de
Die Phospholipidzusammensetzung beeinflusst stark den Einbau von β-Fass-Proteinen in gereinigte bakterielle Außenmembranen
Warum bakterielle Hüllen wichtig sind
Arzneimittelresistente „Superkeime“ stellen eine wachsende Bedrohung dar, weil viele Antibiotika einfach nicht durch ihre robusten äußeren Abwehrschichten hindurchkommen. Diese Studie untersucht eingehend einen Schlüsselteil dieser Abwehr bei gramnegativen Bakterien wie E. coli: eine schützende Außenhülle, die mit fassförmigen Proteinen und spezialisierten Fetten dicht gepackt ist. Indem die Autoren untersuchen, wie die Mischung dieser Fette den Aufbau der Außenhülle steuert, zeigen sie Schwachstellen auf, die bei der Entwicklung künftiger Antibiotika ausgenutzt werden könnten.
Der doppelwandige Schutz
Gramnegative Bakterien sind ungewöhnlich, weil sie zwei Membranen haben. Die innere Membran übernimmt die alltäglichen Zellfunktionen, während die äußere Membran wie ein widerstandsfähiger Regenmantel wirkt und viele Gifte und Antibiotika abwehrt. Diese äußere Schicht besteht aus zwei Lipidtypen: üblichen Phospholipiden auf der inneren Seite und einem starren Zucker‑Fett‑Molekül namens Lipopolysaccharid (LPS) auf der äußeren Seite. Durch diese Hülle verlaufen viele „β‑Fass“-Proteine — hohle Zylinder, die Poren und Tore für Nährstoffe bilden. Eine molekulare Maschine namens BAM (für barrel assembly machine) ist dafür verantwortlich, diese Proteine zu falten und in die Außenmembran einzubauen.
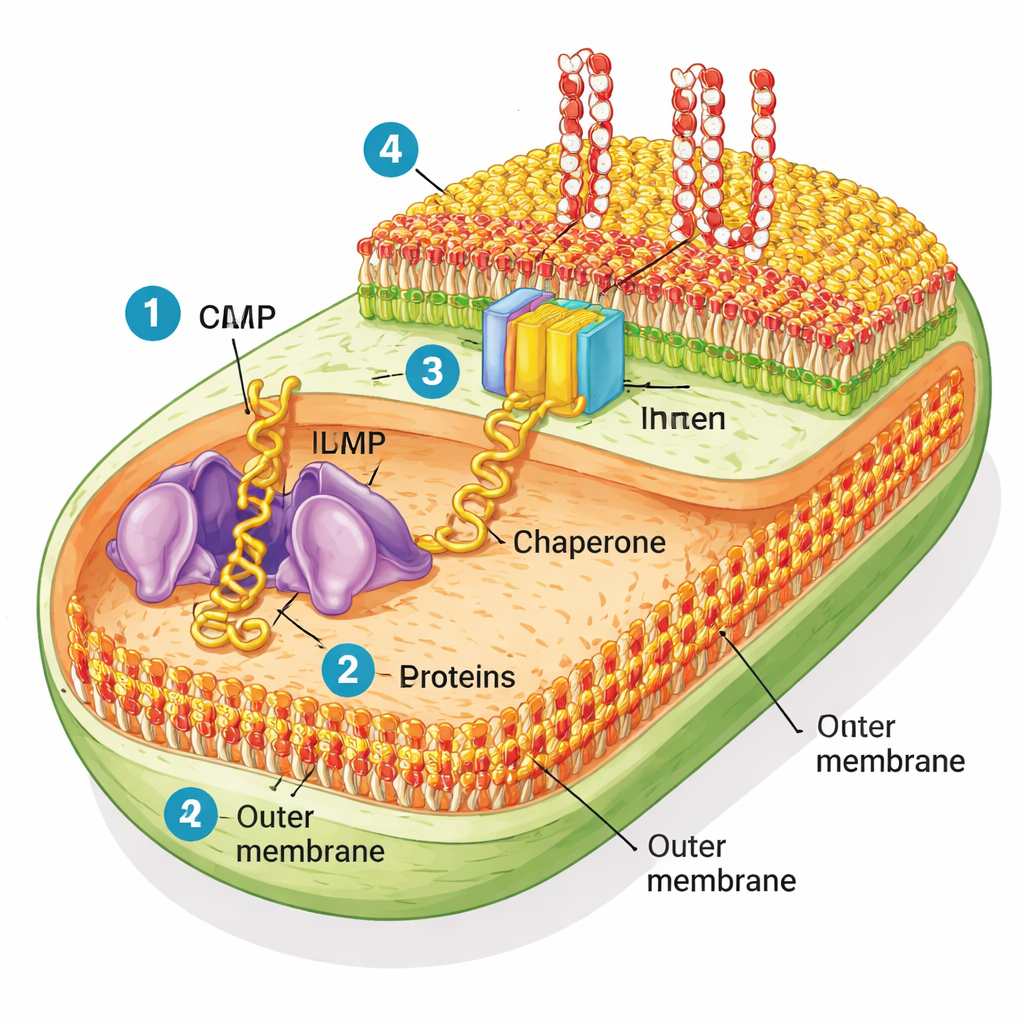
Die bakterielle Hülle im Reagenzglas nachbauen
Um zu prüfen, wie gut BAM in einer realistischen Umgebung arbeitet, haben die Forscher Stücke der E. coli‑Außenmembran gereinigt und winzige Bläschen erzeugt, die sie „native OMs“ nennen. Im Gegensatz zu einfachen künstlichen Membranen, die in vielen Laborstudien verwendet werden, behalten diese nativen Membranen ihre vollständige Mischung aus Proteinen und Lipiden. Das Team nutzte dann eine zellfreie Proteinfabrik, um neue Außenmembranproteine von Grund auf zu synthetisieren, und beobachtete, ob BAM in diesen nativen Bläschen sie falten und einbauen konnte. Sie konzentrierten sich auf ein Modell‑β‑Fass‑Protein namens EspP sowie einige weitere Proteine. Wenn das Helferprotein SurA vorhanden war, faltete BAM in den nativen Membranen EspP effizient, und dieser Prozess wurde durch ein bekanntes BAM‑zielendes Antibiotikum namens Darobactin blockiert — ein klarer Beleg dafür, dass die natürliche Maschine aktiv blieb.
Wenn die Fettmischung aus dem Gleichgewicht gerät
Die Autoren fragten als Nächstes, was passiert, wenn das Lipidgleichgewicht der Außenmembran gestört wird. Sie untersuchten Mutantenstämme von E. coli, denen Schlüsselmechanismen fehlen, die fehlplatzierte Phospholipide in der äußeren Schicht normalerweise korrigieren. Ein System, MlaA, transportiert abweichende Phospholipide zurück zur inneren Membran; ein anderes, das Enzym PldA, baut sie ab. Mit nativen Membranen aus diesen Mutanten stellten die Forscher fest, dass der von BAM getriebene Einbau von EspP in Stämmen ohne MlaA deutlich zurückging und bei fehlendem PldA stark beeinträchtigt war. Diese Effekte resultierten nicht aus dem Verlust von BAM selbst oder anderen wichtigen Proteinen, die weiterhin in normalen Mengen vorhanden waren, sondern deuteten stattdessen auf die veränderte Lipidumgebung als Ursache hin.
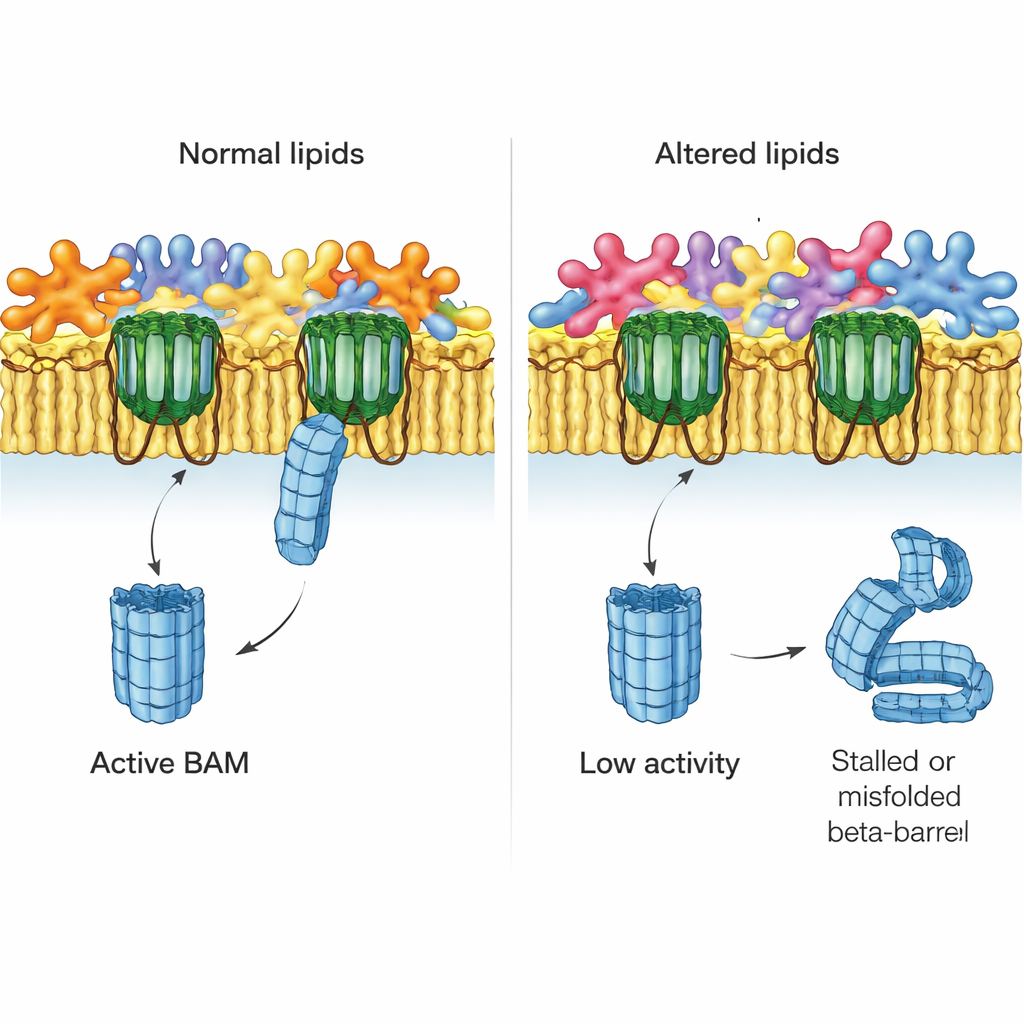
Die Lipidlandschaft im Detail kartieren
Um Funktion mit Chemie zu verknüpfen, entwickelten die Forscher eine empfindliche Massenspektrometriemethode, um Hunderte einzelner Phospholipide in ganzen Zellen und in gereinigten Außenmembranen zu katalogisieren. In normalem E. coli bestätigten sie, dass ein Lipidtyp (Phosphatidylethanolamin, oder PE) in der Außenmembran angereichert ist, während andere (Phosphatidylglycerol und Cardiolipin) dort relativ vermindert vorkommen. Sie fanden auch, dass „Lyso‑Lipide“, die nur einen Fettschwanz haben und dazu neigen, Membranen zu krümmen, überraschend in der Außenmembran konzentriert sind. In Mutantenstämmen, insbesondere solchen ohne PldA, waren diese Muster durcheinander: die üblichen Unterschiede zwischen innerer und äußerer Membran schrumpften oder kehrten sich sogar um, und die Längen und Typen der Fettschwänze verschoben sich. Die Stämme mit den stärksten Lipidstörungen waren dieselben, in denen BAM am schlechtesten funktionierte.
Folgen für Antibiotikastrategien
Zusammengefasst zeigt die Arbeit, dass die Außenmembran nicht nur ein passives Gerüst für Proteine ist. Ihre präzise Phospholipidzusammensetzung beeinflusst stark, wie gut BAM die β‑Fass‑Poren aufbauen kann, die das Bakterium am Leben erhalten. Wenn das Lipidgleichgewicht gestört ist, funktionieren weniger BAM‑Komplexe korrekt, und einige arbeiten langsamer. Obwohl lebende Bakterien solche Veränderungen auf Weisen kompensieren können, die ein Reagenzglassystem nicht nachbildet, unterstreicht diese Studie, wie das gezielte Abstimmen oder Stören bestimmter Lipide die bakterielle Hülle schwächen könnte. Diese Einsicht eröffnet neue Möglichkeiten für Wirkstoffe, die entweder BAM direkt angreifen oder die Lipide der Außenmembran subtil aus dem Gleichgewicht bringen, sodass selbst die widerstandsfähigsten gramnegativen Bakterien anfälliger werden.
Zitation: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Schlüsselwörter: Gramnegative Bakterien, Außenmembranproteine, β-Fass‑Assemblierung, bakterielle Lipide, Antibiotikaresistenz