Clear Sky Science · de
Kynurenin vermittelt die durch Chemotherapie verursachte Darmtoxizität über die Modulation des Darmmikrobioms
Warum das für Menschen unter Chemotherapie wichtig ist
Chemotherapie rettet Leben, bringt aber häufig quälende Nebenwirkungen im Darm mit sich – Schmerzen, Durchfall, Gewichtsverlust –, die Ärzte dazu zwingen können, Dosen zu reduzieren oder die Behandlung vorzeitig abzubrechen. Diese Studie legt eine bislang verborgene Kaskade aus einem im Blut zirkulierenden Molekül, Immunzellen und Darmmikroben offen, die erklärt, warum ein häufig eingesetztes Krebsmedikament, Oxaliplatin, so stark auf den Darm wirken kann, und weist auf neue Wege hin, Patienten zu schützen, ohne die krebsbekämpfende Wirkung zu schwächen.
Eine chemische Verbindung zwischen Therapie und Darmschaden
Die Forschenden begannen mit Patienten mit kolorektalem Krebs, die eine Oxaliplatin-basierte Chemotherapie erhielten. Sie verglichen Blutproben von Personen, die schwere Darmnebenwirkungen entwickelten, mit solchen, die die Behandlung besser verkrafteten. Mithilfe gezielter chemischer Analysen stellten sie fest, dass mehrere Abbauprodukte der Aminosäure Tryptophan in der Gruppe mit hoher Toxizität erhöht waren; ein Molekül – L‑kynurenin – fiel dabei als am stärksten erhöht auf. Patientinnen und Patienten mit mehr L‑kynurenin im Blut zeigten zudem stärkere Entzündungszeichen und niedrigere Leukozytenzahlen, was darauf hindeutet, dass dieses Molekül direkt mit therapiebedingten Schäden verbunden sein könnte.
Kausalitätsnachweis in Mäusen
Um über Korrelationen hinauszukommen, nutzte das Team Mausmodelle. Gesunden Mäusen, die hohe Dosen Oxaliplatin erhielten, zeigten klassische Anzeichen einer Darmverletzung: Gewichtsverlust, verkürzte Kolonlänge, Verdickung der Darmwand, weniger teilende Zellen und mehr sterbende Zellen im Darmephitel. Diese Mäuse wiesen ebenfalls einen starken Anstieg von L‑kynurenin im Blut auf, was die Humanbefunde widerspiegelt. Wenn den Oxaliplatin-behandelten Mäusen zusätzliches L‑kynurenin verabreicht wurde, verschlechterte sich der Darm Schaden weiter – die tumorhemmende Wirkung des Medikaments blieb jedoch erhalten. Umgekehrt waren Mäuse, bei denen das Enzym IDO1, das Tryptophan in L‑kynurenin umwandelt, entfernt oder blockiert wurde, deutlich widerstandsfähiger gegen Darmtoxizität und profitierten weiterhin von der Chemotherapie.
Immunzellen und Darmmikroben im Kreuzfeuer
Bei tiefergehenden Untersuchungen fragten die Wissenschaftler, welche Zellen während der Behandlung überschüssiges L‑kynurenin produzieren. Sie fanden heraus, dass Oxaliplatin bestimmte Immunzellen (CD8-T-Zellen) dazu anregt, das Signalmolekül Interferon‑gamma freizusetzen, das wiederum IDO1 in benachbarten myeloiden Zellen – einer Klasse von weißen Blutzellen – aktiviert. Mäuse, bei denen IDO1 nur in myeloiden Zellen fehlte, produzierten deutlich weniger L‑kynurenin und waren vor Darmverletzungen geschützt, während das Entfernen von IDO1 nur in Darmepithelzellen kaum Wirkung zeigte. Gleichzeitig verschob sich die Zusammensetzung des Darmmikrobioms: Bei normalen Mäusen waren Oxaliplatin und hohe L‑kynurenin-Werte mit dem Verlust eines hilfreichen Bakteriums, Lactobacillus johnsonii, verbunden. Im Gegensatz dazu behielten Mäuse mit reduziertem L‑kynurenin höhere Anteile von L. johnsonii. Wurden die Darmbakterien mit Antibiotika beseitigt, verschwand der schützende Effekt niedriger L‑kynurenin-Werte, und wenn Bakterien von Mäusen mit niedrigem L‑kynurenin in normale Mäuse transplantiert wurden, wurden diese Empfänger widerstandsfähiger gegen Oxaliplatin-bedingte Darmschäden.
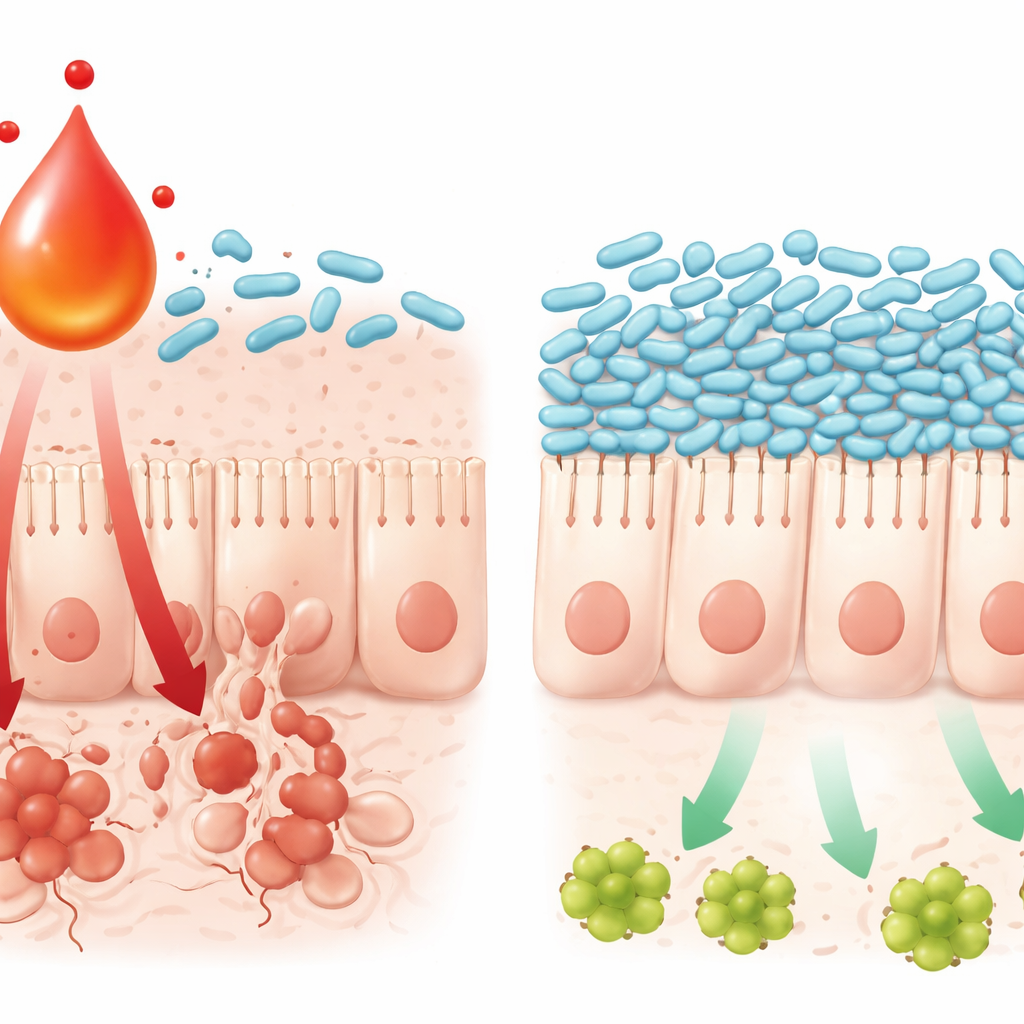
Wie ein Metabolit den Zelltod im Darm antreibt
Die Studie verfolgte außerdem nach, wie diese Chemie–Mikroben-Interaktion das Darmephitel schädigt. Hohe L‑kynurenin-Werte korrelierten mit einer erhöhten Aktivität eines bekannten Entzündungswegs im Darmgewebe, dem TNFα/JNK-Signalweg, der Zellen in Richtung programmierter Zelltod treibt. In Zellkultur erhöhten die Kombination aus Oxaliplatin und L‑kynurenin die Wahrscheinlichkeit, dass Darmzellen diesen Weg aktivieren und absterben, während die Zugabe von L. johnsonii das Signal abschwächte und das Überleben der Zellen erhielt. L‑kynurenin selbst konnte das Wachstum und die Überlebensmechanismen von L. johnsonii in Zellkulturen verlangsamen und beeinträchtigen, was erklärt, warum das Bakterium verschwindet, wenn der Metabolit sich anreichert. Zusammengenommen zeichnen diese Befunde eine sich selbst verstärkende Schleife: Chemotherapie löst immunologisches Signal aus, Immunzellen erhöhen L‑kynurenin, dies stört schützende Bakterien wie L. johnsonii, und die veränderte mikrobielle Gemeinschaft verstärkt wiederum entzündliche Signale, die Darmzellen abtöten.
Neue Ansätze, Patienten während der Behandlung zu schützen
Ermutigend weisen die Ergebnisse auch auf praktikable Strategien hin. Die Behandlung von Mäusen mit einem Wirkstoff namens Epacadostat, der IDO1 hemmt, senkte L‑kynurenin-Werte und reduzierte die durch Oxaliplatin verursachte Darmverletzung deutlich, ohne die Tumorkontrolle zu beeinträchtigen. In einem komplementären Ansatz konstruierten die Forschenden einen harmlosen E.-coli-Stamm so, dass er ein Enzym überproduziert, das L‑kynurenin im Darm abbaut. Mäuse, die diese gentechnisch veränderten Bakterien erhielten, waren ebenfalls vor Darmtoxizität geschützt, wiederum ohne die krebsbekämpfende Wirkung der Chemotherapie zu schmälern. Auch die Gabe von L. johnsonii selbst milderte die Symptome und bewahrte die Darmstruktur.
Was das für Krebspatientinnen und -patienten bedeutet
In der Summe zeigt die Studie, dass ein einzelner, behandlungsgetriebener Metabolit – L‑kynurenin – als zentraler Vermittler zwischen Chemotherapie, Immunsystem, Darmmikroben und Darmverletzung wirkt. Indem sie demonstriert, dass die Blockade seiner Produktion, die Förderung seines Abbaus oder die Wiederherstellung schützender Bakterien die Belastungen der Chemotherapie im Darm abschwächen können, öffnet die Forschung den Weg zu Zusatztherapien, die Patientinnen und Patienten stärken und ihren Komfort verbessern können, ohne die Krebsbehandlung zu untergraben.
Zitation: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Schlüsselwörter: Nebenwirkungen der Chemotherapie, Darmmikrobiom, Tryptophanstoffwechsel, L-kynurenin, kolorektales Karzinom