Clear Sky Science · de
Gemcitabin plus Selinexor bei selektiven fortgeschrittenen Sarkomen: eine Phase‑I‑Studie der spanischen Sarkomforschungsgruppe
Neue Hoffnung für eine seltene und schwere Krebserkrankung
Sarkome sind seltene Krebserkrankungen, die häufig jüngere Erwachsene betreffen und nach Metastasierung schwer zu behandeln sind. Für viele Patientinnen und Patienten halten die verfügbaren Therapien die Erkrankung nur für kurze Zeit unter Kontrolle. In dieser Studie wurde eine neue Wirkstoffkombination geprüft – ein etabliertes Chemotherapeutikum, Gemcitabin, kombiniert mit einer neueren zielgerichteten Tablette, Selinexor – um zu untersuchen, ob das Zusammenwirken beider Wirkstoffe fortgeschrittene Sarkome besser verlangsamen oder verkleinern kann, ohne unbeherrschbare Nebenwirkungen zu verursachen.
Warum die Kombination von zwei Medikamenten besser wirken könnte
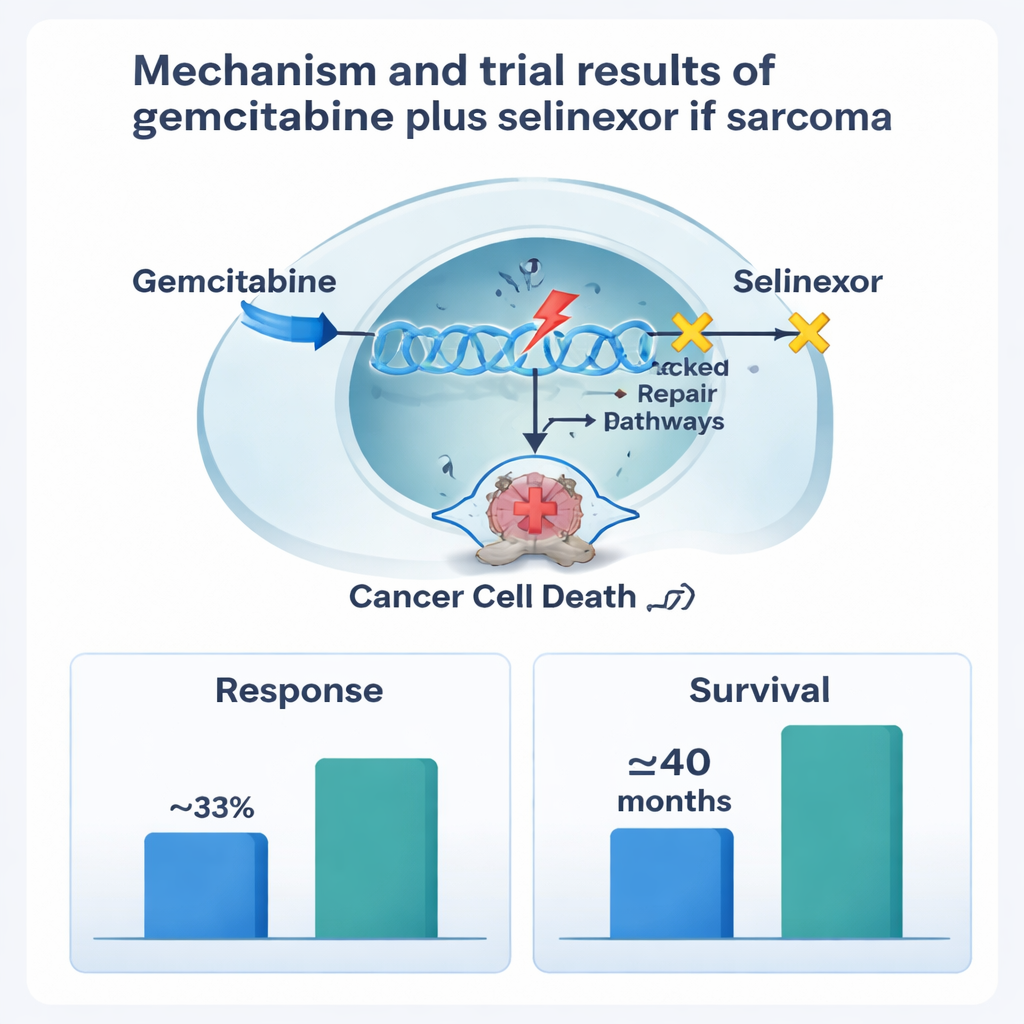
Gemcitabin ist eine Standardchemotherapie, die die DNA sich schnell teilender Zellen, einschließlich Krebszellen, schädigt. Selinexor wirkt auf ganz andere Weise: Es hemmt ein Protein namens Exportin‑1, das normalerweise wichtige Regulationsproteine aus dem Zellkern transportiert. Wenn Exportin‑1 überaktiv ist, wie bei vielen Tumoren, können Krebszellen den körpereigenen „Stoppsignalen“ entkommen und gegen Therapien resistent werden. Indem selinexor tumorunterdrückende Proteine im Zellkern zurückhält, kann es Krebszellen in Richtung Selbstzerstörung treiben. Laborarbeiten legten nahe, dass die Verabreichung von Gemcitabin zur DNA‑Schädigung gefolgt von Selinexor zur Blockade von Reparatur‑ und Überlebenswegen in bestimmten Sarkomen besonders wirksam sein könnte.
Vielversprechende Hinweise aus Laborversuchen
Bevor Patientinnen und Patienten behandelt wurden, testete das Forscherteam die beiden Wirkstoffe gemeinsam an im Labor gezüchteten Krebszellen und konzentrierte sich dabei auf drei Sarkomtypen: Leiomyosarkom, Osteosarkom und maligne periphere Nervenscheidentumoren. In mehreren Zelllinien von Leiomyosarkomen und Nervenscheidentumoren tötete die Kombination mehr Krebszellen als jeder Wirkstoff allein und zeigte echte Synergie. Diese Zellen wiesen bei kombinierter Behandlung stärkere DNA‑Schäden und höhere Raten programmierter Zelltodmechanismen auf. Das Team untersuchte zudem Proteine, die Zellen beim Überleben und bei der Teilung unterstützen, etwa das Protein Survivin. Wenn Selinexor die Survivin‑Spiegel stark senkte und ein weiteres Protein, IκBα, veränderte, war die Kombination besonders erfolgreich. Im Gegensatz dazu zeigten Osteosarkomzellen häufig den gegenteiligen Effekt: Die beiden Medikamente beeinträchtigten sich gegenseitig, was darauf hindeutet, dass dieser Ansatz nur für ausgewählte Sarkomtypen von Nutzen sein könnte.
Wie die Studie bei Patientinnen und Patienten durchgeführt wurde
Die klinische Studie rekrutierte 17 Erwachsene in Spanien mit fortgeschrittenen Sarkomen, die bereits trotz mindestens einer Standardtherapie gewachsen waren. Die Mehrheit hatte ein Leiomyosarkom; eine kleinere Zahl litt an Osteosarkom oder zwei anderen seltenen Sarkomen. Die Untersucher verwendeten ein sorgfältiges stufenweises Design, um die höchste Dosis zu finden, die Patientinnen und Patienten sicher tolerieren konnten. Alle erhielten Gemcitabin intravenös an den Tagen 1 und 8 eines dreiwöchigen Zyklus, gefolgt von wöchentlichen Selinexor‑Tabletten. Das Team überwachte in den ersten Behandlungszyklen genau schwere Nebenwirkungen, um die empfohlene Dosis für Folgestudien festzulegen.
Sicherheit, Nebenwirkungen und erste Nutzenzeichen
Die wichtigsten Nebenwirkungen waren Abfälle der Blutwerte – vor allem der weißen Blutkörperchen und der Blutplättchen –, wie sie häufig bei Chemotherapien auftreten. Diese waren häufig, ließen sich aber in der Regel mit Wachstumsfaktor‑Injektionen, Dosisanpassungen und Behandlungsunterbrechungen gut managen. Übelkeit, Erbrechen und Müdigkeit traten ebenfalls häufig auf, waren überwiegend leicht bis mäßig ausgeprägt, und kein Patient musste die Studie aufgrund von Toxizität abbrechen. Die abschließend empfohlene Dosis hielt Gemcitabin auf einem relativ hohen Niveau, während Selinexor wöchentlich etwas niedriger dosiert wurde, um die Verträglichkeit zu verbessern. Unter 16 Patientinnen und Patienten mit messbaren Tumoren zeigten fünf eine deutliche Tumorverkleinerung und weitere fünf erreichten eine stabile Erkrankung, was zu einer Gesamtansprechrate von etwa 31 Prozent führte. Für die gesamte Gruppe blieb der Krebs median etwa 5 bis 6 Monate unter Kontrolle. Patientinnen und Patienten mit Leiomyosarkom profitierten besonders: Die Erkrankung war im Mittel knapp 8 Monate kontrolliert und das Gesamtüberleben näherte sich dreieinviertel Jahren, wobei die kleine Patientenzahl diese Ergebnisse mit Vorsicht zu interpretieren macht.
Hinweise darauf, wer am meisten profitieren könnte
Da nicht alle Patientinnen und Patienten ansprachen, suchten die Forscher in Tumorproben nach Markern, die einen Nutzen vorhersagen könnten. Hohe Survivin‑Spiegel und starke nukleäre Färbung von IκBα standen beide in Verbindung mit kürzeren progressionsfreien Intervallen, insbesondere beim Leiomyosarkom. Das passt zu den Laborbefunden, wonach ein kompletter Verlust von Survivin mit stärkerer Medikamentensynergie assoziiert ist. Werden diese Befunde in größeren Studien bestätigt, könnten diese Proteine Ärzten helfen, jene Patientinnen und Patienten zu identifizieren, die am wahrscheinlichsten auf die Gemcitabin–Selinexor‑Kombination ansprechen, und jene, die andere Strategien benötigen.
Was das für Patientinnen und Patienten mit Sarkom bedeutet
Für Menschen mit fortgeschrittenen Sarkomen sind die Behandlungsoptionen begrenzt und oft nur von kurzer Wirkdauer. Diese frühe Phase‑I‑Studie zeigt, dass die Kombination von Gemcitabin und Selinexor machbar ist, dass die Nebenwirkungen mit sorgfältiger Unterstützung handhabbar sind und dass es ermutigende Anzeichen für einen Nutzen gibt, besonders beim Leiomyosarkom. Die Untersuchung beginnt zudem, biologische Marker freizulegen, die eine stärkere Individualisierung der Therapie ermöglichen könnten. Größere Phase‑II‑ und Phase‑III‑Studien laufen derzeit, um zu bestätigen, ob diese Kombination tatsächlich das Überleben und die Lebensqualität verbessert. Für Patientinnen, Patienten und Behandelnde stellt sie jedoch einen realistischen neuen Ansatz in der Suche nach besseren Sarkomtherapien dar.
Zitation: Martin-Broto, J., Casado, A., Marquina, G. et al. Gemcitabine plus selinexor in selective advanced sarcomas: a phase I of the Spanish group for research on sarcoma study. Nat Commun 17, 1873 (2026). https://doi.org/10.1038/s41467-026-68729-1
Schlüsselwörter: Sarkombehandlung, Leiomyosarkom, Gemcitabin, Selinexor, Krebs‑klinische Studie