Clear Sky Science · de
Nickelkatalysierte divergente Sulfonierungen von Propargylcarbonaten
Warum diese Chemie über das Labor hinaus Bedeutung hat
Schwefelhaltige Moleküle stehen im Zentrum vieler moderner Arzneimittel, Pflanzenschutzmittel und fortschrittlicher Materialien. Sie präzise, effizient und flexibel herzustellen, ist jedoch oft schwierig. Dieser Artikel beschreibt ein nickelbasiertes katalytisches Verfahren, das einfache Ausgangsstoffe in mehrere verschiedene Familien schwefelreicher Moleküle überführt, dabei die dreidimensionale Struktur streng kontrolliert. Solche Kontrolle kann die Wirkstoffforschung beschleunigen und Chemikern ermöglichen, komplexe Moleküle sauberer und nachhaltiger zu konstruieren.
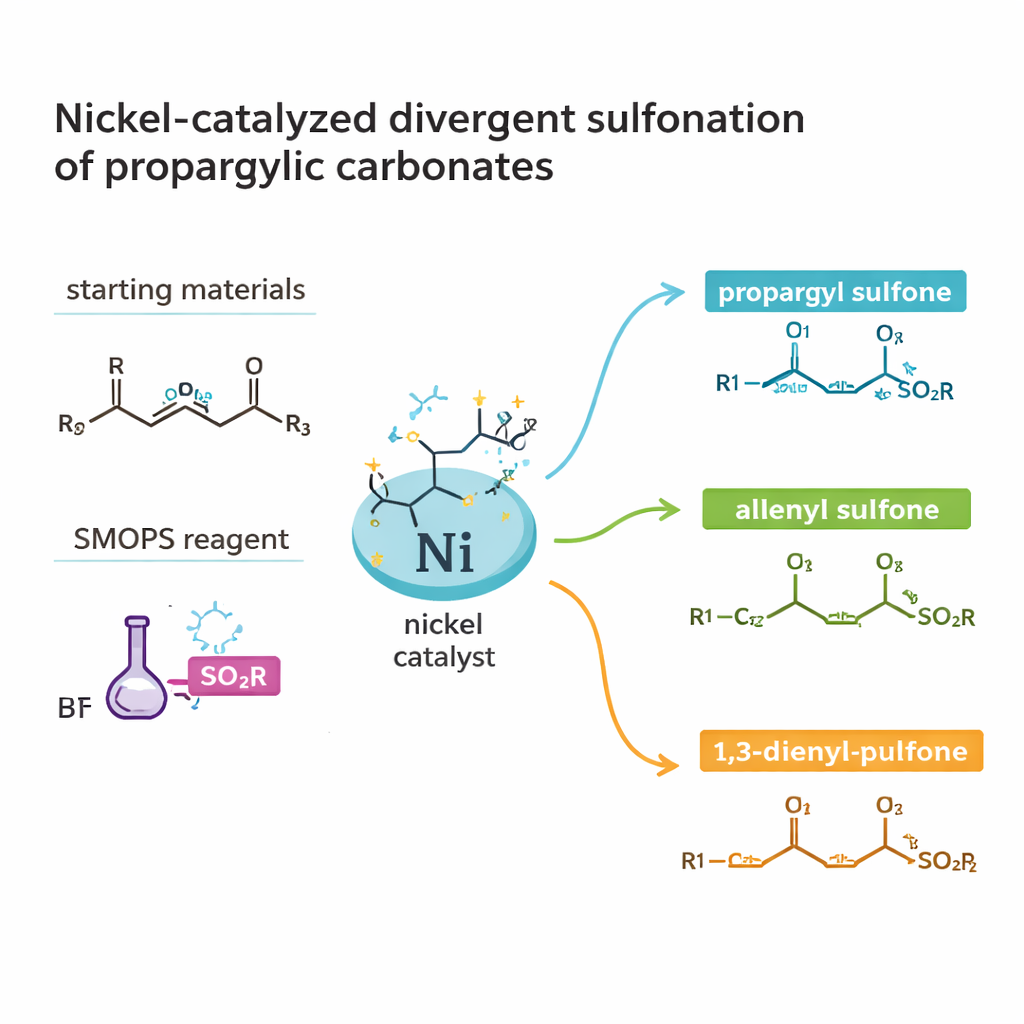
Nützliche Moleküle aus einfachen Bausteinen bauen
Die Arbeit konzentriert sich auf eine Klasse von Verbindungen, die Sulfone und Sulfinate genannt werden und Schwefel enthalten, der an Sauerstoff und Kohlenstoff gebunden ist. Diese Strukturen treten in vielen bioaktiven Naturstoffen und Arzneimitteln auf, aber die klassischen Zugänge sind oft lang und verschwenderisch. Die Autoren fokussieren sich auf einen besonders wertvollen Subtyp: chirale Sulfinate, deren Spiegelbildformen im Körper sehr unterschiedlich reagieren können. Statt von bereits komplexen Bausteinen auszugehen, nutzen sie zwei leicht verfügbare Partner: Propargylcarbonat (eine kleine Kohlenstoffgerüsteinheit mit eingebauter Abgangsgruppe) und eine kommerzielle Schwefelquelle namens SMOPS. Durch die Kombination dieser Komponenten unter Nickelkatalyse zielen sie darauf ab, hochwertige schwefelhaltige Produkte in nur einem oder zwei Schritten zu erhalten.
Ein katalytisches System, drei Produktfamilien
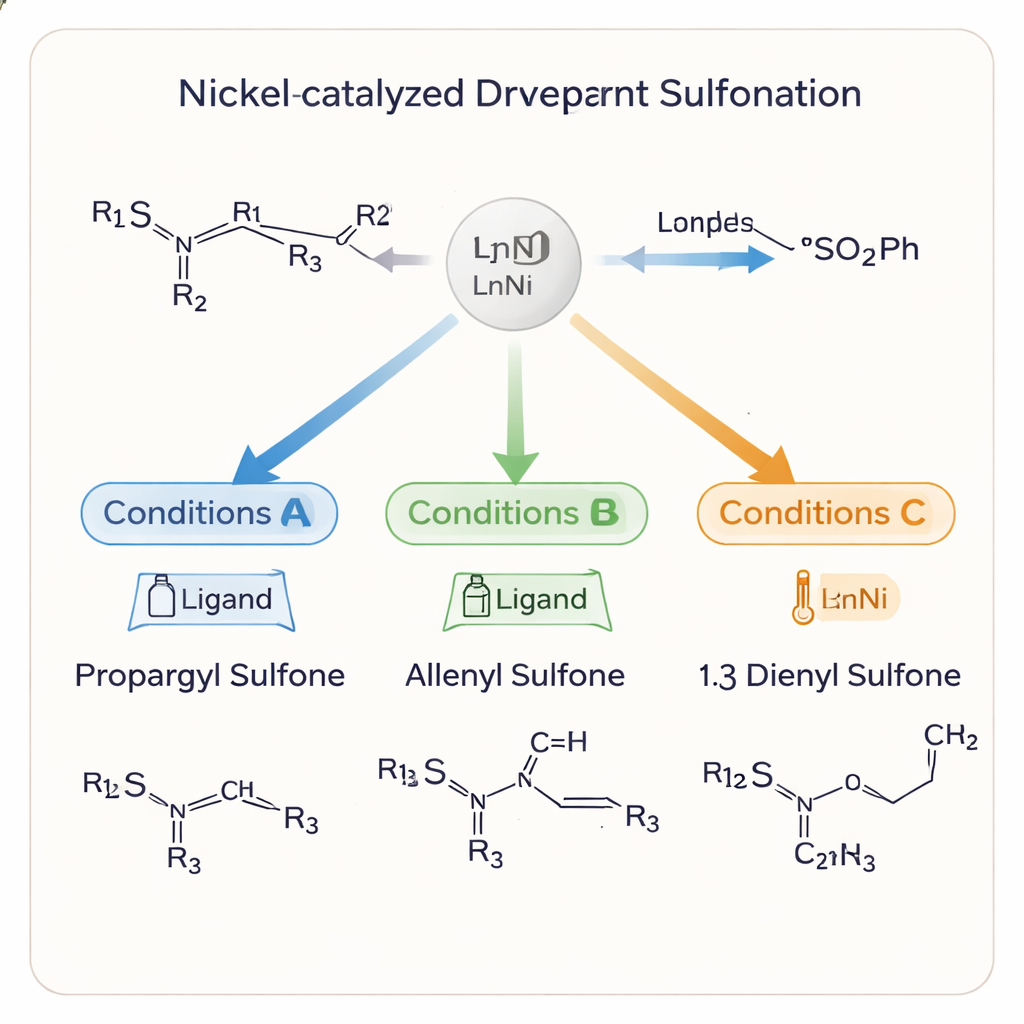
Ein auffälliges Merkmal der Studie ist, dass sich mit den gleichen Grundzutaten drei verschiedene Produkttypen herstellen lassen: Propargylsulfone, Allenylsulfone und 1,3‑dienylsulfone. Jeder dieser Kohlenstoffgerüste führt zu unterschiedlicher Folgechemie und biologischer Aktivität. Durch die gezielte Wahl des an Nickel gebundenen Liganden, Lösungsmittels, der Temperatur und von Additiven kann das Team die Reaktion in die eine oder andere Richtung „steuern“. Unter milden Bedingungen in Acetonitril und mit einem chiralen Phosphinliganden erhalten sie Propargylsulfone in hoher Ausbeute und mit exzellent kontrollierter Händigkeit. Die Behandlung dieser Produkte mit Aluminiumoxid formt die Kohlenstoff‑Dreifachbindung schonend in ein Allenen um, wiederum ohne Verlust der chiralen Information. Der Wechsel zu einem anderen Liganden und Lösungsmittel kanalisiert den Prozess stattdessen in Richtung 1,3‑dienylsulfone und verlängert damit das Kohlenstoffgerüst.
Untersuchung von Umfang und Flexibilität
Um die Allgemeingültigkeit dieses Ansatzes zu testen, variierten die Forschenden beide Reaktionspartner. Sie zeigten, dass viele unterschiedliche Natriumsulfinate — darunter einfache Alkyl‑ und Arylgruppen sowie komplexere Ringsysteme — sauber reagieren und chirale Produkte mit hohem enantiomeren Überschuss liefern. Ebenso funktioniert eine breite Palette von Propargylcarbonaten mit verschiedenen Substituenten am aromatischen Ring oder der Kohlenstoffkette gut, wenngleich einige Substrate mit sehr sperrigen Gruppen oder terminalen Alkinen außerhalb der aktuellen Methode liegen. Das Team demonstriert außerdem, dass sich die Mengen ohne Einbußen bei Effizienz oder Selektivität erhöhen lassen — ein wichtiger Schritt in Richtung praktischer Anwendbarkeit. Dieser weite Anwendungsbereich ermöglicht es Chemikern, viele verschiedene Fragmente zu kombinieren und schnell eine Bibliothek verwandter schwefelhaltiger Moleküle zu erzeugen.
Bausteine in komplexe Ziele überführen
Über die reine Herstellung dieser Sulfone hinaus zeigen die Autoren, wie leicht sich diese in andere nützliche Strukturen umwandeln lassen. Eine Hydrierung wandelt die Dreifachbindung in Alkane oder Alkene um und erhält dabei das chirale Zentrum neben dem Schwefel. Einfache Folgereaktionen verwandeln die Sulfon‑Einheiten in Sulfinate, Sulfonamide und Sulfonylfluoride — Motive, die in der Arzneimittelchemie und bei „click‑artigen“ Kupplungsreaktionen häufig vorkommen. Als besonderes Beispiel nutzen sie ihre Methode als Schrittmacher in einer kompakten Synthese eines chiralen β‑sulfinylhydroxamsäure‑Derivats, einer Molekülklasse, die dafür bekannt ist, bakterielle Enzyme zu hemmen. Dieser Weg umgeht mehrere ältere, umständlichere Schritte und unterstreicht die synthetische Stärke, chirale Sulfinate auf Abruf verfügbar zu haben.
Wie die Reaktion ihren Pfad wählt
Das Team untersucht auch, wie und warum die Reaktion zwischen den Produkten umschaltet. Zeitverlaufsexperimente zeigen, dass sich das Propargylsulfon typischerweise zuerst bildet, dann unter bestimmten Bedingungen in das Allenen und schließlich in das 1,3‑Dien umwandeln kann. Der Nickelkatalysator steuert zusammen mit dem gewählten Liganden und Additiv, welche Zwischenstufen bevorzugt werden und wie sich die Schwefelgruppe entlang der Kohlenstoffkette verschiebt. Aluminiumoxid beispielsweise ermöglicht die Umschichtung Alkin→Allenen bereits bei sehr niedrigen Temperaturen, ohne die dreidimensionale Anordnung der Atome zu zerstören. Ein vereinfachter Mechanismus legt nahe, dass subtile Änderungen der Reaktionsbedingungen ein gemeinsames Nickelzwischenprodukt in unterschiedliche Reaktionspfade lenken und erklärt, wie ein System mehrere präzise definierte Produkte liefern kann.
Was das für zukünftige Medikamente und Materialien bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Dieses nickelkatalysierte Verfahren bietet eine vielseitige chemische „Schaltzentrale“: Aus denselben einfachen Ausgangsstücken können Chemiker gezielt das gewünschte schwefelreiche Gerüst wählen und es in einem einzigen, hochselektiven Schritt erhalten. Da diese Produkte hervorragende Bausteine für Arzneimittel und andere funktionelle Moleküle sind, könnte der Ansatz den Weg vom Konzept bis zum Kandidatenstoff verkürzen. Er zeigt außerdem, wie sorgfältiges Design von Katalysator und Reaktionsbedingungen eine ehemals schwierige Transformation in ein routinemäßiges Werkzeug verwandeln kann und so die schnellere, sauberere Herstellung komplexer, chiraler schwefelhaltiger Moleküle ermöglicht.
Zitation: Gu, W., He, Z., Wang, H. et al. Nickel-catalyzed divergent sulfonations of propargylic carbonate. Nat Commun 17, 1882 (2026). https://doi.org/10.1038/s41467-026-68720-w
Schlüsselwörter: Nickelkatalyse, chirale Sulfone, asymmetrische Synthese, Design organischer Reaktionen, wirkstoffähnliche Bausteine