Clear Sky Science · de
Tumor-intrinsische Merkmale prägen die T‑Zell-Differenzierung vom Präkurzor bis zum symptomatischen Multiplen Myelom
Warum diese Forschung wichtig ist
Das multiple Myelom ist eine Blutkrebserkrankung des Knochenmarks, die fast immer von ruhigeren Frühstadien begleitet wird, die sich — müssen aber nicht — zu einer manifesten Krankheit entwickeln. Viele Menschen leben jahrelang mit diesen Präkanzerosen, ohne zu wissen, ob oder wann ein Fortschreiten stattfindet. Diese Studie stellt eine drängende Frage: Lassen sich die „Stimmung“ und die Vorgeschichte des Immunsystems — insbesondere der T‑Zellen — ablesen, um zu verstehen, wie Myelom entsteht, wie es auf Therapien reagiert und wer das höchste Progressionsrisiko trägt?
Die Späher des Körpers gegen Krebs
T‑Zellen sind vielseitige Immunzellen, die abnorme Zellen, einschließlich Krebszellen, erkennen und zerstören können. Bei soliden Tumoren wie Lungen‑ oder Hautkrebs kann anhaltende Stimulation T‑Zellen in einen erschöpften Zustand treiben, in dem sie unwirksam werden — ein Zustand, den moderne Immuntherapien zu reaktivieren versuchen. Die Autoren stellten eine umfangreiche Einzelzellkarte von mehr als einer Million Zellen aus Knochenmark und Blut von Personen mit multiplem Myelom, dessen Vorstufen (MGUS und smoldering Myelom) und Kontrollen ohne Krebs zusammen. Durch gleichzeitiges Auslesen von Genaktivität und der einzigartigen Rezeptorsequenzen, die jeden T‑Zell‑Klon definieren, rekonstruierten sie die Organisation der T‑Zellen, wie „alt“ oder „erfahren“ diese erscheinen und wie eng sie dem zugrunde liegenden Tumor folgen.
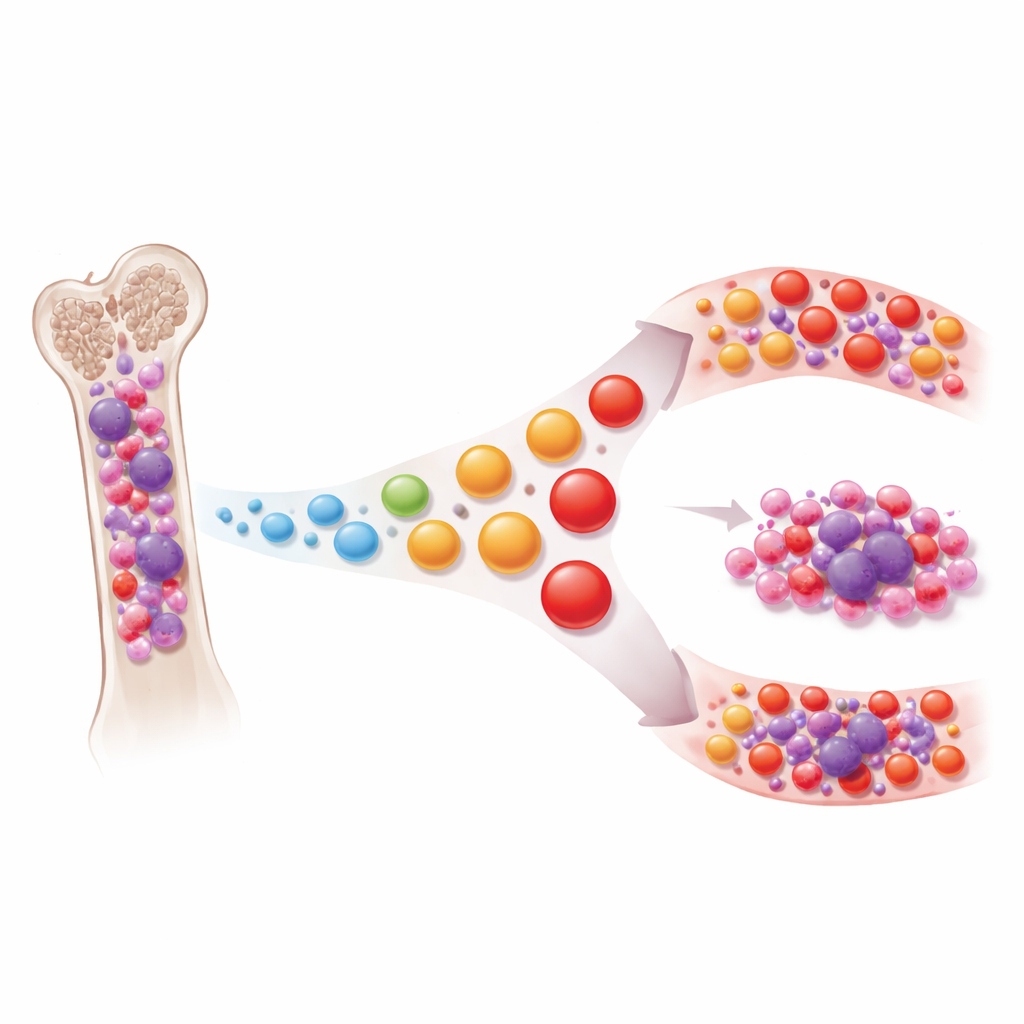
Nicht erschöpft, sondern vorzeitig gealtert
Entgegen dem, was bei vielen soliden Tumoren beobachtet wird, fanden die Forschenden, dass T‑Zellen beim Myelom selten wirklich erschöpft sind. Zellen mit klassischen Erschöpfungsmarkern beschränkten sich größtenteils auf einen einzelnen ungewöhnlichen Patienten. Stattdessen verschoben sich Knochenmark‑T‑Zellen bei smoldering und symptomatischem Myelom von naiven, frühen Stadien hin zu stark erfahrenen „terminalen Gedächtniszellen“, die T‑Zellen bei älteren Individuen ähneln. Dieses Muster — als T‑Zell‑Skewing bezeichnet — verlief parallel zur natürlichen Alterung des Immunsystems, erschien jedoch bei Patienten überzeichnet, als hätten ihre T‑Zellen schneller gealtert als der Rest ihres Körpers. Je weiter das Fortschreiten der Krankheit und je höher die Tumorlast, desto ausgeprägter war diese Verschiebung hin zu späten Gedächtniszellen; ähnliche Veränderungen zeigten sich teilweise auch im Blut.
Hinweise aus T‑Zell‑Fingerabdrücken
Jede T‑Zelle trägt einen einzigartigen Rezeptor; Zellen mit derselben Rezeptorsequenz gehören zu einem Klon, der als Reaktion auf einen Auslöser expandiert ist. Durch Verfolgen dieser Rezeptoren zeigten die Untersuchenden, dass Knochenmarkproben von Myelom viele expandierte T‑Zell‑Klone mit Merkmalen potenter Killerzellen enthalten. Diese Klone erkannten nicht überwiegend gängige Viren. Stattdessen wiesen sie ein ausgeprägtes „nicht‑virales“ Genmuster auf, das mit starker zytotoxischer Maschinerie verknüpft war und bei Menschen mit Myelom gegenüber den Prästadien angereichert war. Tumoren, die Proteinstücke besser auf ihrer Oberfläche präsentierten — durch höhere Aktivität von Antigenpräsentationsgenen — waren tendenziell mit diesen nicht‑viralen, hoch differenzierten T‑Zellen assoziiert. Patienten, deren Tumoren diese stärkere Immunbeteiligung zeigten, hatten im Allgemeinen bessere Überlebensraten, was nahelegt, dass diese T‑Zellen zumindest teilweise tatsächlich antitumoral wirken.
Behandlung, Rückfall und Frühwarnzeichen
Die Studie begleitete auch Patienten, die sich einer autologen Stammzelltransplantation unterzogen — einer häufigen intensiven Therapie. Nach der Transplantation wurde das T‑Zell‑Rezeptorrepertoire stärker von wenigen großen Klonen dominiert. Viele dieser expandierenden Klone ließen sich auf terminal differenzierte CD8‑T‑Zellen zurückverfolgen, die bereits vor der Behandlung vorhanden waren und dasselbe nicht‑virale, myelomassoziierte Profil trugen. Patienten mit noch vorhandenem Resttumor nach Transplantation wiesen tendenziell besonders klonale, verzerrte T‑Zell‑Repertoires auf, was darauf hindeutet, dass eine kräftige, aber alterungsähnliche T‑Zell‑Antwort die Krankheit möglicherweise nicht vollständig beseitigt. Betrachtet man frühere Krankheitsstadien, fanden die Autorinnen und Autoren, dass smoldering‑Patienten, die später in ein aktives Myelom übergingen, häufig einen Abfall regulatorischer CD4‑T‑Zellen zeigten — Zellen, die normalerweise helfen, Immunreaktionen und das Knochenmarkmilieu im Gleichgewicht zu halten. Niedrige Werte dieser Zellen sagten ein schnelleres Fortschreiten voraus, unabhängig von bestehenden klinischen Risikoskalen.
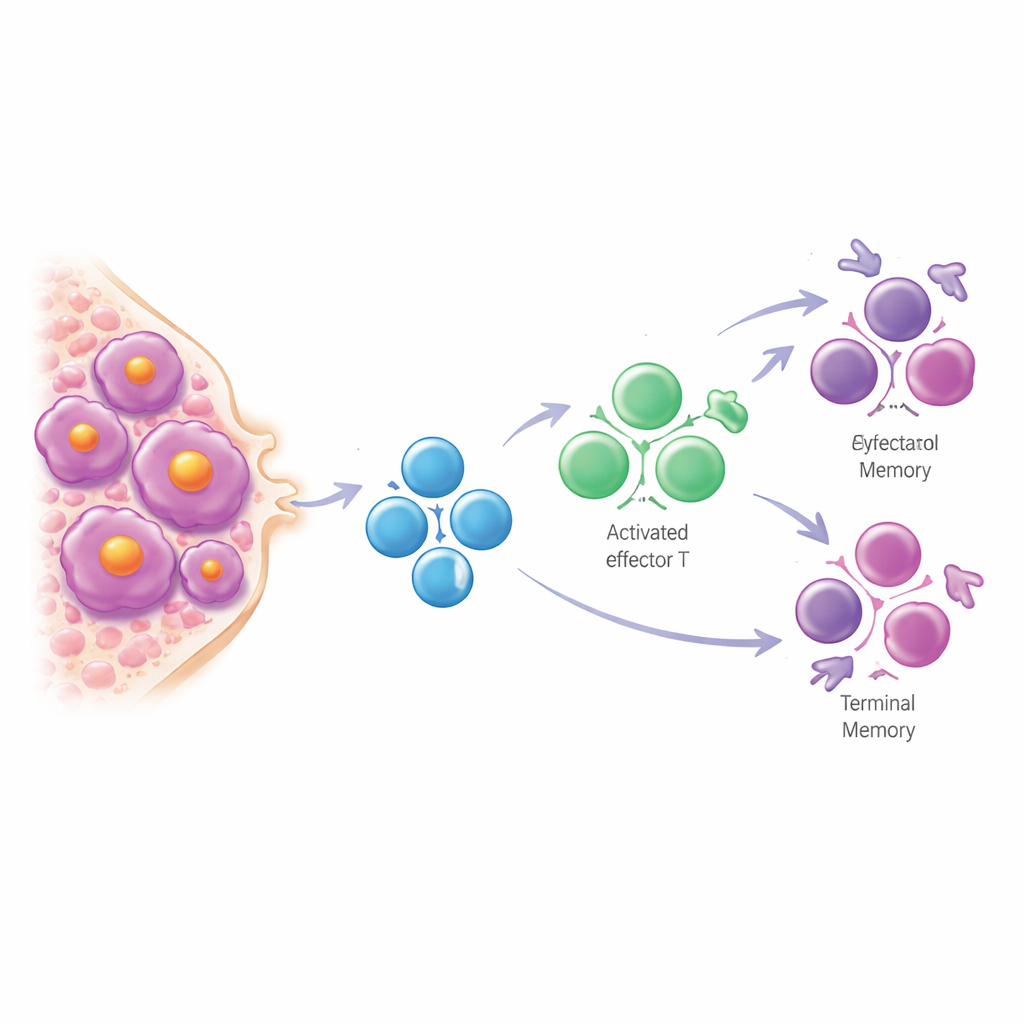
Was das für Patientinnen und Patienten bedeutet
Für Menschen mit Myelom und seinen Vorstufen rückt diese Arbeit die Reaktion des Immunsystems auf den Tumor neu ins Licht. Anstatt einfach zu erschöpfen, scheinen T‑Zellen beim Myelom chronisch in einen späten, gealterten Zustand gedrängt zu werden durch anhaltende Auseinandersetzungen mit Tumorzellen. Diese verzerrte, klonale T‑Zell‑Landschaft spiegelt die Tumorlast wider, beeinflusst das Ansprechen auf Therapien wie Transplantation und T‑Zell‑gerichtete Medikamente und kann — im Fall des Verlusts regulatorischer T‑Zellen — sogar Personen mit höherem Risiko für das Fortschreiten von smoldering zu symptomatischem Myelom kennzeichnen. Langfristig könnten diese Erkenntnisse neue Immuntherapien leiten, die T‑Zellen erneuern oder umlenken, und Klinikern helfen, Immunmerkmale neben traditionellen Markern zu nutzen, um Überwachung und frühe Intervention präziser zu timen.
Zitation: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
Schlüsselwörter: multiples Myelom, T‑Zellen, Immunoseneszenz, Einzelzellsequenzierung, Krebsimmunologie