Clear Sky Science · de
Klickbasierte Bestimmung der Anreicherung von Molekülen in Escherichia coli
Warum kleine Wirkstoffe Probleme haben, gefährliche Bakterien zu erreichen
Die moderne Medizin ist auf Antibiotika angewiesen, doch einige der gefährlichsten Bakterien sind inzwischen durch robuste Außenhüllen abgeschirmt, die viele Wirkstoffe draußen halten. Gramnegative Bakterien wie Escherichia coli besitzen eine besonders effektive Außenmembranbarriere, die es schwer macht, Wirkstoffe zu entwerfen, die tatsächlich in die Zelle eindringen und ihre Ziele erreichen. Diese Arbeit stellt einen neuen Labortest vor, das CHAMP‑Assay, mit dem Forschende schnell messen können, wie gut Tausende verschiedener kleiner Moleküle diese Abwehr überwinden und sich in lebenden E. coli‑Zellen anreichern.
Eine neue Methode, um zu beobachten, wie Wirkstoffe in bakterielle Zellen gelangen
Die traditionelle Antibiotikaforschung stützte sich auf natürlich vorkommende Verbindungen und einfache Wachstumstests, um zu sehen, ob Bakterien überleben oder absterben. Diese Tests zeigen nicht, wie viel Wirkstoff tatsächlich in die Zelle gelangt ist oder wo er sich im Inneren verteilt hat. Die Autorinnen und Autoren entwickelten eine direkte, breit anwendbare Methode zur Verfolgung des Eintritts von Wirkstoffen in das bakterielle Cytosol — die flüssige Innenumgebung, in der viele Antibiotikaziele liegen. Ziel war es, über grobe Messgrößen wie die minimale Hemmkonzentration hinauszukommen, die Wirkstoffaufnahme, Zielbindung und nachgeschaltete biologische Effekte vermischen, und stattdessen eine saubere Messung der intrazellulären Anreicherung zu erhalten.
Bakterien als winzige chemische Aufzeichner nutzen
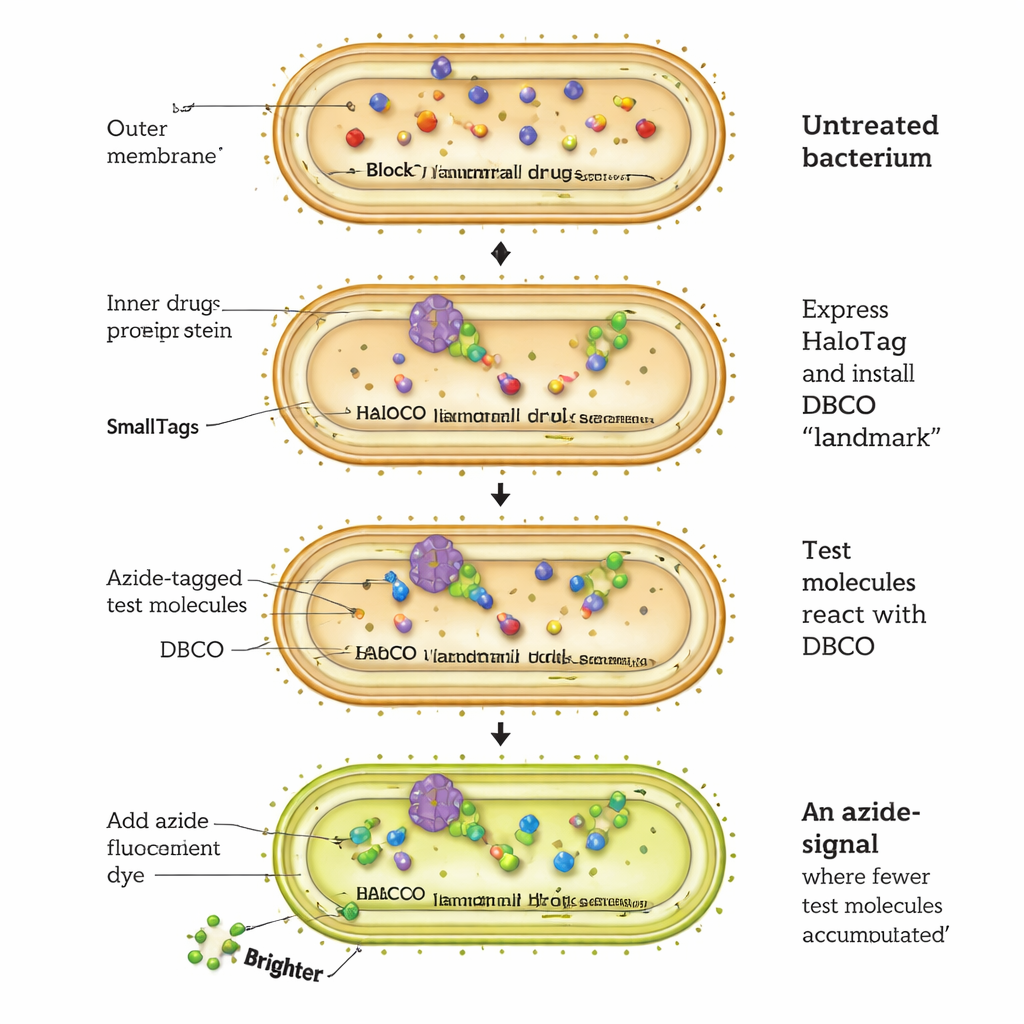
Das CHAMP‑Assay funktioniert, indem ein bakterielles Protein namens HaloTag zu einer Art molekularem Landeplatz umprogrammiert wird. E. coli‑Zellen werden so konstruiert, dass sie HaloTag im Cytosol produzieren. Zunächst bringen Forschende an HaloTag einen speziellen chemischen Griff an — ein „gespanntes“ Alkin namens DBCO — über einen kurzen Chloroalkane‑Linker. Anschließend setzen sie die Bakterien Testmolekülen aus, die jeweils ein sehr kleines Azid‑Tag tragen. Nur jene Testmoleküle, die die Außenmembran überwinden, die Innenmembran passieren und das Cytosol erreichen, können mit dem DBCO‑Griff in einer hochselektiven „Click“‑Reaktion reagieren und HaloTag dauerhaft markieren. Zum Schluss werden die Zellen mit einem azidmarkierten Fluoreszenzfarbstoff behandelt, der nur noch an verbleibendes unbesetztes DBCO bindet. Je heller die Fluoreszenz, desto weniger Testmoleküle sind ins Cytosol gelangt; dunklere Zellen zeigen eine bessere Anreicherung an.
Untersuchung, wie Chemie und Biologie den Wirkstoffeintritt formen
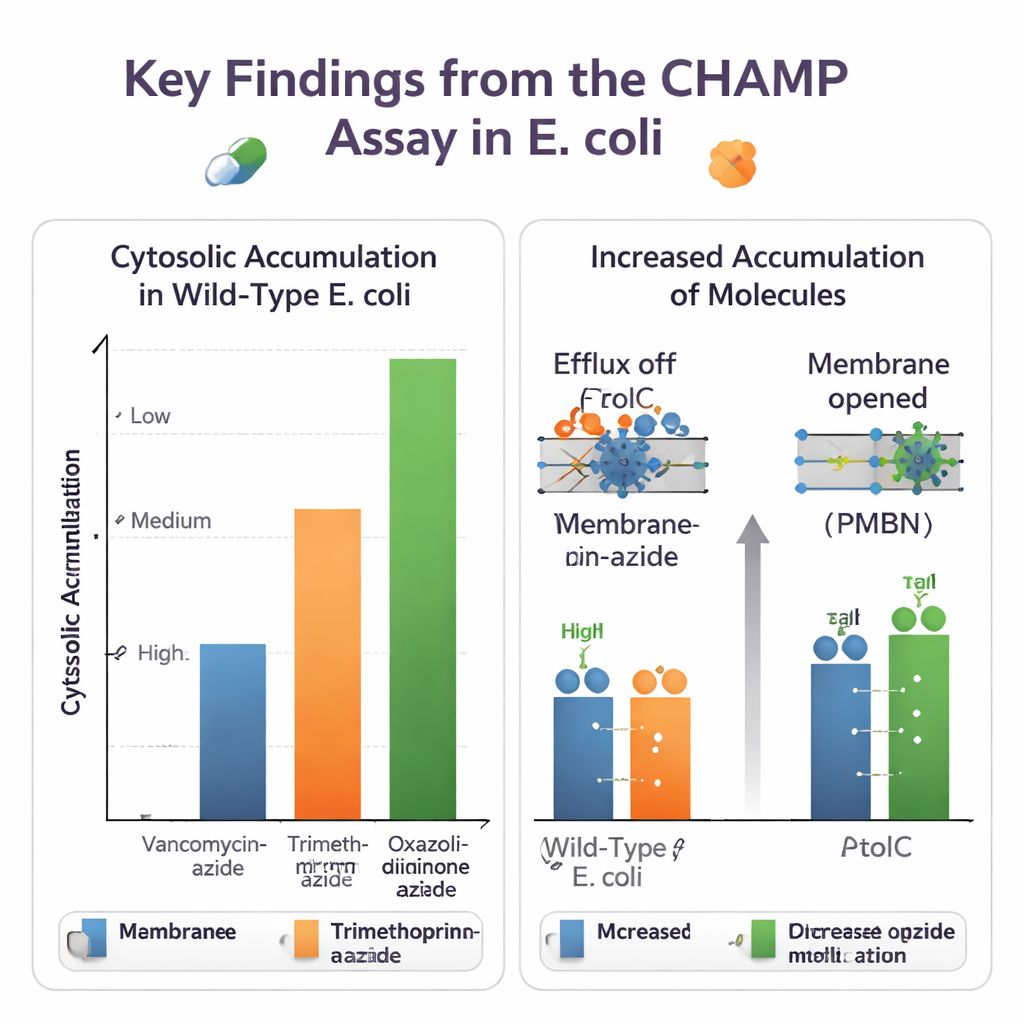
Mithilfe von CHAMP optimierte das Team zunächst die Expression von HaloTag, die Menge des DBCO‑Ankers und die Wahl der Fluoreszenzfarbstoffe, um ein großes und zuverlässiges Signalspektrum zu erzielen. Anschließend nutzten sie Sätze eng verwandter kleiner Moleküle, um zu sehen, wie chemische Modifikationen den Eintritt beeinflussen. Die Umwandlung von Carbonsäuren in Amide sowie das Hinzufügen oder Entfernen basischer Aminogruppen konnten die Cytosolspiegel deutlich verändern. In vielen Fällen verstärkten primäre Amine die Anreicherung, was unabhängige „eNTRy‑Regeln“ anderer Gruppen widerspiegelt. Das Assay funktionierte auch mit azidmarkierten Versionen realer Antibiotika und zeigte große Unterschiede: sperrige Wirkstoffe wie Vancomycin erreichten das Cytosol kaum, während kleinere Antibiotika wie Trimethoprim‑Derivate und einige Oxazolidinone deutlich leichter eindrangen.
Bakterielle Abwehrmechanismen entlarven, die Wirkstoffe wieder hinauspumpen
Da die Methode in lebenden, genetisch manipulierbaren Bakterien durchgeführt wird, kann sie die Rollen verschiedener zellulärer Abwehrmechanismen auseinanderhalten. Die Autorinnen und Autoren verglichen normales E. coli mit Stämmen ohne TolC, einem Schlüsselkomponenten einer wichtigen Multidrug‑Effluxpumpe, sowie mit Zellen, die mit einem kleinen TolC‑Hemmstoff behandelt wurden. Für Novobiocin und mehrere andere azidmarkierte Antibiotika zeigte CHAMP eindeutig höhere Cytosol‑Anreicherung, wenn TolC deaktiviert war, was diese Verbindungen als Substrate der Effluxpumpe bestätigt. Sie testeten auch Wege, die Außenmembranbarriere zu lockern, entweder chemisch mit dem Peptid PMBN oder genetisch durch Überexpression eines weit offenen Porinkanals. Viele Moleküle, die zuvor schlecht akkumulierten, zeigten große Zuwächse, wenn die Membran permeabilisiert war, was verdeutlicht, wie Eintritt und Efflux zusammen die internen Wirkstoffspiegel bestimmen.
Hochskalierung auf Tausende Moleküle für Muster und Regeln
Um echte Hochdurchsatzfähigkeit zu demonstrieren, screenten die Forschenden eine kommerzielle Sammlung von 404 azidmarkierten Verbindungen und eine maßgeschneiderte Bibliothek von 1.152 azidtragenden Molekülen. Sie maßen die Anreicherung in mehreren bakteriellen Kontexten, darunter unbehandelte Zellen, PMBN‑behandelte Zellen, hyperporinierte Zellen und hyperporinierte Zellen ohne TolC. Durch den Vergleich desselben Moleküls unter diesen Bedingungen konnten sie unterscheiden, welche Veränderungen auf Zellbiologie zurückzuführen waren und welche auf Besonderheiten der Click‑Reaktionsgeschwindigkeit. In Kombination mit computergestützten Analysen verbanden sie bestimmte physikochemische Merkmale — wie polare Oberfläche, Wasserstoffbindungsfähigkeit und spezifische Ringskelette — mit stärkerer Erkennung durch TolC‑basierte Effluxsysteme. Diese Art groß angelegter Profilierung beginnt, Gestaltungsprinzipien für Moleküle zu skizzieren, die entweder Pumpen entgehen oder Poren effektiver nutzen.
Was das für künftige Antibiotika bedeutet
Kurz gesagt verwandelt diese Arbeit E. coli in einen Hochdurchsatz‑Sensor, der genau berichtet, wie viel eines Testverbindungs in den Teil der Zelle gelangt, in dem viele Wirkstoffziele liegen. CHAMP ersetzt nicht Tests, ob Bakterien abgetötet werden, füllt jedoch eine entscheidende Lücke, indem es „Hineingelangen“ von „Wirkung“ trennt. Mit der Fähigkeit, innerhalb weniger Tage mehr als tausend Moleküle in verschiedenen Mutanten oder chemisch veränderten Stämmen zu messen, können Forschende systematisch lernen, welche chemischen Eigenschaften den Eintritt fördern, den Efflux verringern oder von membran‑störenden Partnern profitieren. Dieses Wissen sollte die Entwicklung neuer Antibiotika und Hilfsstoffe beschleunigen, die die schwer überwindbaren Abwehrmechanismen Gramnegativer Erreger durchbrechen, bevor der Resistenzverlust weiter Teile des Antibiotikaarsenals vereinnahmt.
Zitation: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Schlüsselwörter: Antibiotikaresistenz, Escherichia coli, Wirkstoffpermeabilität, Effluxpumpen, Click‑Chemie