Clear Sky Science · de
Der TREM2-Expressionsgrad ist entscheidend für den Zustand von Mikroglia, die metabolische Leistungsfähigkeit und die Wirksamkeit von TREM2-Agonisten
Warum Aufräumzellen im Gehirn bei Alzheimer wichtig sind
Die Alzheimer-Krankheit ist vor allem für klebrige Proteinansammlungen im Gehirn bekannt, doch genauso wichtig ist die Frage, wie die körpereigenen Immunzellen des Gehirns auf diese Schäden reagieren. Diese Zellen, Mikroglia genannt, funktionieren wie Hausmeister und Sanitäter: Sie räumen Trümmer weg, steuern Entzündungen und unterstützen das Überleben von Neuronen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage für künftige Therapien: Wie viel eines zentralen Mikroglia-Rezeptors, TREM2, ist „genau richtig“, um das Gehirn zu schützen — und wann könnten Medikamente, die TREM2 steigern, helfen oder schaden?
Ein Dimmer, kein Ein-/Ausschalter
Frühere genetische Studien zeigten, dass Menschen mit bestimmten Verlust-von-Funktion-Varianten im TREM2-Gen ein erhöhtes Risiko für spät beginnende Alzheimer-Krankheit haben. TREM2 wurde jedoch häufig als Ein-/Ausschalter betrachtet: entweder vorhanden oder fehlend. Die Autorinnen und Autoren bauten stattdessen eine spezielle «Reporter»-Maus, in der Mikroglia proportional zu ihrer TREM2-Produktion aufleuchten. Damit konnten sie Mikroglia in niedrige, mittlere und hohe TREM2-Gruppen sortieren und untersuchen, was jede Gruppe tut. Sie analysierten diese Zellen sowohl in gesunden Mäusen als auch in Mäusen, die Amyloid-Plaques entwickeln, ein Kennzeichen Alzheimer-ähnlicher Pathologie. 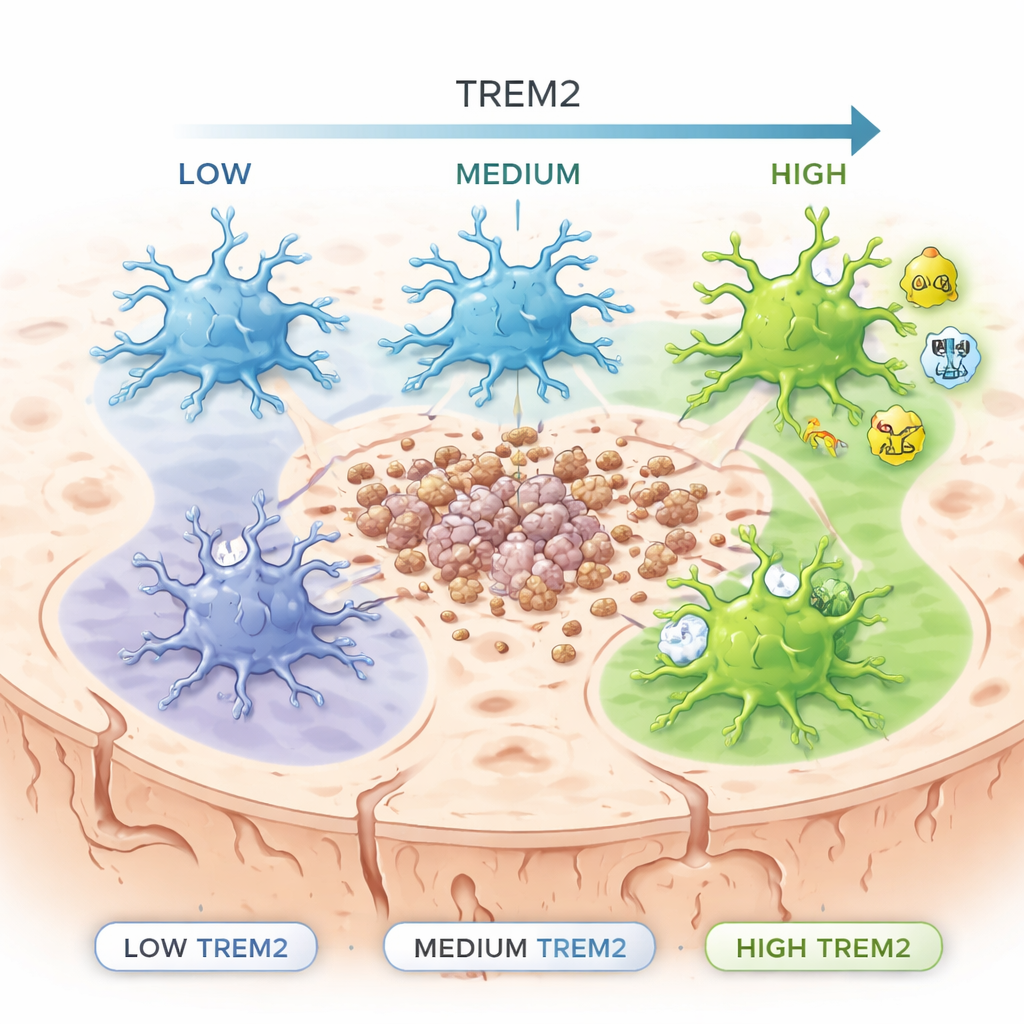
Energieverbrauch und Cholesterinmanagement verändern sich mit dem TREM2-Level
Sobald sie diese Mikroglia-Untergruppen trennen konnten, analysierten die Forschenden, welche Gene aktiviert waren, welche Metaboliten vorhanden waren und wie aktiv die Zellen Energie nutzten. Mikroglia mit mehr TREM2 zeigten stärkere Aktivität in Wegen, die mit oxidativer Phosphorylierung (dem wichtigsten energieerzeugenden System der Zelle) sowie mit Cholesterin- und Lipidstoffwechsel verbunden sind. Messungen der Aufnahme markierten Zuckers bestätigten, dass Zellen mit höherem TREM2 mehr Glukose aufnahmen, besonders in erkrankten Gehirnen. Detaillierte Metaboliten- und Lipidprofile ergaben, dass Mikroglia mit hohem TREM2 mehr Bausteine für zelluläre Energie und antioxidativen Schutz hatten und weniger freies Cholesterin sowie bestimmte Fettsäuremoleküle, was auf effizientere Treibstoffnutzung und bessere Cholesterinentsorgung hindeutet.
Von Metabolismus zur Aufräumleistung
Diese molekularen Signaturen übersetzten sich in echte funktionelle Unterschiede. In kontrollierten Labortests setzte das Team Mikroglia fluoreszent markierten Myelinfragmenten aus — ein Modell für die Arten von Trümmern, die Mikroglia in krankem Gehirngewebe beseitigen müssen. Mikroglia mit niedrigem TREM2 nahmen am wenigsten Material auf; solche mit mittlerem Niveau waren besser; und die Hoch-TREM2-Zellen waren am gefräßigsten. Dasselbe Muster zeigte sich in zwei verschiedenen Alzheimer-ähnlichen Mäusemodellen, was unterstreicht, dass der TREM2-Grad eng mit der „Aufräumkapazität“ der Zelle verknüpft ist. Gleichzeitig zeigten Gen-Netzwerkanalysen, dass höheres TREM2 nicht nur mit verbessertem Metabolismus, sondern auch mit bestimmten Immunantwortprogrammen assoziiert war, einschließlich Interferon-assoziierter Signale, die in einigen Kontexten nützlich und in anderen schädlich sein können. 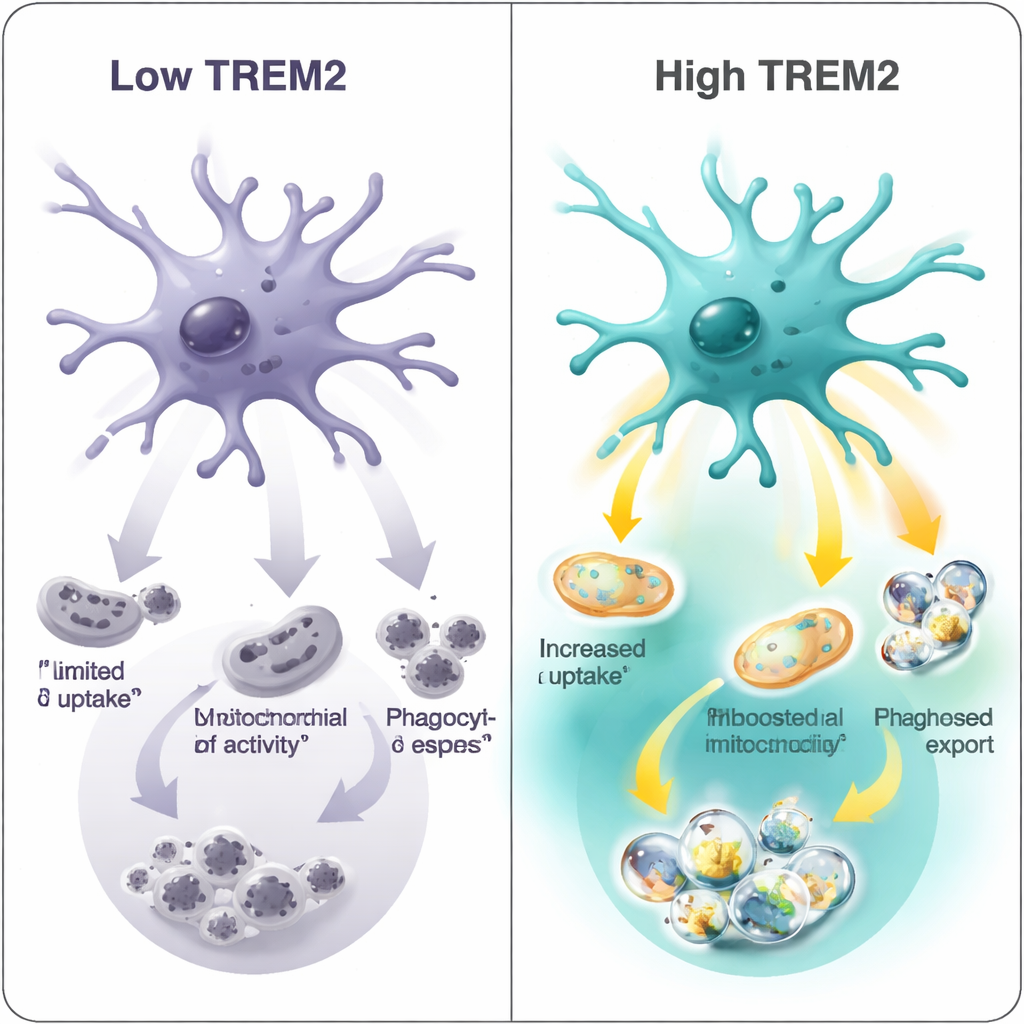
Wann das Anheben von TREM2 hilft — und wann es über das Ziel hinausschießen kann
Da Pharmafirmen Antikörper testen, die TREM2 aktivieren, fragten die Autorinnen und Autoren, wie ein solches Medikament Mikroglia mit unterschiedlichen Ausgangs-TREM2-Spiegeln beeinflusst. Sie behandelten Reporter-Mäuse mit Amyloid-Pathologie mit einem TREM2-aktivierenden Antikörper, der die Blut-Hirn-Schranke passieren kann, und sortierten die Mikroglia anschließend wieder nach TREM2-Expression. Auffällig war, dass die Zellen mit mittlerem TREM2 am stärksten reagierten: Ihre metabolischen Marker zeigten gesteigerte Glykolyse, verbesserte lysosomale und peroxisomale Aktivität und erhöhte Spiegel bestimmter schützender Membranlipide. Mikroglia mit niedrigem TREM2 veränderten sich kaum, vermutlich weil zu wenig Zielmolekül für das Medikament vorhanden war. Bei Mikroglia mit hohem TREM2 schien dieselbe Behandlung den Stoffwechsel jedoch wieder in Richtung eines moderateren Zustands zu verschieben, was auf einen „Deckeneffekt“ hindeutet, bei dem übermäßige Aktivierung gedämpft statt verstärkt wird.
Was das für künftige Alzheimer-Therapien bedeutet
Für nichtfachliche Leserinnen und Leser lautet die Kernbotschaft: Mikroglia mit der richtigen Menge TREM2 sind besser mit Energie versorgt, können Cholesterin besser handhaben und räumen schädliches Material um Amyloid-Plaques besser weg. Doch die Balance ist sensibel. Medikamente, die TREM2 stimulieren, werden wahrscheinlich am besten in einem bestimmten Fenster von Rezeptorlevels wirken — zu wenig TREM2 liefert nicht genug Ziel für Aktivierung; zu viel und das System könnte bereits nahe oder jenseits seines Optimums sein. Das hilft zu erklären, warum eine frühe klinische Studie mit einem TREM2-steigernden Antikörper scheiterte, und legt nahe, dass zukünftige Studien die TREM2-Aktivität und den Mikroglia-Zustand im Zeitverlauf messen sollten, vielleicht mithilfe von Hirnbildgebung, um die richtigen Patientinnen und Patienten und den richtigen Behandlungszeitpunkt zu wählen. Kurz gesagt, diese Arbeit stellt TREM2 als fein einstellbaren „Dimmer“ für Mikroglia-Metabolismus und Aufräumleistung dar, statt als einfachen Ein-/Ausschalter, und bietet eine Roadmap für klügere, gezieltere Immuntherapien bei Alzheimer-Krankheit.
Zitation: Feiten, A.F., Dahm, K., Schlepckow, K. et al. TREM2 expression level is critical for microglial state, metabolic capacity and efficacy of TREM2 agonism. Nat Commun 17, 2002 (2026). https://doi.org/10.1038/s41467-026-68706-8
Schlüsselwörter: Mikroglia, TREM2, Alzheimer-Krankheit, Gehirnstoffwechsel, Immuntherapie