Clear Sky Science · de
Krebs‑Kachexie bei STK11/LKB1‑mutiertem nicht‑kleinzelligem Lungenkrebs hängt vom tumorsekretierten GDF15 ab
Warum manche Lungenkrebserkrankungen gefährlichen Gewichtsverlust auslösen
Krebs wächst nicht immer still an einer Stelle. Bei vielen Menschen raubt er dem Körper im Laufe der Zeit Fett, Muskeln, Kraft und Energie in einer als Kachexie oder Auszehrung bezeichneten Erkrankung. Diese Studie stellt eine drängende Frage für Patienten mit einer häufigen Form von Lungenkrebs: Warum lösen einige Tumoren diesen schweren Gewichtsverlust aus, andere dagegen nicht? Die Forscher führen das Problem auf ein von bestimmten Tumoren erzeugtes Stresssignal zurück und zeigen, dass das Blockieren dieses Signals bei Tieren den Gewichtsverlust weitgehend stoppen oder sogar umkehren kann.
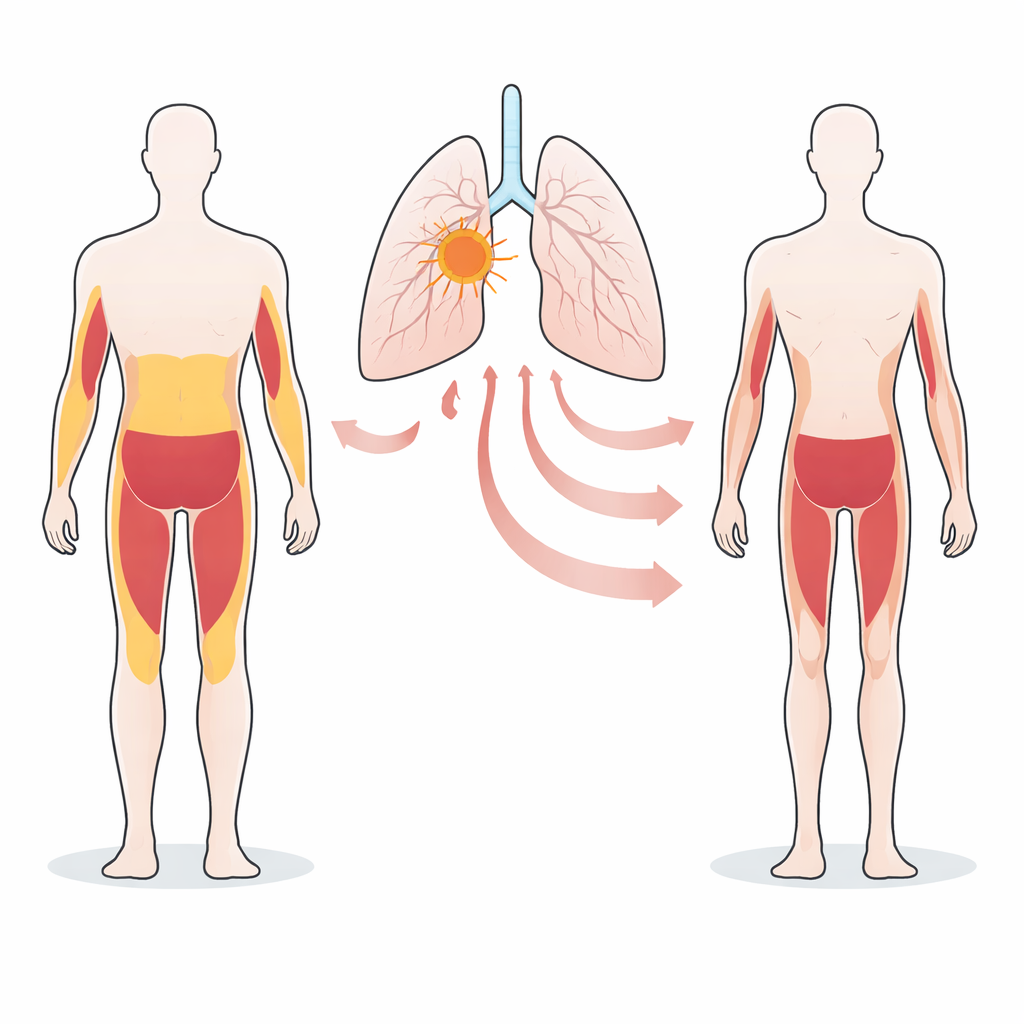
Eine verborgene Verbindung zwischen Tumorgenen und Körperauszehrung
Das Team konzentrierte sich auf nicht‑kleinzellige Lungenkarzinome mit fehlerhaften Versionen eines Gens namens STK11/LKB1. Frühere Arbeiten zeigten, dass Tumoren mit diesem Defekt häufig mit massivem Gewichts‑, Fett‑ und Muskelverlust bei Mäusen und Patienten einhergehen. Hier verglichen die Wissenschaftler zahlreiche menschliche Lungen-Tumorzelllinien, die beim Wachstum in Mäusen entweder Kachexie auslösten oder nicht. Sie fanden heraus, dass kachektische Tumoren mit STK11/LKB1‑Defekten deutlich höhere Mengen eines stresshormonähnlichen Proteins namens GDF15 produzierten und dass dieses Protein ins Blut gelangte. Im Gegensatz dazu trugen Zellen des Wirts nur wenig zu dem im Blut gemessenen GDF15 bei, was den Tumor selbst als Hauptquelle ausweist.
Nachweis, dass das Tumorsignal Gewicht, Fett- und Muskelverlust antreibt
Um zu prüfen, ob tumorproduziertes GDF15 tatsächlich die Auszehrung verursacht, nutzten die Forscher genetische Werkzeuge, um GDF15 ausschließlich in den Krebszellen auszuschalten, ohne andere Gene zu verändern. In mehreren verschiedenen STK11/LKB1‑mutierten Lungenkrebszelllinien führte das Abschalten von GDF15 nicht zu verlangsamtem Tumorwachstum, schützte die Mäuse jedoch massiv vor Verlust von Körpergewicht, Fettmasse, Muskelmasse und Griffkraft. Dieser Schutz zeigte sich bei beiden Geschlechtern und in Modellen, bei denen Tumoren unter die Haut oder direkt in die Lunge eingesetzt wurden, was darauf hindeutet, dass der Effekt von ins Blut freigesetzten Faktoren ausgeht und nicht vom Tumorort abhängt. Selbst wenn Tumoren nur moderate Mengen an GDF15 produzierten, schwächte das Ausschalten dieses Signals die Auszehrung ab, was zeigt, dass bereits relativ niedrige Spiegel biologisch relevant sein können.
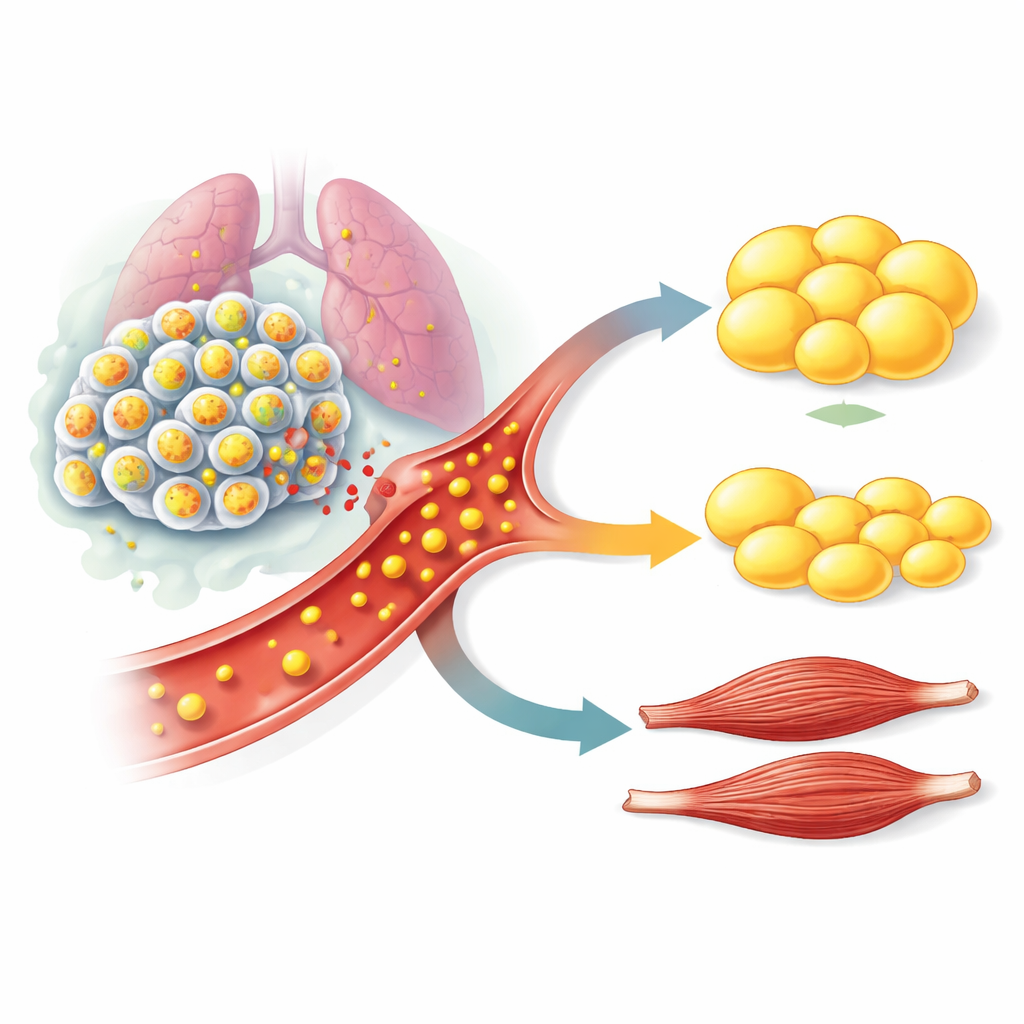
Antikörper, die das Signal blockieren, zeigen therapeutisches Potenzial
Da Pharmafirmen bereits Antikörper entwickeln, die GDF15 neutralisieren, prüfte das Team, ob ein solcher Ansatz in ihren Modellen hilfreich sein könnte. Sie behandelten Mäuse mit STK11/LKB1‑mutierten Tumoren mit einem GDF15‑blockierenden Antikörper, ähnlich demjenigen, das derzeit in klinischen Studien erprobt wird. Bei früher Gabe verhinderte der Antikörper den üblichen Verlust von Fett, Muskelmasse und Kraft, ohne die Tumorwachstumsrate zu verändern. Bei späterer Gabe — nachdem die Tiere bereits einen großen Teil ihres Fetts verloren hatten — konnte derselbe Antikörper weiteren Abbau stoppen und Körperreserven sowie Muskelmasse teilweise wiederherstellen. Ähnliche Ergebnisse zeigten sich in einem Mausmodell für Lungenkrebs mit intaktem Immunsystem, was darauf hinweist, dass die Befunde nicht auf immunsupprimierte Tiere beschränkt sind.
Wie ein gestresster Tumor den Auszehr‑Schalter umlegt
Die Studie untersucht außerdem, warum STK11/LKB1‑mutierte Tumoren so viel GDF15 produzieren. Zellen nutzen ein internes Alarmsystem, die Stressantwort, um mit Nährstoffmangel und anderen Bedrohungen fertigzuwerden. In Tumoren ohne funktionierendes STK11/LKB1 ist dieser Alarm chronisch aktiv und erhöht die Produktion sowie die Verarbeitung von GDF15 zu seiner reifen, sekretierbaren Form. Wenn die Forscher ein funktionierendes STK11/LKB1‑Gen in eine humane Lungenkrebszelllinie zurückführten, ebbte die Stressantwort ab. Die GDF15‑Spiegel im Tumor und im Blut sanken deutlich, die Nahrungsaufnahme verbesserte sich, und die Tiere entwickelten keine Kachexie mehr, obwohl die Tumoren weiterhin vorhanden waren.
Was das für Patienten mit Lungenkrebs bedeutet
Für Menschen mit nicht‑kleinzelligem Lungenkrebs und STK11/LKB1‑Mutationen legt diese Arbeit nahe, dass der Tumor selbst wie ein endokrines Organ wirken kann, indem er GDF15 ins Blut freisetzt und so eine systemische Auszehrung antreibt. In Mäusen reduzierte das Blockieren von GDF15 — entweder durch Entfernung aus dem Tumor oder durch einen zirkulierenden Antikörper — Fett‑ und Muskelverlust deutlich, ohne den Tumor direkt zu verkleinern. Das eröffnet die Möglichkeit, dass bei den etwa 15 Prozent der Lungenkrebspatienten mit STK11/LKB1‑Defekten Anti‑GDF15‑Therapien helfen könnten, Kraft und Körpergewicht über ein breites Spektrum an Blut‑GDF15‑Spiegeln zu erhalten. Anders ausgedrückt: Das Abschwächen dieses einzelnen tumorproduzierten Signals könnte eines Tages eine praktikable Möglichkeit bieten, eine der belastendsten Komplikationen des Krebses zu lindern.
Zitation: Yu, J., Guo, T., Gupta, A. et al. Cancer cachexia in STK11/LKB1-mutated non-small cell lung cancer is dependent on tumor-secreted GDF15. Nat Commun 17, 2182 (2026). https://doi.org/10.1038/s41467-026-68702-y
Schlüsselwörter: Krebs‑Kachexie, nicht‑kleinzelliger Lungenkrebs, GDF15, STK11 LKB1 Mutation, Muskel‑ und Fettverlust