Clear Sky Science · de
Meta-verstärkte Dunkelfeld-interferometrische Streumikroskopie
Die kleinsten Bausteine des Lebens sichtbar machen
Viele der wichtigsten Akteure in der Biologie — etwa Proteine, Viren und winzige Membranbläschen, sogenannte Exosomen — sind deutlich kleiner als die Wellenlänge des sichtbaren Lichts. Diese nanoskaligen Akteure in Aktion zu beobachten, ohne fluoreszenzmarkierende Tags anzubringen, die sie beeinflussen könnten, ist ein lang gehegtes Ziel. Diese Arbeit stellt eine neue Art von Mikroskop vor, das diese nahezu unsichtbaren Partikel vor einem nahezu perfekt dunklen Hintergrund deutlich hervorhebt und so den Weg zu schonenderen, schnelleren und empfindlicheren Messungen in Biologie und Medizin öffnet.
Warum winzige Partikel so schwer zu erkennen sind
Gewöhnliche Lichtmikroskope haben bei nanoskaligen Objekten Schwierigkeiten, weil so kleine Partikel nur eine verschwindend geringe Menge Licht streuen — die Streustärke fällt stark ab, wenn der Partikel kleiner wird. Die interferometrische Streumikroskopie (iSCAT) löst dieses Problem teilweise, indem sie die Interferenz zwischen dem schwachen Signal des Partikels und einem stärkeren, ebenen Referenzstrahl aufzeichnet, der von einer Fläche reflektiert wird. Das erhöht die Empfindlichkeit genug, um einzelne Proteine und Viren sichtbar zu machen. Es gibt jedoch einen Kompromiss: Wenn man den Referenzstrahl abdunkelt, um den Kontrast zu verbessern, reduziert man gleichzeitig die Gesamtzahl der Photonen, sodass das Bild verrauschter wird. iSCAT weiter voranzutreiben, um zuverlässig noch kleinere Partikel zu detektieren, ist daher zunehmend schwierig geworden.
Eine ebene Fläche in eine aktive Lichtantenne verwandeln
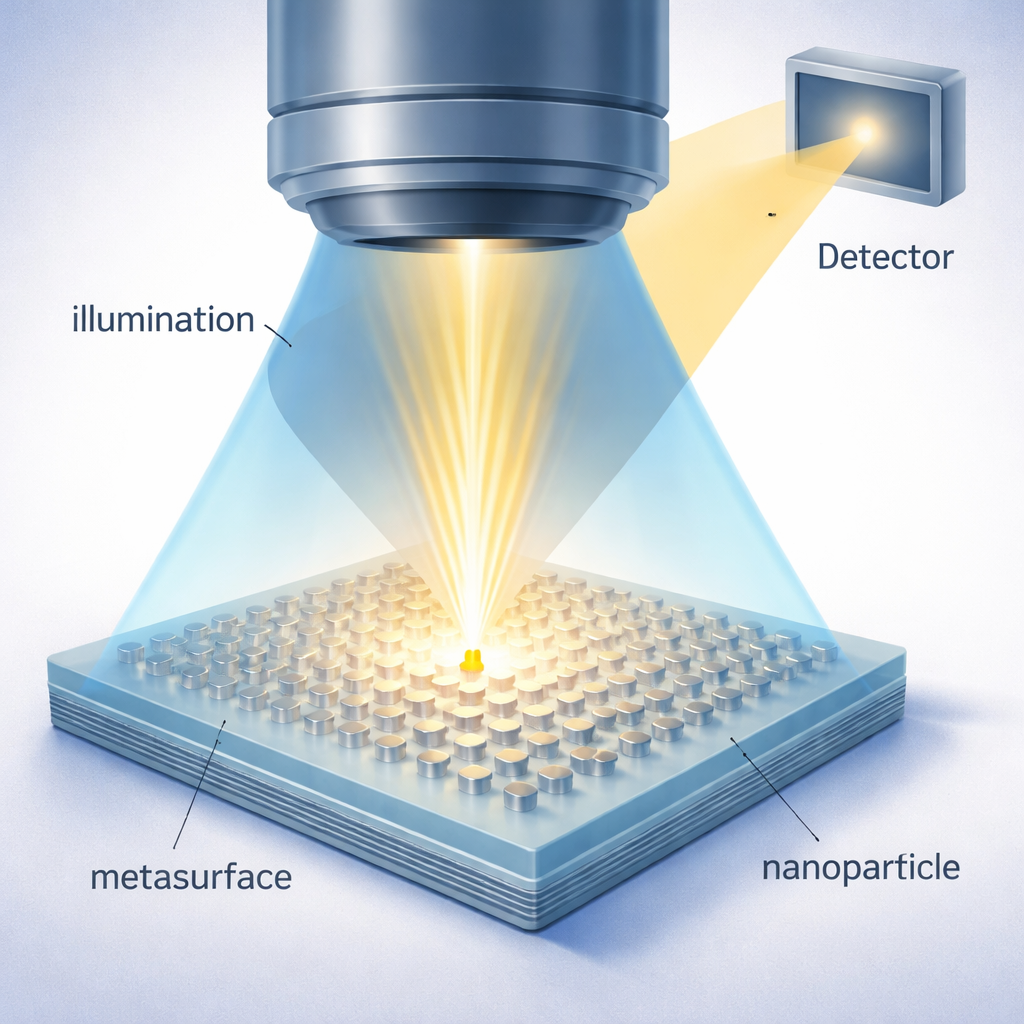
Die Autoren gehen dieses Problem an, indem sie die übliche Glasplatte durch eine sorgfältig konstruierte „Metafläche“ aus dicht angeordneten, hexagonal gereihten Silber-Nanosäulen ersetzen, die jeweils nur einige Dutzend Nanometer groß sind. Diese winzigen Metallstrukturen verhalten sich kollektiv wie ein Antennenarray für Licht. Im normalen Zustand sind sie so ausgelegt, dass sie einander bei der Streuung in den Aufnahmewinkel des Mikroskops weitgehend auslöschen und so einen sehr dunklen Hintergrund erzeugen — dies wird als Dunkelmodus bezeichnet. Wenn sich jedoch ein Nanopartikel der Metafläche nähert, stört es das lokale elektromagnetische Gleichgewicht. Diese Störung verschiebt die Phasen und Amplituden der Schwingungen der Nanosäulen, sodass sie nun stark in Richtung Detektor abstrahlen und lokal in einen hellen Modus umschalten, der sich um den Partikel zentriert.

Signale von Nanopartikeln und Biomolekülen verstärken
Diese neue Technik, meta‑verstärkte Dunkelfeld‑interferometrische Streumikroskopie (MAD‑iSCAT) genannt, nutzt die Metafläche effektiv als aktiven Verstärker für die Anwesenheit des Partikels. Anstatt sich hauptsächlich auf die schwache Streuung des Partikels zu stützen, misst MAD‑iSCAT, wie der Partikel die deutlich stärkeren Lichtwellen der Metafläche umformt. Da diese Wellen intensiv sind und sehr empfindlich auf winzige Umweltänderungen reagieren, können bereits sehr kleine Partikel eine detektierbare helle Stelle im Bild auslösen. Simulationen und Experimente zeigen, dass das Signal mit der Partikelgröße viel sanfter wächst als bei konventioneller „Rayleigh“-Streuung, sodass die Methode auch bei sehr kleinen Durchmessern wirksam bleibt, an denen traditionelle Ansätze versagen würden.
Das neue Mikroskop in der Praxis testen
Um zu zeigen, dass MAD‑iSCAT praktisch funktioniert, fertigten die Forscher ihre Silber‑Metaflächen mittels Nanoimprint‑Techniken und beschichteten sie mit einer dünnen schützenden Polymerschicht. Anschließend bildeten sie Polystyrolkugeln mit Durchmessern zwischen 45 und 200 Nanometern ab und verglichen die Helligkeit mit denselben Partikeln auf einer einfachen Polymerfolie. Die Metafläche steigerte die scheinbare Streuintensität je nach Größe und Lichtfarbe um mehr als ein bis zwei Größenordnungen. In wässrigen Umgebungen, in denen viele biologische Proben leben, verglich das Team MAD‑iSCAT direkt mit einem hochmodernen iSCAT‑Aufbau. Für Partikel von nur wenigen Dutzend Nanometern lieferte MAD‑iSCAT um den Faktor zehn bis mehrere zehn höhere Bildkontraste — und das mit nur zwei Aufnahmen statt hunderter, was auf eine deutlich höhere Durchsatzrate hinweist.
Echte biologische Nanopartikel beobachten
Über die Kunststoff-Testkügelchen hinaus zeigten die Autoren, dass MAD‑iSCAT einzelne Exosomen, die von Brustkrebszellen freigesetzt wurden, und sogar einzelne Ferritin‑Proteinkomplexe sichtbar machen kann. Durch Verfolgen der Bewegung von Exosomen in Lösung schätzten sie deren Größen und stellten fest, dass MAD‑iSCAT Signalstärken lieferte, die 10‑ bis 100‑mal stärker waren als bei einfacher Streuung zu erwarten. Für Ferritin, einen großen Proteinkomplex von etwa 440 Kilodalton, beobachteten sie klare Punkte mit deutlich verbessertem Signal‑Rausch‑Verhältnis im Vergleich zu standardmäßigen interferometrischen Ansätzen. Diese Ergebnisse zeigen, dass die neue Methode bis hinunter zur Skala einzelner Biomoleküle reicht und dabei weiterhin in realistischen Flüssigumgebungen funktioniert.
Was das für künftige Biosensorik bedeutet
Alltäglich ausgedrückt verwandelt MAD‑iSCAT eine ansonsten gewöhnliche Objektträgerfläche in eine intelligente Oberfläche, die nur dann aufleuchtet, wenn ein nanoskaliges Objekt sie berührt. Durch die Kombination eines nahezu schwarzen Hintergrunds mit stark verstärkten Signalen um jedes Partikel herum macht die Technik das Erkennen und Vermessen winziger biologischer Strukturen ohne Marker erheblich einfacher. Zwar stehen die aktuellen Geräte noch vor Herausforderungen in Bezug auf Fertigungsgenauigkeit und Sichtfeld, doch das Konzept verspricht schnellere, empfindlichere Werkzeuge zum Wiegen einzelner Moleküle, zur Überwachung krankheitsrelevanter Vesikel wie Exosomen und möglicherweise zur Erweiterung labelfreier optischer Bildgebung in den Bereich der Superauflösung.
Zitation: Lee, H., Zhao, J., Hu, P. et al. Meta-amplified dark-field interferometric scattering microscopy. Nat Commun 17, 1977 (2026). https://doi.org/10.1038/s41467-026-68697-6
Schlüsselwörter: labelfreie Mikroskopie, Nanopartikelerkennung, plasmonische Metaflächen, Biosensorik, interferometrische Streuung