Clear Sky Science · de
Hochgeschwindigkeits‑Blind‑Structured‑Illumination‑Mikroskopie mittels unüberwachtem Algorithmus‑Unrolling
Scharfere Filme des Lebens in Zellen
Die moderne Biologie hängt oft davon ab, lebende Zellen in Aktion zu beobachten, doch viele zentrale Strukturen sind schlicht zu klein und zu schnell, als dass herkömmliche Mikroskope sie klar erfassen könnten. Diese Arbeit stellt eine neue Methode vor, mit der verwischte, schnell aufgenommene Bilder in Echtzeit in gestochen scharfe, superaufgelöste Filme verwandelt werden können — ohne perfekt abgestimmte Hardware. Die Methode, unrolled blind structured illumination microscopy (UBSIM) genannt, verspricht, fortgeschrittene, hochfrequente Zellbildgebung für normale Labore zugänglicher zu machen.
Warum normale Mikroskope nicht ausreichen
Traditionelle Lichtmikroskope sind durch Beugung begrenzt, eine grundlegende Eigenschaft des Lichts, die feine Details unterhalb einiger hundert Nanometer verwischt. Structured Illumination Microscopy (SIM) begegnet diesem Problem, indem es gemustertes Licht auf eine Probe projiziert und die entstehenden Interferenzmuster nutzt, um zusätzliche Details zu extrahieren und die Auflösung etwa zu verdoppeln. Klassisches SIM erfordert jedoch genau bekannte Beleuchtungsmuster und sorgfältige Kalibrierung, was teuer und empfindlich sein kann. Eine neuere Variante, blind‑SIM, lockert diese Hardware‑Anforderungen, indem sie zufällige Muster zulässt und sowohl Probe als auch Beleuchtung aus den Messdaten rekonstruiert. Der Nachteil ist, dass dieser Lösungsprozess langsam und iterativ ist und Sekunden bis Minuten pro Bild braucht — viel zu langsam für Echtzeit‑Filme lebender Zellen.
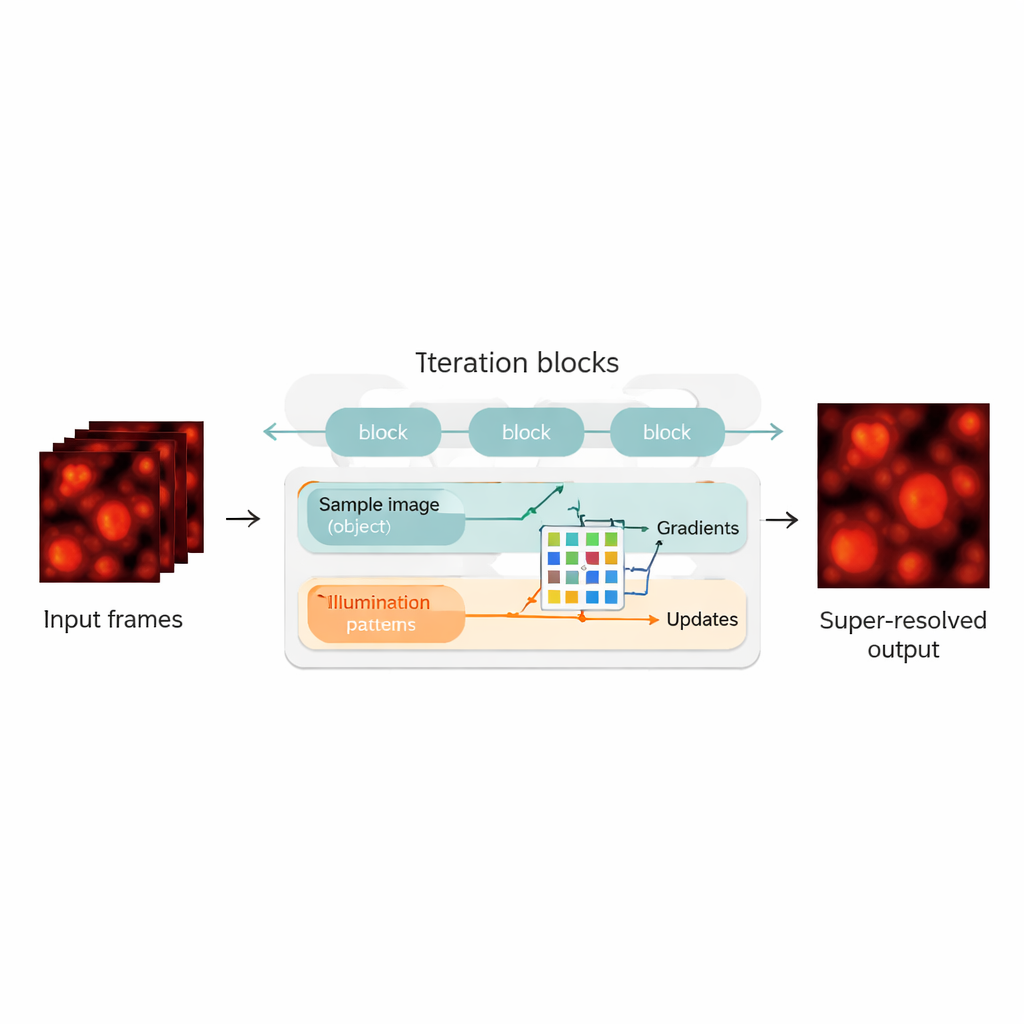
Physik mit neuronalen Netzen verbinden
Die Autoren überbrücken diese Lücke, indem sie die blind‑SIM‑Rekonstruktion als Hybrid aus physikbasiertem Modell und neuronaler Architektur neu gestalten. Sie „rollen“ den ursprünglichen iterativen Algorithmus aus — jede Iteration wird zu einer Schicht in einem neuronalen Netzwerk und bildet eine Kette von Aktualisierungsblöcken. Innerhalb jedes Blocks berechnet die Methode, wie gut die aktuelle Schätzung von Probe und Beleuchtung die gemessenen Bilder erklärt, ermittelt Gradienten (Verbesserungsrichtungen) und führt diese in ein kompaktes Faltungsnetz (CNN) ein. Dieses Netzwerk lernt, klügere Korrekturschritte vorzunehmen und wirkt wie ein automatisch abgestimmter Beschleuniger für den ursprünglichen Algorithmus. Wichtig ist, dass UBSIM unüberwacht trainiert wird: Anstatt perfekte Beispielbilder als Ground‑Truth zu benötigen, braucht es nur das physikalische Modell, wie Licht durch das Mikroskop läuft. Das verringert das Risiko, dass das Netzwerk plausibel aussehende, aber falsche Strukturen „halluziniert“.
Schnell, genau und weniger anfällig für Fehlschlüsse
Um UBSIM zu testen, verwendete das Team zunächst simulierte Mikroskopiebilder, bei denen die tatsächlichen zugrundeliegenden Strukturen bekannt sind. Sie zeigten, dass UBSIM etwa die doppelte Auflösung gegenüber gewöhnlichen Weitfeldbildern wiederherstellt, vergleichbar mit standardmäßigem blind‑SIM, aber zwei bis drei Größenordnungen schneller läuft — ein 256×256‑Bild kann in etwa 10 Millisekunden statt in Sekunden rekonstruiert werden. Qualitätsmaße der Bilder, darunter Fehler, Ähnlichkeit und Signal‑Rausch‑Verhältnisse, verbesserten sich deutlich gegenüber konventionellen Bildern. UBSIM erwies sich zudem als vertrauenswürdiger als gängige Deep‑Learning‑Superauflösungsnetzwerke, wenn es mit unbekannten Daten konfrontiert wurde. Während Standardnetzwerke, die auf einem bestimmten Strukturtyp trainiert sind, dazu neigen, dieses Muster auf andere Proben zu übertragen und so subtile, irreführende Artefakte einzuführen, behielt UBSIM eine konsistente Treue bei, weil es an die zugrunde liegende Bildgebungsphysik gebunden ist und nicht nur an visuelle Beispiele.
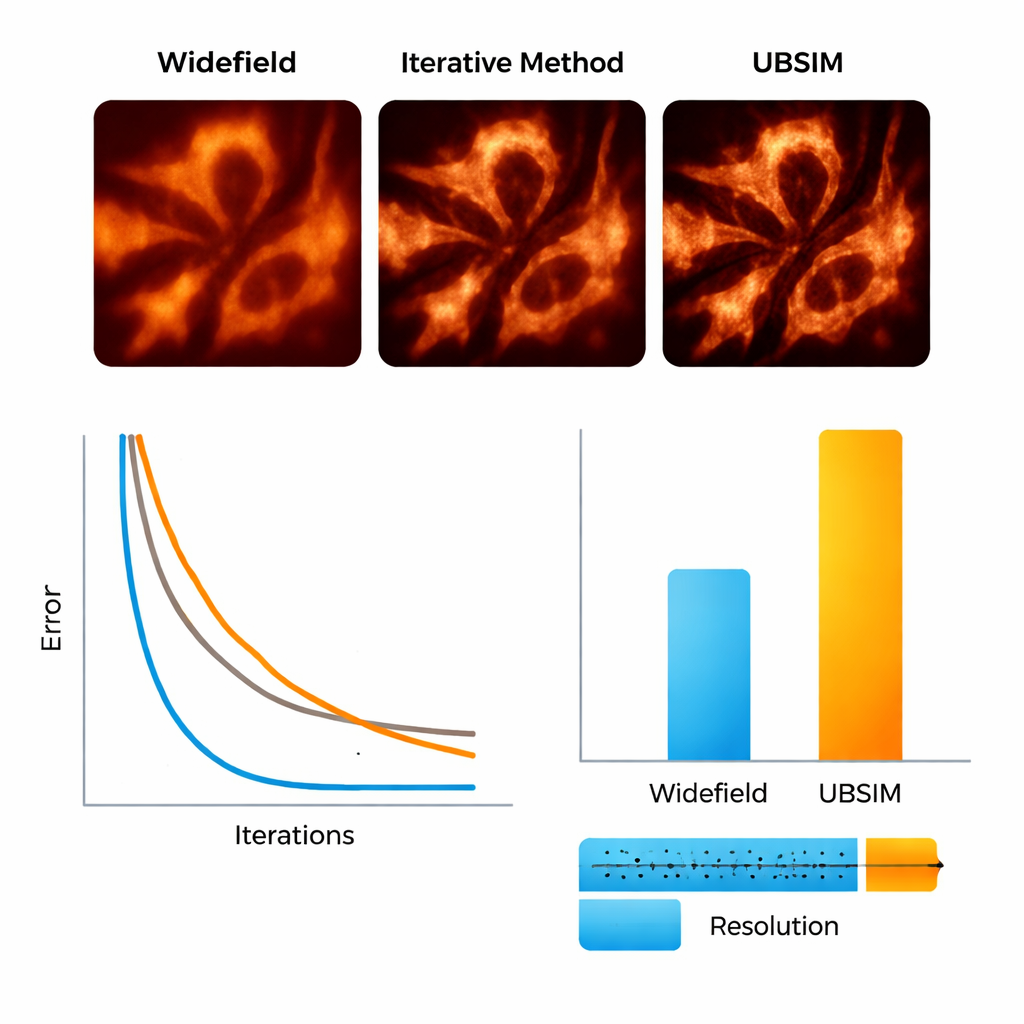
Zellgerüste und Membranen in Bewegung sehen
Die Forscher gingen dann zu echten biologischen Proben über. Mit einer flexiblen Aufstellung, die zufällige Streumuster auf lebende Zellen projiziert, bildeten sie Aktinfilamente — das proteinhaltige „Gerüst“ innerhalb von Zellen — sowie das endoplasmatische Retikulum (ER) ab, ein verästeltes Membrannetzwerk, das an Proteinproduktion und Stressreaktionen beteiligt ist. Mit UBSIM, das aus verschwommenen Bändern scharf getrennte Stränge machte, verbesserte sich die Auflösung der Aktinfasern von etwa 300 Nanometern auf rund 150 Nanometer. Besonders eindrucksvoll ermöglichte UBSIM Superauflösung in Videogeschwindigkeit: Durch Rohdatenaufnahmen mit bis zu 100 Bildern pro Sekunde und Rekonstruktionen mit bis zu 50 superaufgelösten Bildern pro Sekunde konnte das Team ER‑Tubuli beim Wachsen, Kollabieren und Umorganisieren in Echtzeit beobachten. Diese Dynamiken, die in Bruchteilen einer Sekunde bis zu wenigen Sekunden stattfinden, sind normalerweise schwer mit ausreichendem Detail zu visualisieren.
Was das für die zukünftige Zellbildgebung bedeutet
Für Nicht‑Spezialisten ist die zentrale Botschaft, dass UBSIM es deutlich praktischer macht, winzige zelluläre Strukturen in Echtzeit zu verfolgen — mit Klarheit über die üblichen Grenzen von Lichtmikroskopen hinaus — und das ohne perfekte Hardwarekalibrierung oder riesige Trainingsdatensätze. Indem die Zuverlässigkeit physikbasierter Modelle mit der Geschwindigkeit moderner neuronaler Netze kombiniert wird, verwandelt dieser Ansatz Stapel verrauschter, gemusterter Bilder schnell in vertrauenswürdige, extrem scharfe Filme, die für Routineexperimente ausreichen. Mit weiteren Verfeinerungen und besseren Beleuchtungsstrategien könnte die Methode Forschern helfen zu untersuchen, wie Organellen wie das ER auf Stress reagieren, wie sich das zelluläre Gerüst bei Bewegung oder Teilung umorganisiert und wie Krankheiten die zelluläre Architektur auf Nanoskala verändern.
Zitation: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
Schlüsselwörter: Superauflösungsmikroskopie, strukturierte Beleuchtung, Deep Learning, Lebendzell‑Bildgebung, Dynamik des endoplasmatischen Retikulums