Clear Sky Science · de
Geografische Ausbreitung von antimikrobieller Resistenz nach Massenverabreichung von Azithromycin
Warum das für die Gesundheit von Kindern wichtig ist
Azithromycin, ein häufig eingesetztes Antibiotikum, wurde in Massendurchführungen eingesetzt, um das Leben kleiner Kinder in Teilen Subsahara‑Afrikas, darunter Niger, zu retten. Diese Kampagnen haben Kindersterblichkeit reduziert, werfen aber eine ernste Frage auf: Könnten sie gleichzeitig dazu beitragen, dass medikamentenresistente Bakterien von behandelten Dörfern in benachbarte Gemeinden gelangen, die das Medikament nie erhalten? Diese Studie untersucht, ob ein solcher "Spillover" von Resistenz zwischen Dörfern stattfindet — eine zentrale Frage für Länder, die Nutzen und Risiken einer Ausweitung dieser Programme abwägen.
Leben rettende Kampagnen und ihr verstecktes Risiko
Frühere große Studien zeigten, dass die zweimal jährliche Verabreichung von Azithromycin an alle Kleinkinder in Gebieten mit hoher Sterblichkeit die Todesfälle um etwa 14–18 Prozent reduziert. Dieser Erfolg veranlasste die Weltgesundheitsorganisation und Regierungen wie die Nigerias, einen breiteren Einsatz dieser Strategie in Erwägung zu ziehen. Antibiotika töten jedoch nicht nur schädliche Bakterien; sie begünstigen auch das Überleben von Stämmen, die gegen sie resistent sind. In früheren Arbeiten derselben Forschergruppe zeigten sich klare Hinweise auf Azithromycin‑resistente Bakterien bei behandelten Kindern. Unklar war jedoch, ob diese resistenten Keime in behandelten Dörfern bleiben oder nach außen gelangen und so die Wirksamkeit der Antibiotika für andere gefährden.
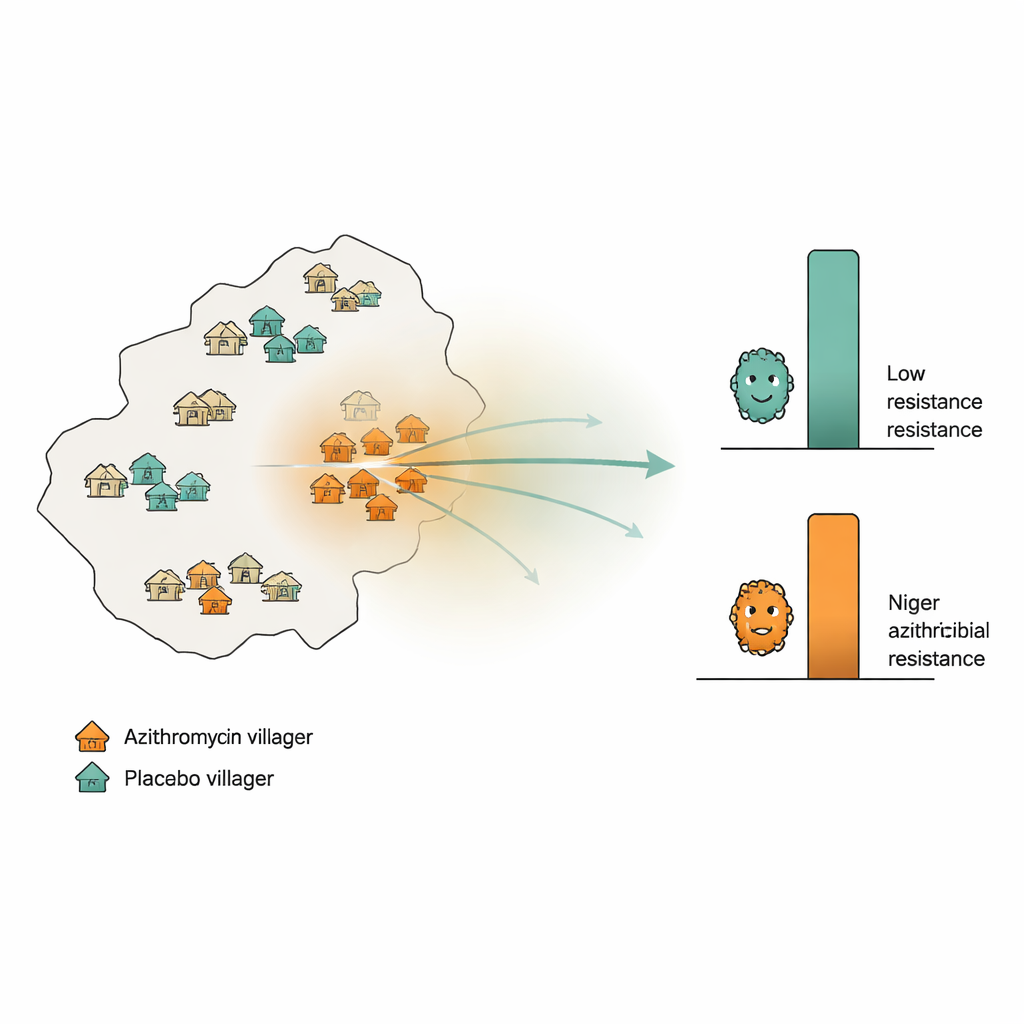
Resistenzverfolgung über eine ländliche Landschaft
Die Forscher nutzten ein großes Überlebensstudienprogramm für Kinder in der Region Dosso in Niger, wo 594 Dörfer zufällig ausgewählt worden waren, entweder zweimal jährlich über zwei Jahre Azithromycin oder ein inaktives Placebo zu erhalten. Zusätzlich wurden 30 separate "Monitoring"‑Dörfer zufällig bestimmt: Die Hälfte erhielt Azithromycin, die andere Hälfte Placebo. Aus diesen Monitoring‑Dörfern entnahm das Team bei Studienbeginn und erneut nach 24 Monaten Rektalabstriche von je 10 Kindern pro Dorf. Mithilfe tiefer DNA‑Sequenzierung bestimmten sie, wie viele Gene, die mit Resistenz gegen Makrolid‑Antibiotika (zur Klasse gehört Azithromycin) verknüpft sind, durchschnittlich in jedem Dorf vorhanden waren. Für jedes Monitoring‑Dorf berechneten sie außerdem, wie intensiv Azithromycin in der Umgebung verwendet wurde — sie zählten alle in nahegelegenen Dörfern verabreichten Dosen und gewichteten Dörfer stärker, die näher lagen.
Suche nach Anzeichen von Ausbreitung zwischen Dörfern
Wenn Resistenz geografisch auslaufen würde, erwarteten die Forscher höhere Werte von Resistenzgenen in Placebo‑Dörfern, die von stark behandelten Nachbarn umgeben waren, verglichen mit Placebo‑Dörfern in Gebieten mit geringem Azithromycin‑Einsatz. Sie prüften diese Idee auf mehrere Weisen: durch einfache rangbasierte Korrelationen zwischen der Intensität der Behandlung in der Umgebung und der Resistenz; durch Wiederholung der Analyse über verschiedene Distanzbänder (innerhalb von 10, 20 oder 30 Kilometern); und durch eine rigorose Permutationsstrategie, bei der die Behandlungszuweisungen in der größeren Studie zufällig vertauscht wurden, um zu sehen, ob scheinbare Muster rein zufällig entstehen könnten. Sie führten außerdem eine "Negative‑Control"‑Analyse durch, die dieselben Berechnungen mit Placebo‑Dosen statt Azithromycin‑Dosen wiederholte; ein ähnliches Muster dort würde auf Confounding und nicht auf echten Spillover hinweisen.
Was die Daten über Resistenz zeigten
Über all diese Prüfungen hinweg zeigten Placebo‑Dörfer niedrige Werte von Makrolid‑Resistenzgenen, die nahe ihren Ausgangswerten blieben, unabhängig davon, wie viel Azithromycin in ihrer Umgebung eingesetzt wurde. Statistische Tests fanden keinen signifikanten Zusammenhang zwischen dem umliegenden Medikamenteneinsatz und der Resistenz in diesen unbehandelten Gemeinden. Im Gegensatz dazu zeigten Dörfer, deren eigene Kinder Azithromycin erhielten, über den Zeitraum von zwei Jahren einen deutlichen Anstieg von Resistenzgenen, was mit direkter Selektion durch die Behandlung übereinstimmt — dieser Anstieg verstärkte sich jedoch nicht systematisch in Gebieten mit höherer umgebender Behandlungsintensität. Als die Forscher lebende Pneumokokken aus den Nasen der Kinder untersuchten, fanden sie erneut keinen Zusammenhang zwischen geografischer Behandlungsintensität und Resistenz. Analysen mit verschiedenen mathematischen Modellen und alternativen Definitionen der Behandlungsintensität führten zu denselben grundlegenden Ergebnissen.
Begrenzungen, Vorbehalte und der größere Kontext
Die Studie kann kleine Spillover‑Effekte nicht vollständig ausschließen, zumal nur 30 Monitoring‑Dörfer intensiv getestet wurden, und sie untersuchte keine sehr feinskalige Ausbreitung innerhalb von Haushalten oder innerhalb einzelner Dörfer. Sie geht außerdem davon aus, dass Entfernung und Anzahl der Dosen die Haupttreiber einer Ausbreitung sind, und konzentriert sich auf ein Zeitfenster von zwei Jahren; langfristigere Effekte oder andere Programmdesigns, etwa solche, die ganze Gemeinden zur Augenerkrankungsbehandlung behandeln, könnten andere Muster zeigen. Trotz dieser Einschränkungen deutet die Evidenz darauf hin, dass in diesem Setting der größte Teil des Resistenzdrucks aus Massenazithromycinkampagnen auf die Gemeinden beschränkt ist, die das Medikament tatsächlich erhalten, und nicht stillschweigend über die Landschaft hinweg verteilt wird.
Was das für künftige Antibiotikakampagnen bedeutet
Für Gesundheitsbehörden in Ländern wie Niger bieten diese Ergebnisse vorsichtige Beruhigung. Während massenhafte Azithromycin‑Behandlungen die Antibiotikaresistenz innerhalb behandelter Dörfer erhöhen, fand diese Studie keine starken Hinweise darauf, dass eine solche Resistenz über 24 Monate hinweg in benachbarte unbehandelte Dörfer ausläuft. Das bedeutet, dass frühere Schätzungen des Resistenzrisikos aus diesen kinderüberlebensfördernden Studien unwahrscheinlich stark durch unerkannte geografische Spillover verzerrt sind. Entscheidungsträger müssen weiterhin den lebensrettenden Nutzen dieser Kampagnen gegen den lokalen Anstieg der Resistenz abwägen, können dies aber mit größerer Zuversicht tun, dass sich das Problem zumindest mittelfristig und im Dorf‑zu‑Dorf‑Maßstab nicht schnell nach außen ausbreitet.
Zitation: Srivathsan, A., Arzika, A.M., Maliki, R. et al. Geographic spillover of antimicrobial resistance from mass distribution of azithromycin. Nat Commun 17, 2152 (2026). https://doi.org/10.1038/s41467-026-68691-y
Schlüsselwörter: antimikrobielle Resistenz, Azithromycin, Massenmedikation, Kindersterblichkeit, Niger