Clear Sky Science · de
Funktionelle und strukturelle Einblicke in Wechselwirkungen zwischen β-Arrestin 1 und Gαs bzw. Gαi1
Warum das für Gesundheit und Medizin wichtig ist
Viele heutige Medikamente — von Allergietabletten über Herzmittel bis zu Psychopharmaka — wirken, indem sie eine große Familie von Zelloberflächenproteinen ansteuern, die als G-Protein-gekoppelte Rezeptoren (GPCRs) bezeichnet werden. Diese Rezeptoren übermitteln Signale in die Zelle mithilfe von zwei Haupthelfern: G-Proteinen und Proteinen, die Beta-Arrestine genannt werden. Diese Studie untersucht, wie ein Beta-Arrestin (Beta-Arrestin 1) direkt mit zwei Typen von G-Proteinen innerhalb der Zelle kommuniziert. Das Verstehen dieses verborgenen Gesprächs könnte Forschern helfen, präzisere Medikamente mit weniger Nebenwirkungen zu entwickeln, indem sie die Signalweiterleitung innerhalb unserer Zellen gezielter steuern.
Zwei wichtige Botenstoffe in unseren Zellen
Wenn ein Hormon oder ein Medikament an einen GPCR an der Zelloberfläche bindet, löst das zwei grundlegende Kommunikationswege aus. Ein Weg nutzt G-Proteine, die wie molekulare Timer durch den Austausch eines kleinen Moleküls (GDP gegen GTP) an- und abgeschaltet werden. Der andere Weg nutzt Beta-Arrestine, die sowohl die G-Protein-Signalgebung beenden als auch eigene Signalwege aktivieren können. Lange Zeit untersuchten Wissenschaftler vor allem, wie Rezeptoren getrennt mit G-Proteinen oder Beta-Arrestinen interagieren. Neuere Arbeiten deuteten jedoch darauf hin, dass G-Proteine und Beta-Arrestine auch direkt aneinander binden oder sogar große „Mega-Komplexe“ mit dem Rezeptor bilden könnten. Die Details, wie diese Proteine gekoppelt sind und was das für die Signalübertragung bedeutet, blieben jedoch unklar.
Messen, wer an wen bindet
In dieser Studie konzentrierten sich die Forscher auf Beta-Arrestin 1 und zwei G-Protein-„Alpha“-Untereinheiten: Gαs, das in der Regel zelluläre Aktivität anregt, und Gαi1, das sie im Allgemeinen dämpft. Mit einer empfindlichen Bindungstechnik testeten sie, wie stark gereinigtes Beta-Arrestin 1 und jedes G-Protein unter verschiedenen Bedingungen aneinander haften. Sie fanden heraus, dass entscheidend nicht ist, ob das G-Protein „an“ oder „aus“ ist, sondern ob Beta-Arrestin 1 in einer aktiveren, flexibleren Form vorliegt. Eine Version von Beta-Arrestin 1, der sein C-Terminus fehlt — die sich wie ein lockeres, aktives Ensemble von Konformationen verhält — band stark an sowohl Gαs als auch Gαi1. Im Gegensatz dazu band die ruhende Form von Beta-Arrestin 1 oder eine Form, die durch ein rezeptorähnliches Peptid fixiert war, schwach oder gar nicht. Das deutet darauf hin, dass G-Proteine bevorzugt Beta-Arrestin 1 erkennen, wenn dieses aktive-ähnliche Zustände durchläuft, die nach Rezeptoraktivierung auftreten können. 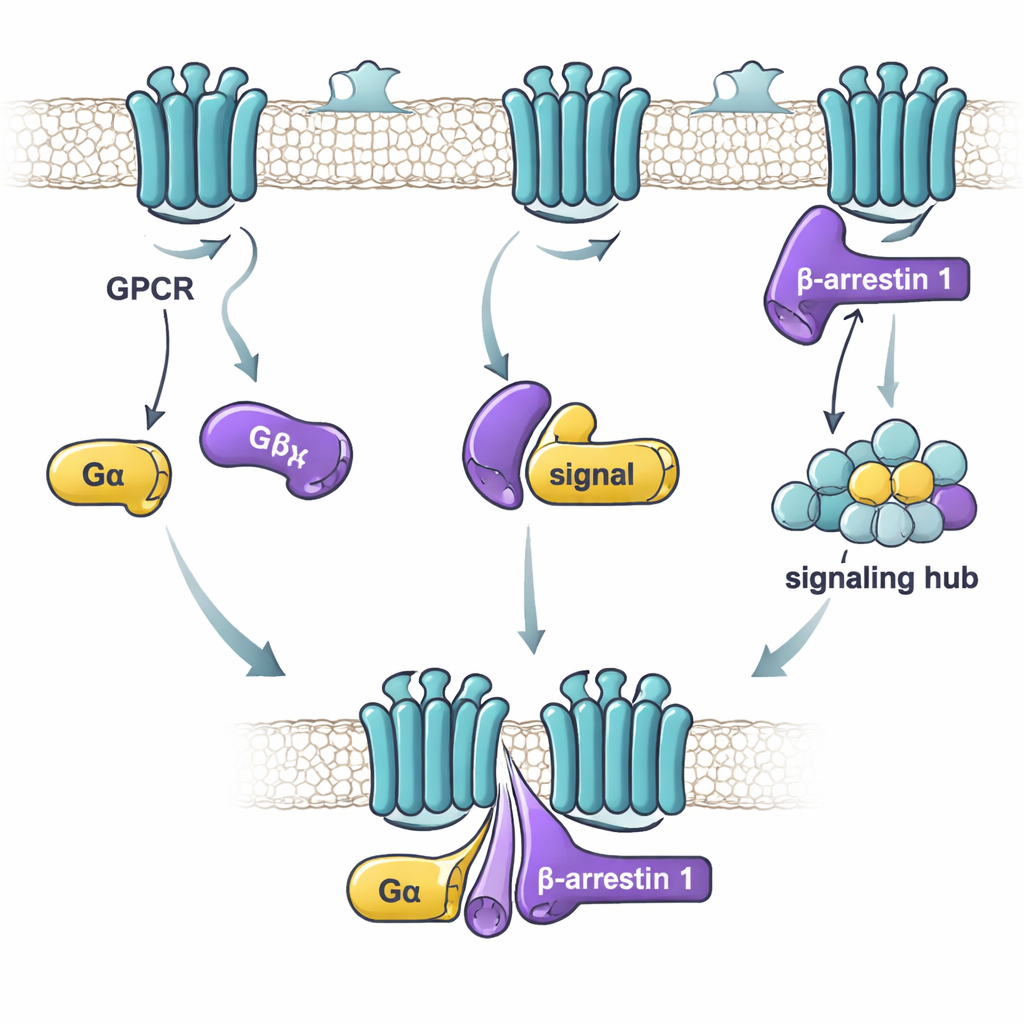
Beobachtung subtiler Formänderungen
Um zu sehen, wie die Bindung die Proteinstruktur beeinflusst, verwendete das Team eine Methode, die verfolgt, wie schnell Wasserstoffatome am Proteinrückgrat mit schwerem Wasserstoff aus dem Lösungsmittel ausgetauscht werden. Langsamerer Austausch bedeutet in der Regel, dass eine Region stärker geschützt oder starrer geworden ist; schnellerer Austausch deutet auf erhöhte Flexibilität oder Exposition hin. Wenn das aktive-ähnliche Beta-Arrestin-1-Fragment an Gαs oder Gαi1 band, zeigten beide G-Proteine deutliche Musterveränderungen in mehreren Bereichen, was darauf hindeutet, dass sie sich um den Komplex herum umgestalteten. Im Gegensatz dazu veränderte sich Beta-Arrestin 1 selbst nur geringfügig, hauptsächlich in flexiblen Schleifen. Durch Experimente mit isolierten Domänen der G-Proteine zeigten die Forscher außerdem, dass sowohl der katalytische „Ras-ähnliche“ Teil als auch der umgebende alpha-helikale Abschnitt zur Bindung beitragen. Beim Gαs spielt die helikale Region eine besonders starke Rolle; beim Gαi1 sind beide Regionen etwa gleichbedeutend.
Funktion ohne Umschalten des Hauptschalters
Die nächste Frage war, ob dieser direkte Kontakt beeinflusst, wie G-Proteine aktiviert werden. Das Team verwendete eine fluoreszierende GTP-analoge Sonde, die aufleuchtet, wenn ein G-Protein von GDP auf GTP wechselt — ein standardmäßiger Aktivitätsnachweis. Überraschenderweise veränderte die Zugabe von Beta-Arrestin 1 weder die Geschwindigkeit noch das Ausmaß dieses Nukleotidaustauschs für Gαs oder Gαi1. Mit anderen Worten: Beta-Arrestin 1 wirkt nicht wie ein klassisches „Einschalt“-Enzym für G-Proteine. Stattdessen zeigt sich sein Einfluss an seiner eigenen Struktur. Mit einem geschickt konstruierten Beta-Arrestin 1, dessen Schwanzbewegung über Fluoreszenz verfolgt werden konnte, fanden sie, dass aktives Gαs, nicht aber Gαi1, die Freisetzung des C-terminalen Schwanzes von Beta-Arrestin fördert, wenn ein rezeptorabgeleitetes Peptid vorhanden ist. In lebenden Zellen bestätigten zusätzliche Bildgebungs- und Energieübertragungs-Sensoren, dass Gαs und Beta-Arrestin 1 bei Hormonstimulation nahe zusammenkommen und dass Gαs Beta-Arrestin 1 in eine aktivere Konformation drängt. 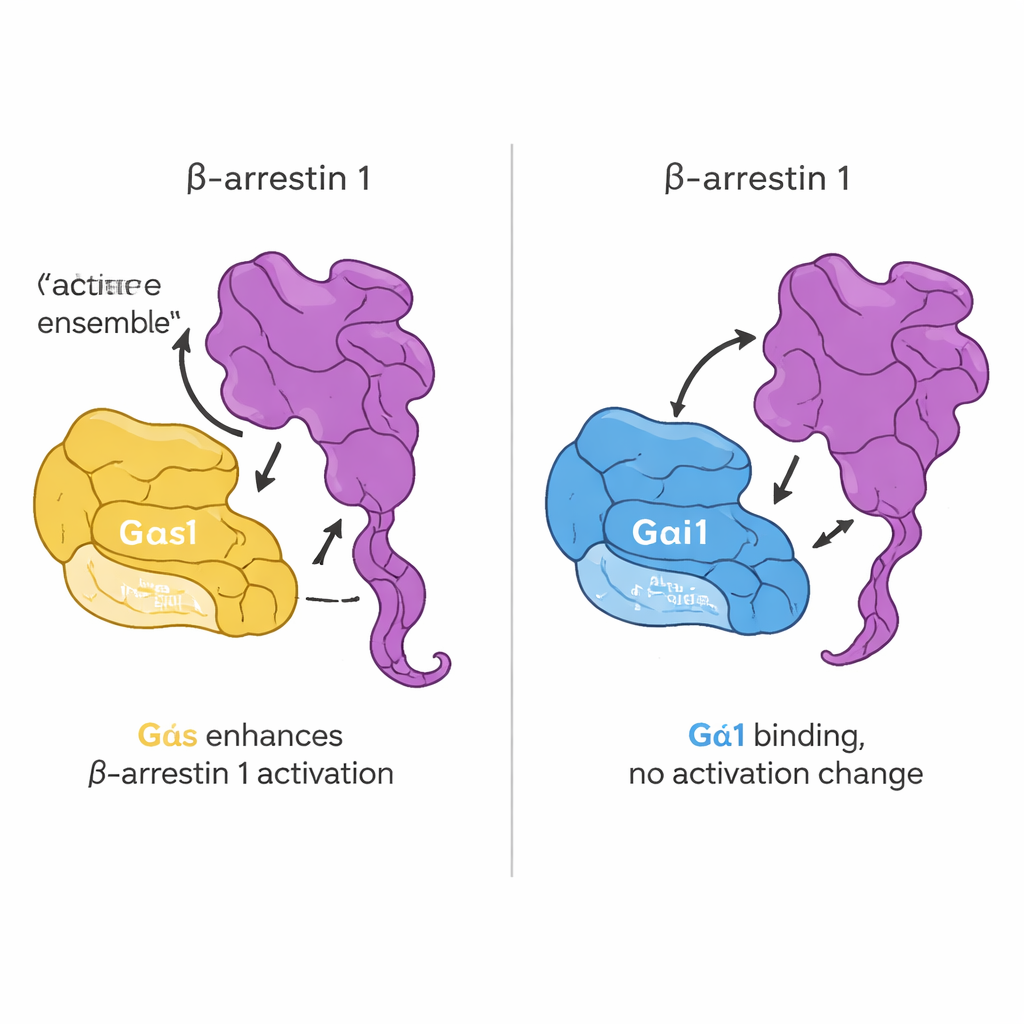
Eine neue Ebene der Kontrolle in der Zell-Signalgebung
In der Zusammenführung dieser Ergebnisse schlagen die Autoren vor, dass Gαs und Gαi1 beide direkt an Beta-Arrestin 1 binden, jedoch auf leicht unterschiedliche Weise und mit verschiedenen Folgen. Keines der G-Proteine ändert durch diesen Kontakt sein Haupt-„Ein/Aus“-Verhalten. Stattdessen wirkt die Interaktion, besonders bei Gαs, eher wie ein Feinstellknopf an Beta-Arrestin 1, der es in eine stabilere, aktivere, Schwanz-freigegebene Form drängt oder so stabilisiert. Das fügt der GPCR-Signalgebung eine bisher unterschätzte Ebene hinzu: Rezeptoren können nicht nur G-Proteine und Beta-Arrestine koordinieren, sondern G-Proteine und Beta-Arrestine können auch direkt gegenseitig modulieren. Langfristig könnte die Kartierung dieser subtilen Wechselwirkungen Designern von Arzneistoffen dabei helfen, Signale in nützliche Bahnen zu lenken — förderliche Wege zu verstärken und diejenigen zu vermeiden, die Nebenwirkungen verursachen.
Zitation: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Schlüsselwörter: G-Protein-gekoppelte Rezeptoren, Beta-Arrestin, G-Protein-Signalgebung, Zelluläre Signalübertragungsmechanismen, Strukturelle Biologie