Clear Sky Science · de
Epigenomweite Analyse identifiziert DNA-Methylierungsvermittler des behandlungsbedingten kardiometabolischen Risikos bei Überlebenden von Kinderkrebs
Warum die Nachwirkungen von Krebs im Körper nachhallen
Dank besserer Therapien werden die meisten Kinder mit Krebs heute erwachsen. Viele dieser Überlebenden sehen sich jedoch Jahrzehnte später neuen Gesundheitsproblemen gegenüber, darunter Fettleibigkeit, Bluthochdruck und diabetesähnliche Zustände. Diese Studie stellt eine drängende Frage: Wie hinterlassen Behandlungen in der Kindheit so langanhaltende Folgen für Herz und Stoffwechsel? Durch die Untersuchung chemischer Markierungen auf DNA in Blutzellen finden die Forschenden Hinweise darauf, dass frühere Chemotherapien und Bestrahlungen den Körper „umprogrammieren“ könnten und so das langfristige kardiometabolische Risiko erhöhen.
Verborgene Risiken bei erwachsenen Kinderkrebsüberlebenden verfolgen
Das Team untersuchte fast 3.000 Erwachsene, die Kinderkrebs überlebt haben und langfristig in der St. Jude Lifetime Cohort nachbetreut werden. Diese Überlebenden waren in der Kindheit verschiedenen Chemotherapien und Bestrahlungen am Kopf oder Rumpf (Brustkorb, Bauch, Becken) ausgesetzt und kehrten Jahre später für umfassende Gesundheitschecks und Blutuntersuchungen zurück. Die Forschenden konzentrierten sich auf fünf zentrale kardiometabolische Probleme, die bekanntermaßen das Risiko für Herzkrankheiten und vorzeitigen Tod erhöhen: Fettleibigkeit, gestörte Blutzuckerwerte, hohe Triglyceride, hoher Cholesterinspiegel und Bluthochdruck. Durch den Vergleich von Überlebenden mit und ohne diese Erkrankungen suchten sie an Millionen Genomstellen nach Unterschieden in der DNA-Methylierung — winzigen chemischen Schaltern, die mitsteuern, wie Gene ein- oder ausgeschaltet werden.
Chemische Markierungen auf DNA als Gedächtnis der Behandlung
Im gesamten Genom fanden die Forschenden fast 1.900 DNA-Stellen, deren Methylierungsniveaus mit mindestens einer der fünf kardiometabolischen Erkrankungen verknüpft waren. Die meisten dieser Stellen standen im Zusammenhang mit nur einem Problem, doch eine kleine Gruppe schien als „Hubs“ mit mehreren Problemen verbunden zu sein. Fünf Schlüsselstellen, gelegen in der Nähe von zwei Genen namens CPT1A und LMNA, waren mit allen fünf kardiometabolischen Risiken gleichzeitig assoziiert. Diese Gene sind dafür bekannt, die Fettverarbeitung im Körper und die zelluläre Struktur aufrechtzuerhalten, was nahelegt, dass die Behandlung gemeinsame Stoffwechsel- und Herz-Kreislauf-Wege stören könnte. Viele der Methylierungsänderungen überschneiden sich mit Signalen, die zuvor in der Allgemeinbevölkerung beobachtet wurden, insbesondere solchen im Zusammenhang mit Entzündungen, andere schienen jedoch spezifisch für Krebsüberlebende zu sein — ein Hinweis darauf, dass die Behandlung einen eigenen charakteristischen biologischen Abdruck hinterlässt.
Therapie, DNA-Veränderungen und Krankheit verbinden
Der nächste Schritt war zu prüfen, ob diese Methylierungsänderungen tatsächlich dazu beitragen, zu erklären, wie Therapie später zu Erkrankungen führt, und nicht nur als Begleiterscheinung auftreten. Die Forschenden konzentrierten sich auf neue oder sich verschlechternde kardiometabolische Probleme, die erst nach der Blutentnahme auftraten, um die zeitliche Abfolge von Behandlung zu DNA-Veränderung zu Krankheit zu wahren. Mithilfe statistischer Mediationsanalysen identifizierten sie 24 Methylierungsstellen, die zusammen bis zu etwa einem Viertel des Zusammenhangs zwischen bestimmten Behandlungen und späteren kardiometabolischen Problemen erklärten. Bestrahlungen des Kopfes und des Rumpfes zeigten besonders starke Muster: Gruppen von Methylierungsstellen erklärten zusammen etwa 10–20 % der Wirkung dieser Strahlentherapien auf gestörte Blutzuckerwerte. Eine herausragende Stelle nahe dem Gen ANTXR2 schien etwa 20 % des Effekts der Rumpfbestrahlung auf spätere Glukoseprobleme zu vermitteln.
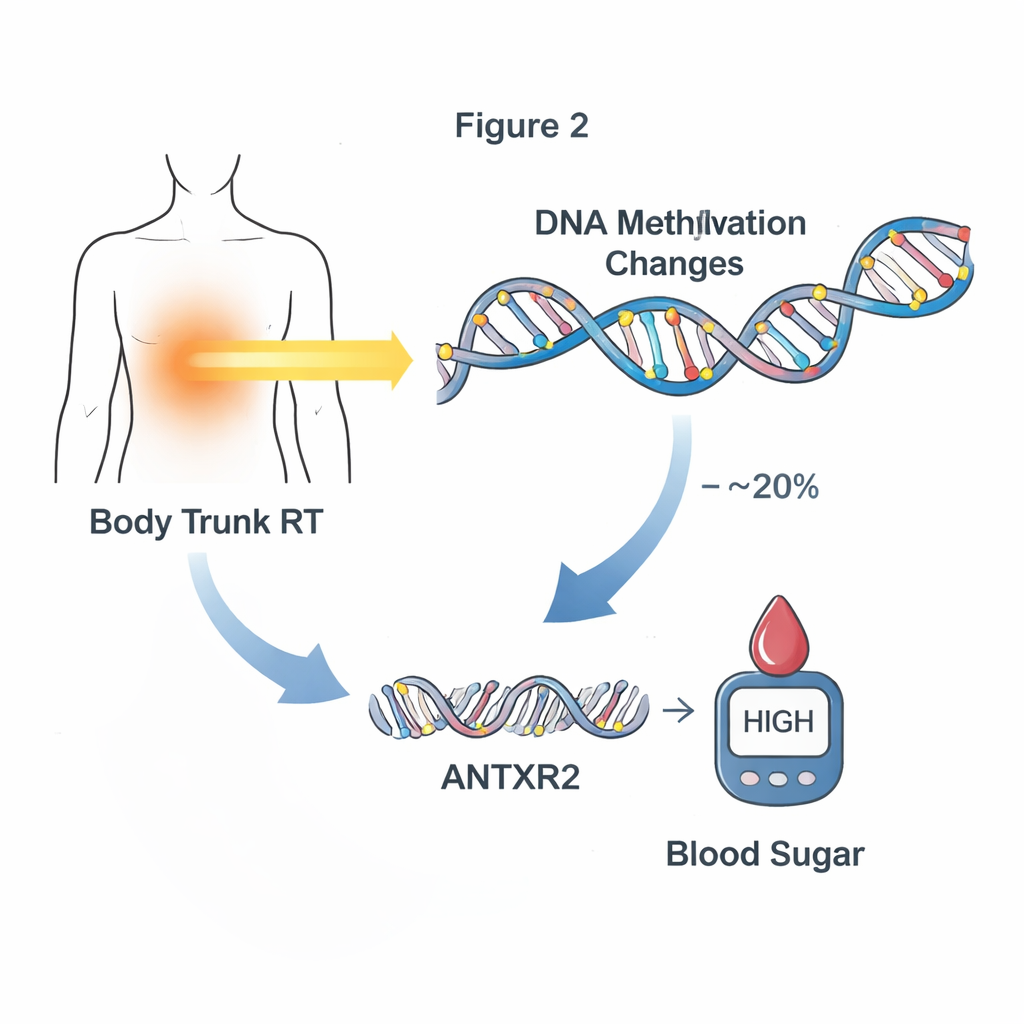
Von DNA-Marken zur Genaktivität
Um zu verstehen, wie diese Methylierungsmarken die Biologie verändern könnten, untersuchte das Team die Genaktivität in einer Teilgruppe von Überlebenden, für die sowohl DNA- als auch RNA-Daten aus dem Blut vorlagen. Sie fanden Dutzende von Methylierungsstellen, bei denen höhere oder niedrigere Methylierung mit Veränderungen der Expression benachbarter Gene verknüpft war. Darunter war die Schlüssel-Mediatorstelle nahe ANTXR2, bei der die Methylierungsniveaus stark mit der Expression dieses Gens verbunden waren, insbesondere bei Überlebenden, die eine Rumpfbestrahlung erhalten hatten. ANTXR2 reguliert Blutgefäße und das umliegende Gewebegefüge — Systeme, die beeinflussen, wie Glukose und Insulin sich im Körper bewegen. Dieses Muster deutet auf eine Ereigniskette hin, in der Strahlung die Methylierung verändert, was die Genaktivität verschiebt und dadurch den Körper in Richtung gestörter Blutzuckerregulation drängt.
Was das für Überlebende und künftige Versorgung bedeutet
Für Nicht-Fachleute ist die Kernbotschaft: Krebsbehandlungen in der Kindheit schädigen nicht nur Gewebe im Moment der Therapie; sie können auch langanhaltende „Notizen“ auf der DNA hinterlassen, die die Gesundheit über Jahrzehnte prägen. In dieser Studie helfen einige dieser Notizen — DNA-Methylierungsänderungen — zu erklären, warum bestimmte Überlebende ein höheres Risiko haben, Fettleibigkeit, erhöhte Blutfettwerte oder Glukoseprobleme im Zusammenhang mit Diabetes und Herzkrankheiten zu entwickeln. Während diese chemischen Markierungen nur einen Teil der Erklärung liefern, könnten sie letztlich als blutbasierte Biomarker dienen, um Überlebende mit dem höchsten Risiko zu identifizieren und um zu testen, ob Lebensstiländerungen oder neue Therapien einen Teil dieser epigenetischen Geschichte sicher überschreiben können. Die Arbeit bringt die Nachsorge einen Schritt näher zur Präzisionsmedizin: molekulare Fußabdrücke früherer Behandlung zu nutzen, um eine frühere, gezieltere Prävention von Herz- und Stoffwechselerkrankungen zu ermöglichen.
Zitation: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Schlüsselwörter: Überlebende von Kinderkrebs, DNA-Methylierung, kardiometabolisches Risiko, Strahlentherapie, Epigenetik