Clear Sky Science · de
Kotranslationale Bestimmung quaternärer Strukturen in Chaperon-Fabriken
Wie zelluläre „Fertigungsstraßen“ große Maschinen in Form halten
In jeder unserer Zellen müssen Tausende Proteinbauteile zu komplexen molekularen Maschinen zusammensetzen, von den Motoren, die DNA kopieren, bis zu den Fabriken, die andere RNAs herstellen. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie entscheiden Zellen in Echtzeit, welche Helferproteine jedes neu entstehende Teil beim Aufbau begleiten, und wie organisieren sie diesen Prozess in der chaotischen Flüssigkeit der Zelle?
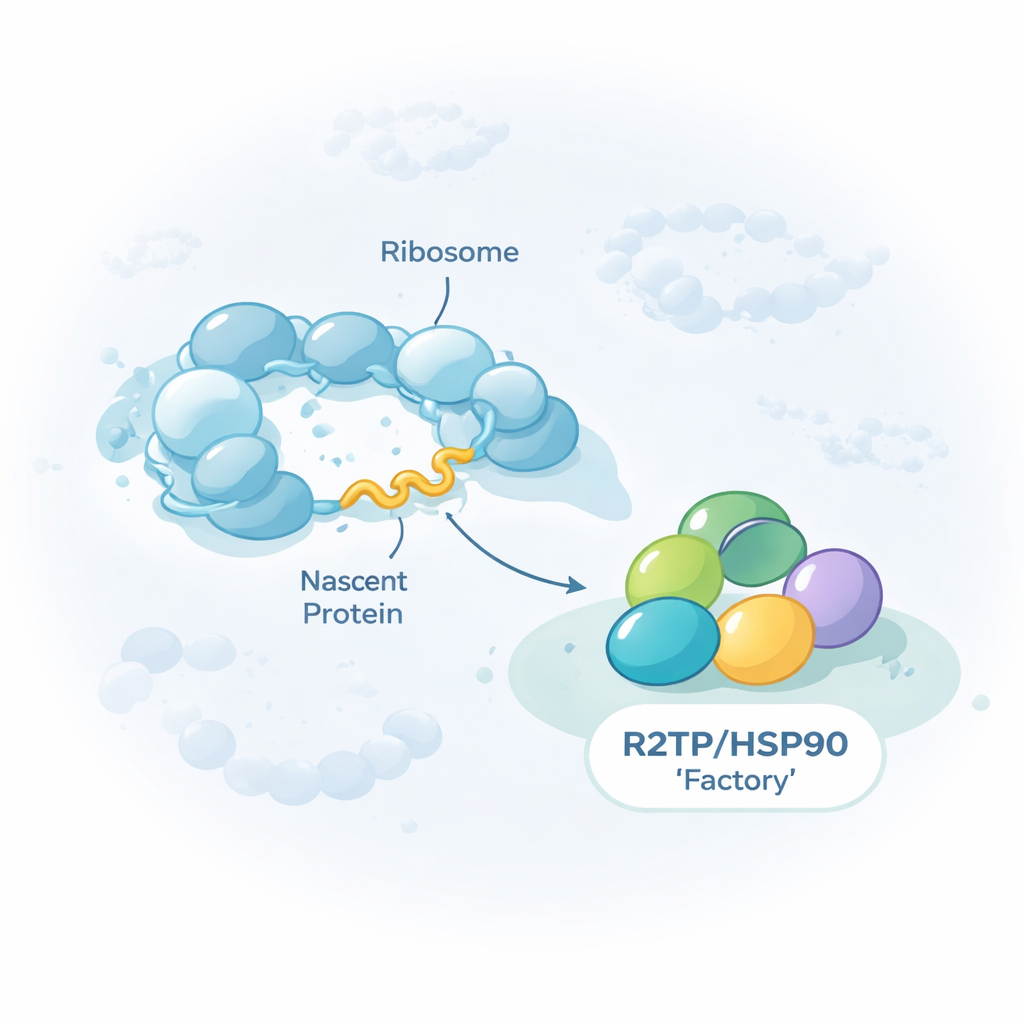
Ein Allzweckhelfer für zelluläre Megamaschinen
Die Arbeit konzentriert sich auf eine Gruppe von Helferproteinen beziehungsweise Chaperonen, die als HSP90/R2TP bekannt sind. Statt einzelne Proteine zu falten, ist dieses Chaperon auf den Zusammenbau riesiger Mehrkomponentenkomplexe spezialisiert, darunter die drei nuklearen RNA-Polymerasen, die DNA in RNA transkribieren, bestimmte RNA–Protein-Partikel und große Remodelling-Maschinen, die die DNA-Verpackung umgestalten. Die Autoren zeigen, dass R2TP diese Klienten nicht erst nach deren Fertigstellung trifft. Stattdessen bindet es häufig bereits, während jedes Klienten noch an Ribosomen, den Proteinproduktionsmaschinen der Zelle, hergestellt wird. Durch Anreicherung von R2TP aus humanen Zellen und Sequenzierung der mitgefangenen RNAs identifizierten sie etwa 150 Boten-RNAs, deren kodierte Proteine während ihrer eigenen Translation von R2TP kontaktiert werden.
Helfer, die auf wachsenden Proteinketten mitfahren
Um zu prüfen, ob diese Bindung wirklich während der Proteinsynthese stattfindet, setzte das Team Wirkstoffe ein, die die Translation einfrieren oder stören. Wenn sie Verbindungen verwendeten, die wachsende Proteinketten von Ribosomen abziehen, verschwanden die meisten Boten-RNAs aus R2TPs Griff. Wurde jedoch ein Medikament eingesetzt, das Ribosomen nur anhält und die naszierenden Ketten angeschlossen lässt, nahm die R2TP-Bindung zu. Mit konstruierten Reporter-RNAs bestätigten sie dies: Wird die Translation künstlich früh gestoppt, bindet das Chaperon die Nachricht nicht mehr. Zusammengenommen deuten diese Ergebnisse auf eine klare Eingreifregel hin: R2TP erkennt seine Klienten primär über die entstehende Proteinkette, wie sie aus dem Ribosom herauskommt, und weniger über die RNA-Sequenz selbst.
Chaperon-gebaute „Fabriken“, die spezifische Nachrichten konzentrieren
Mit fortgeschrittener Einzelmolekül-Bildgebung machten die Autoren dann eine überraschende Entdeckung. Anstatt viele verschiedene Klienten-Nachrichten zufällig verteilt zu sehen, beobachteten sie, dass einige Schlüsseltranskripte – insbesondere jene, die die großen Untereinheiten der RNA-Polymerase II und einen großen Spleißfaktor namens PRPF8 kodieren – sich oft in hellen Foci im Zytoplasma sammelten. Diese Foci waren angereichert an R2TP und seinem Partner HSP90 sowie an ribosomalen Komponenten und den gerade entstehenden Proteinen, was zeigt, dass es aktive Translationsorte sind. Wurden Translation oder die energieabhängige ATPase-Aktivität von R2TP oder HSP90 blockiert, lösten sich diese Foci auf. Die Autoren bezeichnen diese Strukturen als „R2TP-Fabriken“: spezialisierte Kondensate, in denen ausgewählte Boten-RNAs und Chaperone konzentriert werden, um zeitnahe, schützende Kontakte zwischen entstehenden Proteinketten und ihren Assemblierungshilfen zu begünstigen.
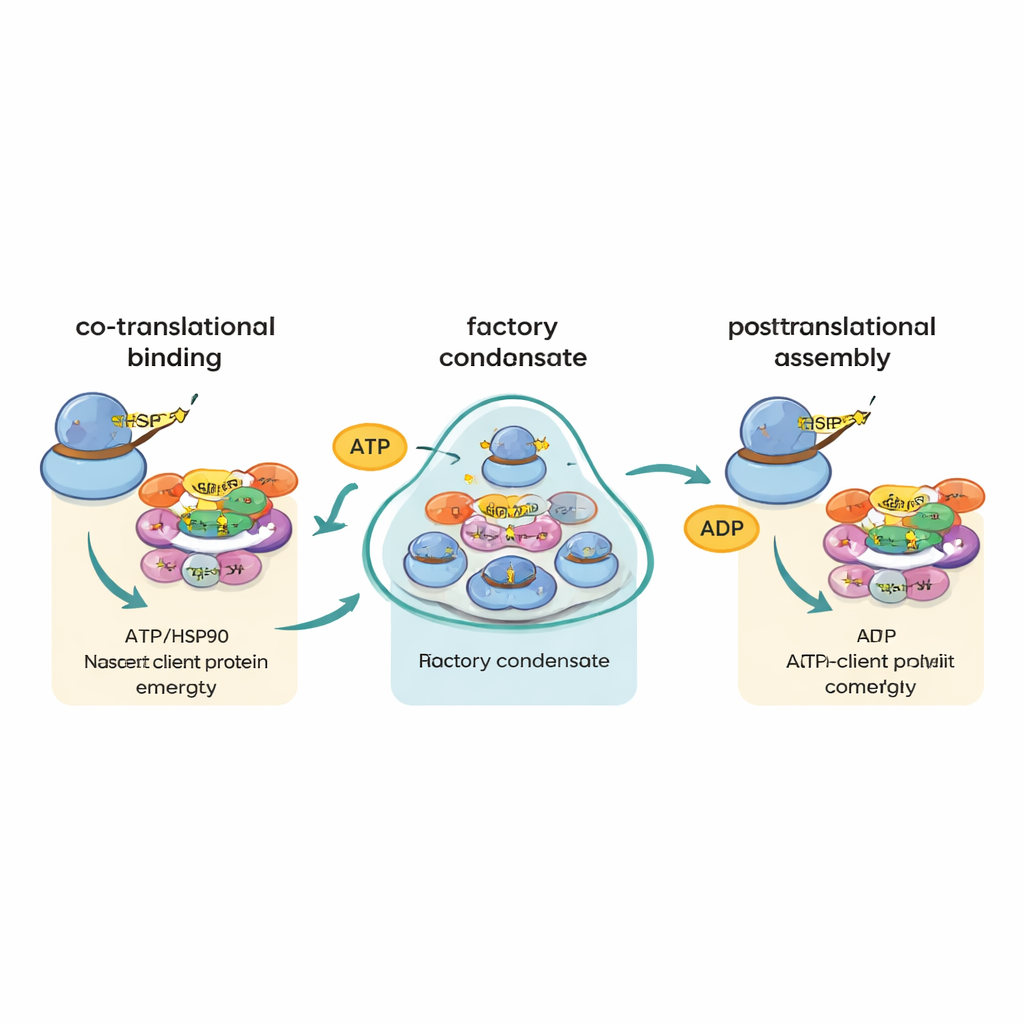
Bauteile lenken, ohne ihre Baupläne zusammenzuführen
Eine frühere Idee war, dass Nachrichten für verschiedene Teile desselben Komplexes sich finden und nebeneinander translatiert werden könnten, sodass ihre Proteinprodukte sofort zusammengesetzt werden. Die neue Arbeit schließt dieses „ko-lokalisierte Bauplan“-Modell weitgehend aus. Selbst für Proteingepaare, von denen bekannt ist, dass sie im selben Komplex zusammenkommen, traten ihre Boten-RNAs selten gemeinsam auf. Stattdessen stützen die Daten eine andere Strategie, die die Autoren „kotranslationelle Chaperon-Weiterleitung“ oder kurz „cha-cha“ nennen. In diesem Modell heften sich R2TP und HSP90 an, sobald ein großes oder assemblierungsempfindliches Protein aus dem Ribosom zu erscheinen beginnt, und bestimmen dessen Schicksal, indem sie es durch weitere Assemblierungsschritte führen. Die Fabriken selbst bringen demnach nicht primär passende Nachrichten zusammen; vielmehr erhöhen sie die Wahrscheinlichkeit, dass anfällige neue Proteine rasch auf das richtige Chaperon treffen.
Warum diese verborgene Organisation für Gesundheit und Krankheit wichtig ist
Indem die Studie zeigt, dass R2TP und HSP90 nicht nur fragile Proteinbauteile schützen, sondern auch den Ort und die Art ihrer Translation mitgestalten, legt sie eine unerwartete Ebene intrazellulärer Organisation offen. Der cha-cha-Mechanismus hilft zu erklären, wie Zellen zuverlässig riesige molekulare Komplexe bauen, obwohl die Nachrichten für ihre Teile selten die gleiche Adresse teilen. Er erklärt auch, warum Defekte in Chaperonen oder ihren Energiesystemen lebenswichtige Maschinen wie RNA-Polymerasen und Spleißfaktoren destabilisieren können, mit Folgen von Entwicklungsstörungen bis hin zu Krebs. Im Kern zeigt die Arbeit, dass Zellen auf dynamische Chaperon-„Fabriken“ angewiesen sind, um frisch hergestellte Bauteile in die richtigen Assemblies zu lenken und so ihre innere Maschinerie effizient und geordnet zu halten.
Zitation: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Schlüsselwörter: Protein-Chaperone, kotranslationeller Zusammenbau, molekulare Maschinen, RNA-Polymerase, zelluläre Qualitätskontrolle