Clear Sky Science · de
Iterative Entdeckung potenter polymerer Antibiotika mittels mehrstufigem und multitaskendem Lernen gegen antimikrobielle Resistenz
Warum neue Antibiotika uns alle betreffen
Medikamentenresistente Infektionen nehmen weltweit zu und machen vertraute Erkrankungen schwerer und mitunter unbehandelbar. Diese Studie beschreibt einen neuen Weg, schnell eine andere Art von Antibiotikum zu entdecken: winzige synthetische Polymere, die sowohl hartnäckige Bakterien abtöten als auch alten Medikamenten wie Penicillin wieder Wirksamkeit verleihen können. Die Arbeit verbindet fortgeschrittene künstliche Intelligenz mit Chemie und Tierexperimenten, um einen enormen chemischen Raum zu durchsuchen, den man mit trial-and-error nicht erschließen könnte.
Auf der Suche nach neuen Verteidigern in einem überfüllten chemischen Universum
Konventionelle Antibiotika zielen meist auf bestimmte bakterielle Proteine, denen Bakterien nach und nach entgehen können. Im Gegensatz dazu ahmen die in dieser Studie untersuchten Polymere körpereigene Abwehrpeptide nach, die physisch bakterielle Membranen schädigen und weniger anfällig für Resistenzentwicklung sind. Die Herausforderung ist, dass es Zehntausende möglicher Polymerstrukturen gibt und ihr Verhalten von einem feinen Gleichgewicht aus positiver Ladung sowie wasser- und fettliebenden Komponenten abhängt. Manuelle Tests in ausreichender Menge, um sichere und wirkstarke Kandidaten zu finden, würden Jahre dauern. Die Autor*innen bauten eine kombinatorische Bibliothek von rund 100.000 verwandten Polymeren auf, sogenannte Poly(β‑Aminoester), die jeweils so entworfen wurden, dass sie sich zu nanoskaligen Partikeln selbstassemblieren, die stark mit bakteriellen Zelloberflächen interagieren können.
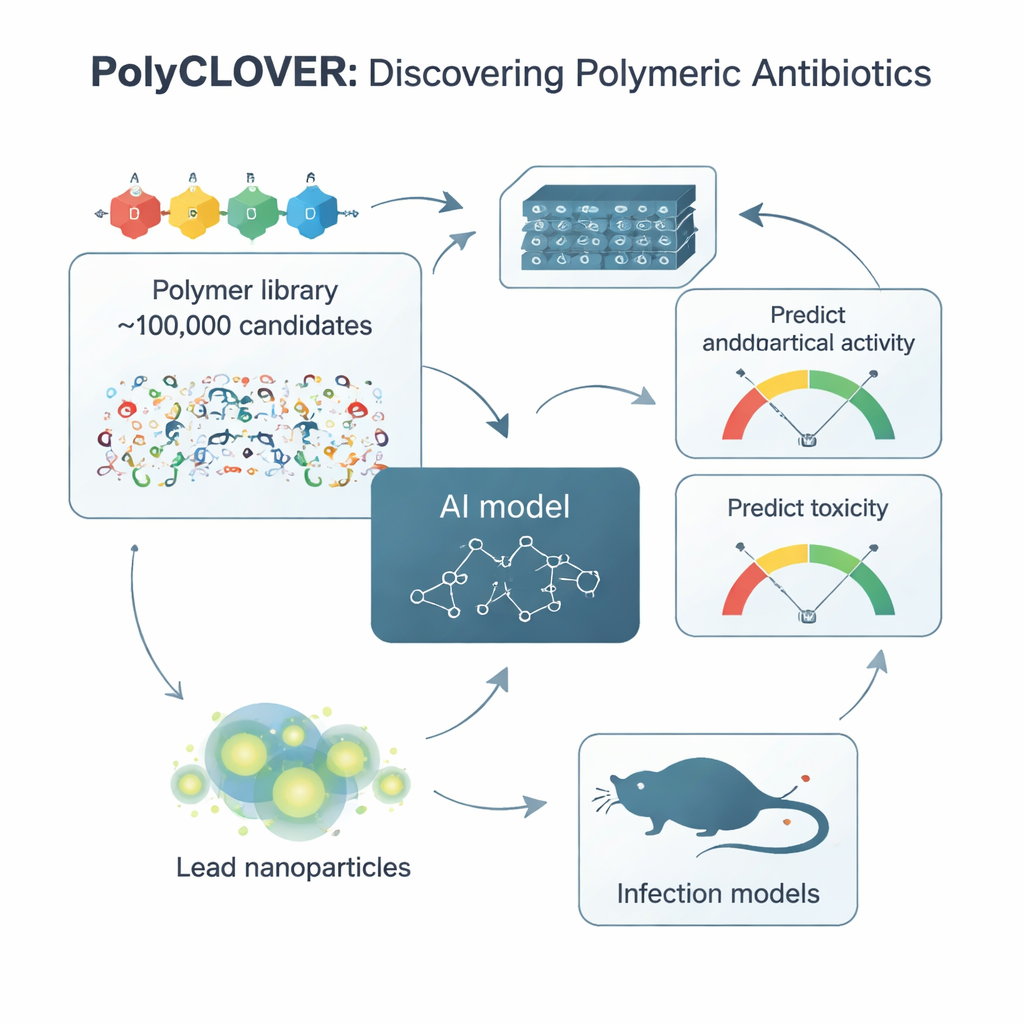
Der KI beibringen, die „Körpersprache" von Polymeren zu lesen
Um diese Bibliothek zu navigieren, entwickelte das Team ein Framework namens PolyCLOVER. Im Kern steht ein graphbasiertes neuronales Netzwerk, das jedes Polymer wie ein Netzwerk verbundener Atome behandelt und dem Modell erlaubt, subtile Strukturunterschiede zu erfassen. Da nur sehr wenige annotierte Beispiele vorlagen, welche Polymere gute oder schlechte Antibiotika sind, nutzten die Forschenden eine mehrstufige, selbstüberwachte Lernstrategie. Zuerst wurde das Modell an etwa einer Million unbeschrifteter Polymerstrukturen trainiert, um allgemeine chemische Muster zu erfassen. Dann wurde es weiter auf der unbeschrifteten Bibliothek mit 100.000 Mitgliedern trainiert und schließlich an einer kleinen Menge von 220 Polymeren feinjustiert, die synthetisiert und sowohl auf antibakterielle Wirksamkeit als auch auf Schädigung roter Blutkörperchen getestet worden waren. Dieses gestufte Lernen verbesserte die Fähigkeit des Modells dramatisch, vorherzusagen, welche neuen Polymere zugleich potent und sicher sind.
Experimente und Algorithmen voneinander lernen lassen
PolyCLOVER bleibt nicht bei einer einzigen Vorhersagerunde stehen. Es läuft in einer Schleife, in der die KI die vielversprechendsten und informativsten Kandidaten vorschlägt, Chemiker*innen sie in Hochdurchsatzformat synthetisieren und testen und die neuen Ergebnisse zurückfließen, um das Modell zu verfeinern. Der Auswahlschritt verwendet einen „upper confidence bound“-Ansatz, der Exploitation (Bevorzugung gut vorhergesagter Polymere) und Exploration (Erkundung unsicherer Bereiche, in denen das Modell am meisten lernen kann) ausbalanciert. Über etwa vier iterative Runden verbesserten sich die vorgeschlagenen Polymere stetig: Sie wurden wirksamer gegen Methicillin-resistente Staphylococcus aureus (MRSA), während die Toxizität gegenüber roten Blutkörperchen im akzeptablen Bereich blieb. Innerhalb von nur 20 Tagen Experimentierzeit konvergierte das System auf eine kleine Gruppe von Spitzenkandidaten.
Winzige selbstassemblierende Partikel, die Löcher in Bakterien stanzen
Die finalen drei Leitpolymere, bezeichnet H1, H2 und H3, bildeten spontan positiv geladene Nanopartikel von etwa 100 Nanometern Durchmesser. In Labortests töteten sie MRSA ebenso effektiv wie ein Standardantibiotikum, Streptomycin, und das deutlich schneller—sie reduzierten die Bakterienzahl binnen Minuten bis Stunden um mehrere Größenordnungen, selbst in proteinreichem Serum. Elektronenmikroskopie und fluoreszierende Sonden zeigten, dass diese Partikel rasch an der bakteriellen Oberfläche andocken und die Integrität und das elektrische Potenzial der Membran stören, wodurch Zellinhalte auslaufen. Wichtig ist, dass MRSA nach nahezu einem Monat Exposition gegenüber diesen Polymeren sehr wenig Resistenz entwickelte, im krassen Gegensatz zu Streptomycin, dessen erforderliche Dosis im selben Zeitraum stark anstieg.
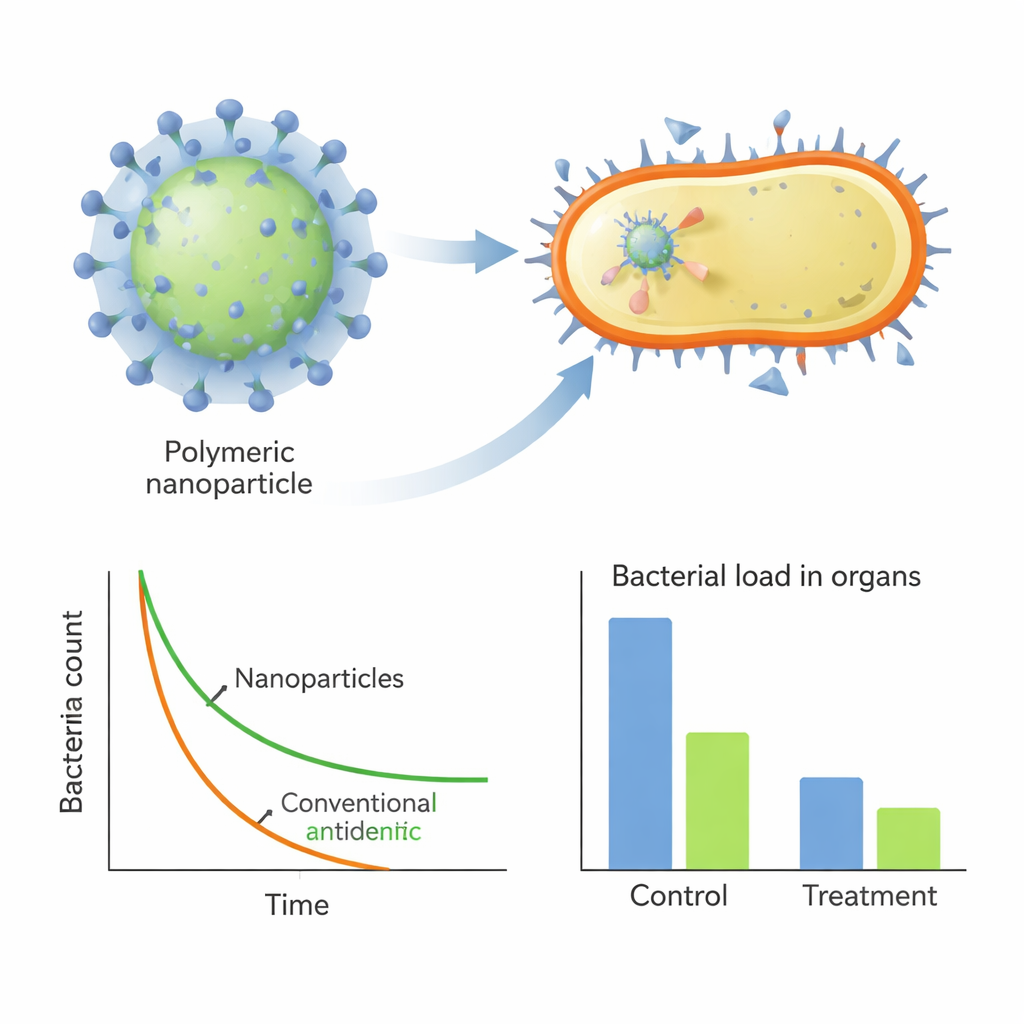
Alte Antibiotika in Tierinfektionen wieder zum Leben erwecken
Neben ihrer Eigenwirkung fungierten die Nanopartikel auch als starke Helfer für herkömmliche Medikamente. In Kombination mit Penicillin G, gegen das MRSA normalerweise stark resistent ist, bildete das beste Polymer (H2) Nanokomposite, die das Antibiotikum im Partikel einschlossen. Diese Verbunde zeigten im Labor starke Synergie und senkten die für die Hemmung von MRSA erforderliche Penicillindosis drastisch. In Mausmodellen für Lungeninfektion und eine schwere Bauchhöhleninfektion führten Behandlungen mit den Leitpolymeren—allein oder in Kombination mit Penicillin—zu deutlich reduzierten Bakterienlasten in Organen, verringerten Entzündungsmarker im Blut und begrenzten Gewebeschäden, alles ohne erkennbare Toxizität.
Ein neues Playbook für klügere Antibiotikaforschung
Für Nicht-Spezialist*innen ist die Kernbotschaft, dass PolyCLOVER zeigt, wie KI und automatisierte Experimente gemeinsam völlig neue Antibiotikaklassen deutlich schneller entdecken können als bisher. Anstatt sich allein auf Zufall und langsames Screening zu verlassen, lernt dieser Ansatz aus jedem Experiment, um Polymere zu fokussieren, die sowohl gegen medikamentenresistente Bakterien angreifen als auch herkömmliche Antibiotika effektiver zu ihnen transportieren. Obwohl weitere Arbeit nötig ist, bevor eines dieser Materialien in die Klinik kommt, bietet die Studie einen vielversprechenden Weg, unser schwindendes Arsenal gegen resistente Infektionen aufzufüllen, und schlägt eine allgemeine Strategie zur Gestaltung vieler anderer intelligenter Biomaterialien vor.
Zitation: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
Schlüsselwörter: antimikrobielle Resistenz, polymerische Antibiotika, Nanopartikel, Maschinelles Lernen, medikamentenresistente Bakterien