Clear Sky Science · de
Differenzielle Störung von Membranlipiden durch Lipopeptid-Antibiotika: Colistin und Turnercyclamycine
Warum das für künftige Antibiotika wichtig ist
Medikamentenresistente Infektionen könnten bis zur Mitte dieses Jahrhunderts jährlich Millionen von Menschen das Leben kosten; zu den tödlichsten Ursachen gehören gramnegative Bakterien, die bereits vielen Antibiotika trotzen. Colistin gehört zu den wenigen verbliebenen Wirkstoffen, die solche Infektionen noch behandeln können, ist jedoch belastend für Patientinnen und Patienten, und Bakterien lernen zunehmend, ihm zu entgehen. Diese Studie analysiert, wie Colistin im Vergleich zu einer neuen Familie natürlicher Antibiotika, den Turnercyclamycinen, wirkt, und zeigt, dass winzige chemische Veränderungen sehr unterschiedliche Arten des Bakterienabtaus bewirken können — und so potenziell sicherere Medikamente ermöglichen.
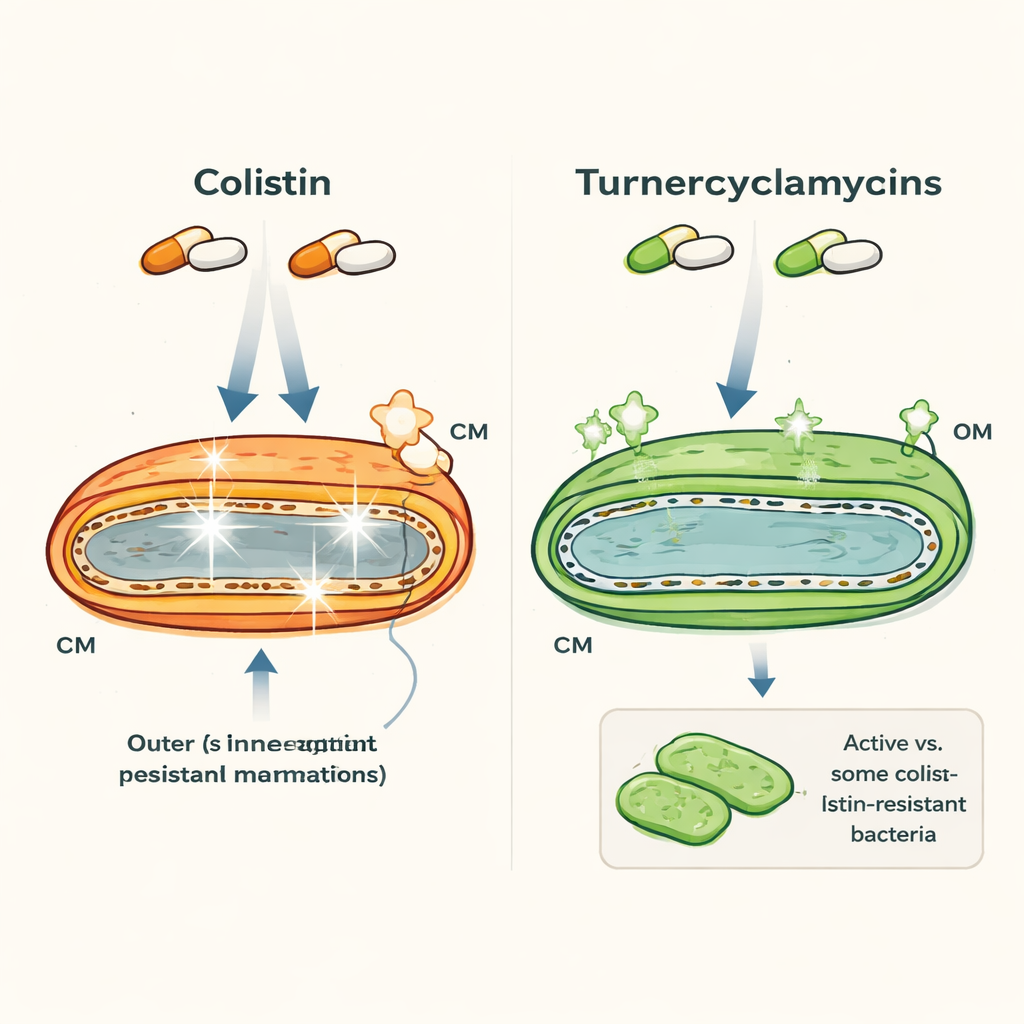
Zwei ähnlich aussehende Wirkstoffe mit sehr unterschiedlichem Verhalten
Colistin und Turnercyclamycine sind beide Lipopeptide — Moleküle, die einen fetten Schwanz mit einem Peptidring kombinieren — und richten sich gegen gramnegative Bakterien wie Escherichia coli und Acinetobacter. Auf den ersten Blick ähneln sie sich, doch ihre Eigenschaften unterscheiden sich deutlich. Colistin ist ein Reservewirkstoff, der schnell wirkt, aber Nieren und Nerven schädigen kann; zudem tragen Bakterien zunehmend Resistenzgene wie mcr-1. Turnercyclamycine, aus Schiffswurmbakterien entdeckt, töten viele der gleichen Erreger, einschließlich einiger Colistin-resistenter Stämme, zeigen in Laborversuchen jedoch deutlich geringere Toxizität. Auffällig ist, dass zwei Versionen, die sich nur durch eine kleine Verlängerung des Fettschwanzes unterscheiden, bereits unterschiedliche Resistenzmuster zeigen — ein Hinweis darauf, dass sehr subtile strukturelle Merkmale entscheidend sind.
Wie Colistin Löcher sticht und Turnercyclamycine Zeit gewinnen
Die Autorinnen und Autoren nutzten fluoreszierende Farbstoffe, Zeit‑Kill‑Assays und Elektronenmikroskopie, um zu beobachten, wie diese Wirkstoffe die bakteriellen Membranen über die Zeit beeinflussen. Colistin macht sowohl die äußere Membran als auch die innere, zytoplasmatische Membran schnell durchlässig, was innerhalb weniger Stunden zum raschen Zelltod führt. Turnercyclamycine töten dagegen langsamer — es dauert 6 bis 10 Stunden, bis Kulturen vollständig eliminiert sind — und stören hauptsächlich die äußere Membran. Farbstoffe, die aufleuchten, wenn die innere Membran verletzt wird, zeigten starke Signale bei Colistin, aber nur moderate, verzögerte Signale bei Turnercyclamycinen; hochaufgelöste Bilder bestätigten zudem wenig sichtbare Schäden an der inneren Membran, selbst wenn die Zellen abstarben. Das spricht dafür, dass Turnercyclamycine nicht über den klassischen „Porenbildenden“-Mechanismus töten, wie er bei vielen membranzielenden Antibiotika üblich ist.
Lipidbausteine als versteckte Stellschrauben
Beide Wirkstofffamilien sind letztlich vom bakteriellen Baustein Lipopolysaccharid (LPS) abhängig, der in der inneren Membran synthetisiert und normalerweise zur Außenfläche exportiert wird. Schalteten die Forschenden frühe Schritte der LPS‑Biosynthese aus, verloren sowohl Colistin als auch Turnercyclamycine ihre Aktivität; blockierten sie jedoch die Transportmaschinerie, die LPS nach außen bringt, blieben die Wirkstoffe wirksam. Das bedeutet, dass das Vorhandensein von LPS‑Bausteinen essenziell ist, ihr endgültiger Bestimmungsort jedoch nicht. Ein zentraler Unterschied zeigte sich bei direkten Bindungsmessungen: Colistin haftet an gereinigtem LPS mit mikromolarer Affinität, während für Turnercyclamycine keine messbare Bindung festgestellt wurde. Stattdessen wurden Turnercyclamycine stark von anderen Membranlipiden beeinflusst. Bestimmte Phospholipide, insbesondere Phosphatidylglycerol, konnten ihre Aktivität abschwächen oder modulieren, und die Wirkstoffe wurden leicht von äußeren Membranvesikeln — winzigen lipidbasierten Bläschen, die Bakterien abgeben — gebunden.
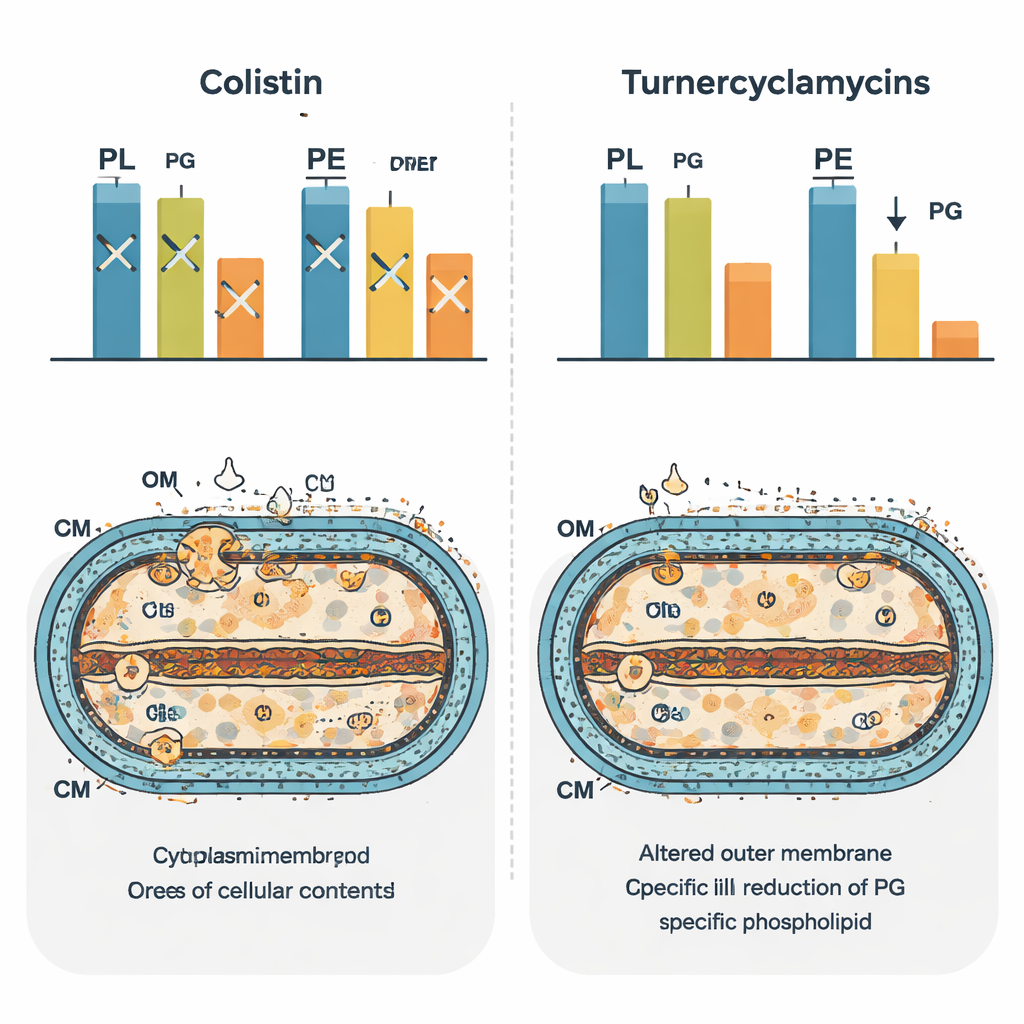
Umschaltung der bakteriellen Lipidlandschaft
Um die breiteren Auswirkungen auf die Zelle zu erfassen, verwendete das Team massenspektrometrische „Phospholipidomics“, um Hunderte von Lipidspezies nach der Behandlung zu katalogisieren. Colistin erzeugte ein charakteristisches Muster von Veränderungen, das seine breite Störung der Membranhomöostase widerspiegelt. Turnercyclamycine führten zu einem anderen Signaturmuster, das stark an Bakterien erinnerte, denen der Lipidtransporter MlaA fehlt. In diesen Zellen waren bestimmte Diacyl‑Lipide vermindert und Monoacyl‑Formen erhöht, was darauf hindeutet, dass der normale Kreislauf und die Umgestaltung von Phospholipiden zwischen den Membranen aus dem Gleichgewicht geraten waren. Bemerkenswert war der Rückgang von Phosphatidylglycerol in turnercyclamycinförderbehandelten Zellen, was die Vorstellung untermauert, dass dieses Lipid direkt mit ihrer Wirksamkeit verknüpft ist. Die Autorinnen und Autoren schlagen vor, dass Turnercyclamycine als molekulare Imitate wirken könnten, die die Wege stören, die Fettsäure-, LPS‑ und Phosphatidylglycerol‑Synthese oder ‑Transport verbinden.
Was das für die Entwicklung besserer Wirkstoffe bedeutet
Vereinfacht gesagt zeigt die Studie, dass Colistin durch rasches Aufreißen beider Schutzschichten eines gramnegativen Bakteriums tötet, unterstützt durch enge Bindung an LPS, während Turnercyclamycine eher als Saboteure der Lipidversorgungskette der Zelle fungieren. Sie gleiten in die äußere Membran, stören allmählich die Herstellung und das Recycling bestimmter Lipide und lassen schließlich die Zellhülle versagen — ohne die innere Membran massiv zu zerstören. Weil dieser schonendere, gezieltere Mechanismus mit geringerer Toxizität und einem anderen Resistenzprofil einhergeht, bietet sein Verständnis eine Roadmap für die Gestaltung neuer Lipopeptid‑Antibiotika. Durch Feinabstimmung von Merkmalen wie Länge und Sättigungsgrad des Fettschwanzes könnten Chemiker Wirkstoffe entwickeln, die menschliches Gewebe schonen, gegen Colistin‑resistente Stämme wirksam bleiben und im Wettlauf gegen antibiotikaresistente Bakterien einen Schritt voraus sind.
Zitation: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Schlüsselwörter: Antibiotikaresistenz, gramnegative Bakterien, Colistin, Lipopeptid-Antibiotika, Membranlipide