Clear Sky Science · de
Strukturelle Grundlage der dynamischen Konformationen von AP-4 und seiner Assoziation mit ARF1
Wie Zellen ihre Fracht sortieren und verschicken
Jede Zelle ist ein geschäftiges Lagerhaus, das ständig tausende Protein‑„Pakete“ an die richtigen Ziele sortiert und verschickt. Wenn dieses Liefersystem in Nervenzellen gestört ist, können schwerwiegende Störungen von Gehirn und Bewegungssteuerung die Folge sein. Diese Studie entschlüsselt, wie eine wichtige Versandmaschine, genannt AP-4, ihre Form ändert und sich mit einem Regulationsprotein, ARF1, zusammentut, um Fracht in winzige Transportbläschen zu laden — und warum ihre Beweglichkeit für gesunde Neurone so wichtig ist.
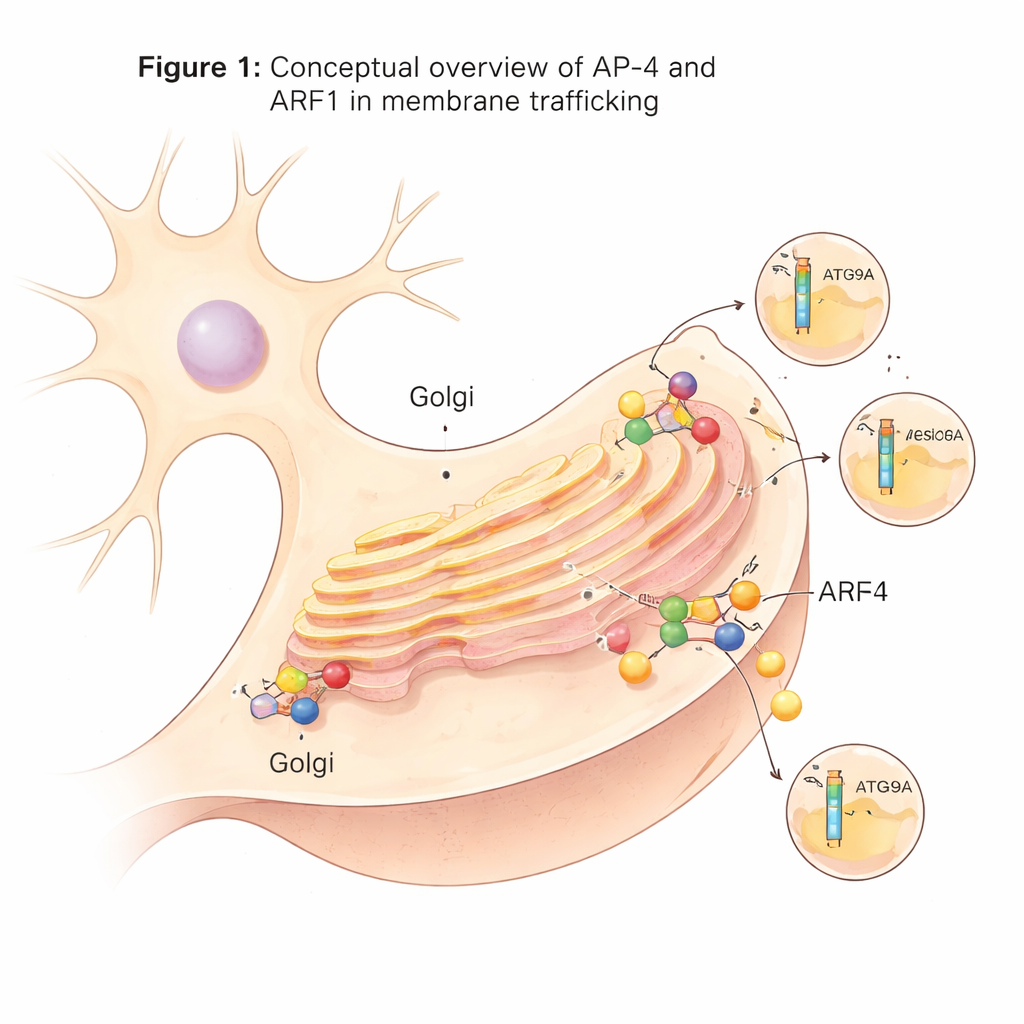
Ein spezialisierter Versandapparat in Nervenzellen
Innerhalb der Zellen entstehen viele Transportvesikel an einer zentralen Sortierstation, dem trans‑Golgi‑Netzwerk. Diese Vesikel sind auf Adaptorkomplexe (AP‑Komplexe) angewiesen, die wie Ladestellen funktionieren: sie erkennen Frachtproteine und helfen, um sie herum beschichtete Vesikel zu formen. AP‑4 ist einer dieser Adapter und ungewöhnlich, weil es—anders als viele andere—nicht das verbreitete Gerüstprotein Clathrin nutzt. Obwohl AP‑4 in vielen Geweben vorkommt, spielt es besonders in Neuronen eine wichtige Rolle. Fehlt AP‑4 oder ist es defekt, können essenzielle Frachtproteine wie das autophagiebezogene Protein ATG9A und bestimmte Glutamatrezeptoren nicht richtig transportiert werden, was zu einer schweren neuroentwicklungsbedingten Erkrankung führt, der sogenannten AP‑4‑Defizienzsyndrom.
Ein formwandelnder Komplex in Ruhe
Die Autoren nutzten Kryo‑Elektronenmikroskopie, eine leistungsfähige Bildgebungsmethode zur Darstellung großer Proteinassemblies, um die dreidimensionale Struktur des AP‑4‑„Kerns“ in Lösung zu bestimmen. AP‑4 besteht aus vier Untereinheiten, die zusammen eine schalenartige Struktur bilden. Sie fanden heraus, dass AP‑4 nicht in einer einzigen starren Form verharrt. Stattdessen wechselt es natürlich zwischen einer „geschlossenen“ Form, in der eine Untereinheit (die C‑terminale Domäne der mittleren Untereinheit) in die Mitte der Schale eingezogen ist, und einer „offenen“ Form, in der dieses Stück hinausschwingt und hochflexibel wird. Einzelmolekül‑Fluoreszenzexperimente zeigten zusätzlich, dass diese Untereinheit mindestens drei Zustände einnimmt—geschlossen, teilweise offen und vollständig offen—was offenbart, dass AP‑4 von Natur aus dynamisch ist, noch bevor es an Membranen bindet.
ARF1s Rolle: Rekrutierer, nicht Hauptschalter
Viele verwandte Adaptorkomplexe werden von einer inaktiven in eine aktive Form geschaltet, wenn sie kleine Regulatorproteine namens ARFs binden. Um zu klären, wie das für AP‑4 funktioniert, lösten die Forschenden Strukturen von AP‑4 in Komplex mit ARF1, einem kleinen GTP‑bindenden Protein, das an Membranen verankert ist. Sie fanden, dass ARF1 hauptsächlich an eine der großen AP‑4‑Untereinheiten nahe deren N‑Termin bindet, ähnlich wie bei anderen AP‑Komplexen. Überraschenderweise löst die ARF1‑Bindung keine dramatische strukturelle Umordnung in AP‑4 aus. Geschlossene und offene Formen koexistieren weiterhin, und die Gesamtarchitektur bleibt weitgehend unverändert. Biochemische Tests bestätigten, dass spezifische Kontaktstellen zwischen ARF1 und AP‑4 für die Membranrekrutierung essenziell sind, aber ARF1 allein bringt AP‑4 nicht in einen einzigen aktiven Zustand.
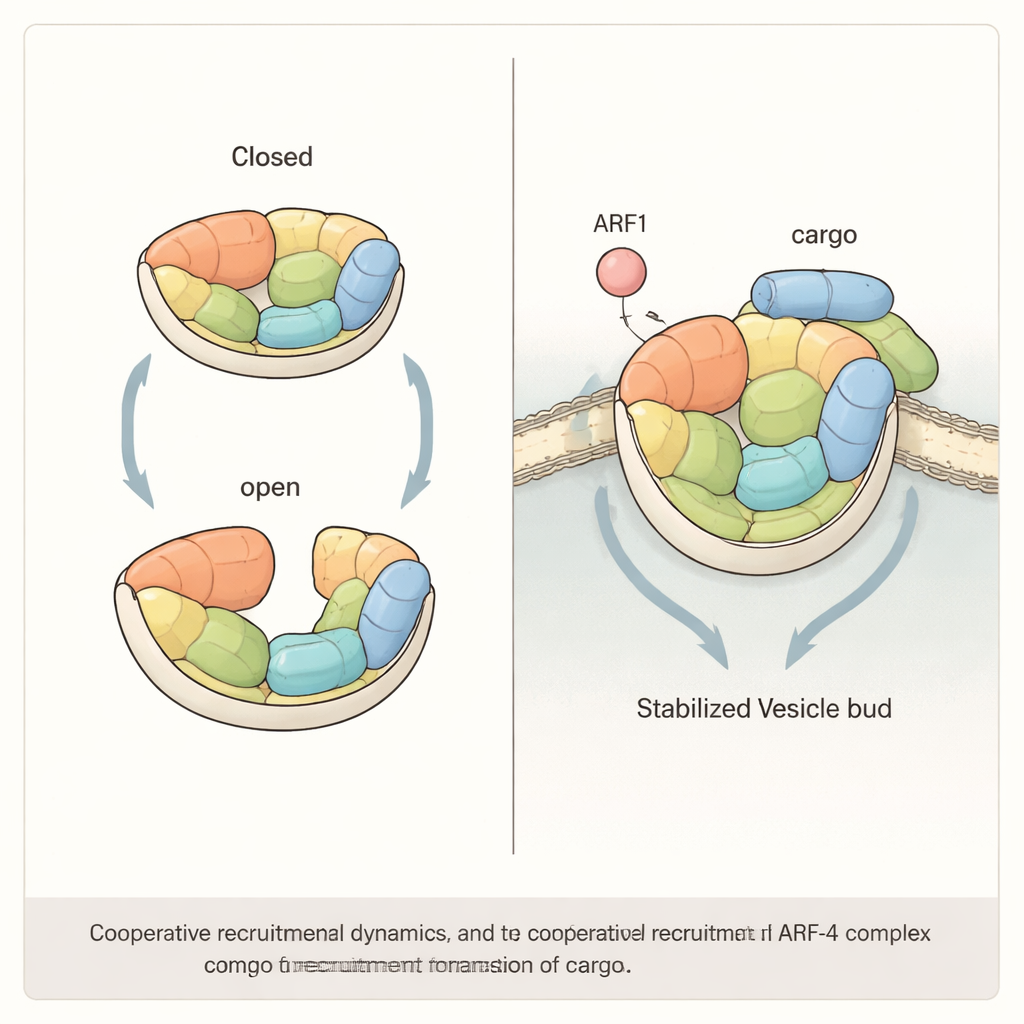
Zusammenarbeit von Regulator und Fracht
Die Studie zeigt weiter, dass die effiziente Rekrutierung von AP‑4 an Membranen wahrscheinlich die Kooperation von ARF1 und den Frachtproteinen selbst erfordert. Durch Rekonstituierung des Systems auf künstlichen Perlen und Liposomen fanden die Autoren, dass entweder ARF1 oder ein kurzes C‑Terminalstück des Frachtproteins ATG9A AP‑4 anziehen kann, bei gleichzeitigem Vorhandensein beider Faktoren jedoch deutlich mehr AP‑4 rekrutiert wird als durch bloßes Addieren ihrer einzelnen Effekte zu erwarten wäre. Wenn die Forschenden Mutationen einführten, die AP‑4 starrten und seine Fähigkeit verminderten, zwischen offenen und geschlossenen Zuständen zu wechseln, ging dieser synergistische Effekt verloren. In humanen Zellen, denen eine Schlüsseluntereinheit von AP‑4 fehlte, konnten lediglich solche „starren“ mutierten Versionen des Komplexes den normalen ATG9A‑Transport vom Golgi nicht wiederherstellen — ein Hinweis darauf, dass die Flexibilität von AP‑4 keine bloße Kuriosität ist, sondern eine funktionelle Voraussetzung.
Warum Beweglichkeit für die Gehirngesundheit wichtig ist
Insgesamt zeichnet die Arbeit AP‑4 als einen formwandelnden Adapter, der mehrere Konformationen in Lösung und an Membranen ausprobiert. ARF1 wirkt weniger als Ein‑/Aus‑Schalter denn als membranbasierter Rekrutierer, der gemeinsam mit Frachtproteinen AP‑4 in produktiven Konfigurationen für die Vesikelbildung stabilisiert. Wird dieses Gleichgewicht gestört—durch Schwächung der ARF1‑ oder Frachtbindung oder durch Einfrieren von AP‑4 in einer einzigen Form—beeinträchtigt das den Frachtexport vom Golgi und kann zu neuroentwicklungsbedingten Erkrankungen beitragen. Indem die Studie die strukturelle Grundlage des dynamischen Verhaltens von AP‑4 offenlegt, liefert sie einen Rahmen zum Verständnis AP‑4‑verwandter Störungen und deutet auf mögliche Strategien hin, den richtigen Transport in betroffenen Neuronen wiederherzustellen.
Zitation: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Schlüsselwörter: Membrantransport, AP-4-Adaptorkomplex, ARF1, Vesikelbildung, neuroentwicklungsstörung