Clear Sky Science · de
ZNF683+ NK-Zellen steuern die Chemotherapieempfindlichkeit bei fortgeschrittenem HPSCC durch Umgestaltung des Immunmikromilieus
Warum bestimmte Chemotherapien bei einigen Halskrebserkrankungen besser wirken
Menschen mit fortgeschrittenem Hypopharynxkarzinom — einem tief im Rachen verborgenen Tumor — erhalten oft aggressive Chemotherapie mit unsicherem Ausgang. Manche Tumoren schrumpfen deutlich, andere kaum. Diese Studie stellt eine einfache, aber entscheidende Frage: Was unterscheidet die Tumoren, die gut ansprechen? Indem die Forschenden einzelne Immunzellen nacheinander untersuchen, entdecken sie eine bestimmte Art von „Schutz“-Zelle, die das Gleichgewicht zwischen Erfolg und Misserfolg der Standardchemotherapie kippen kann.
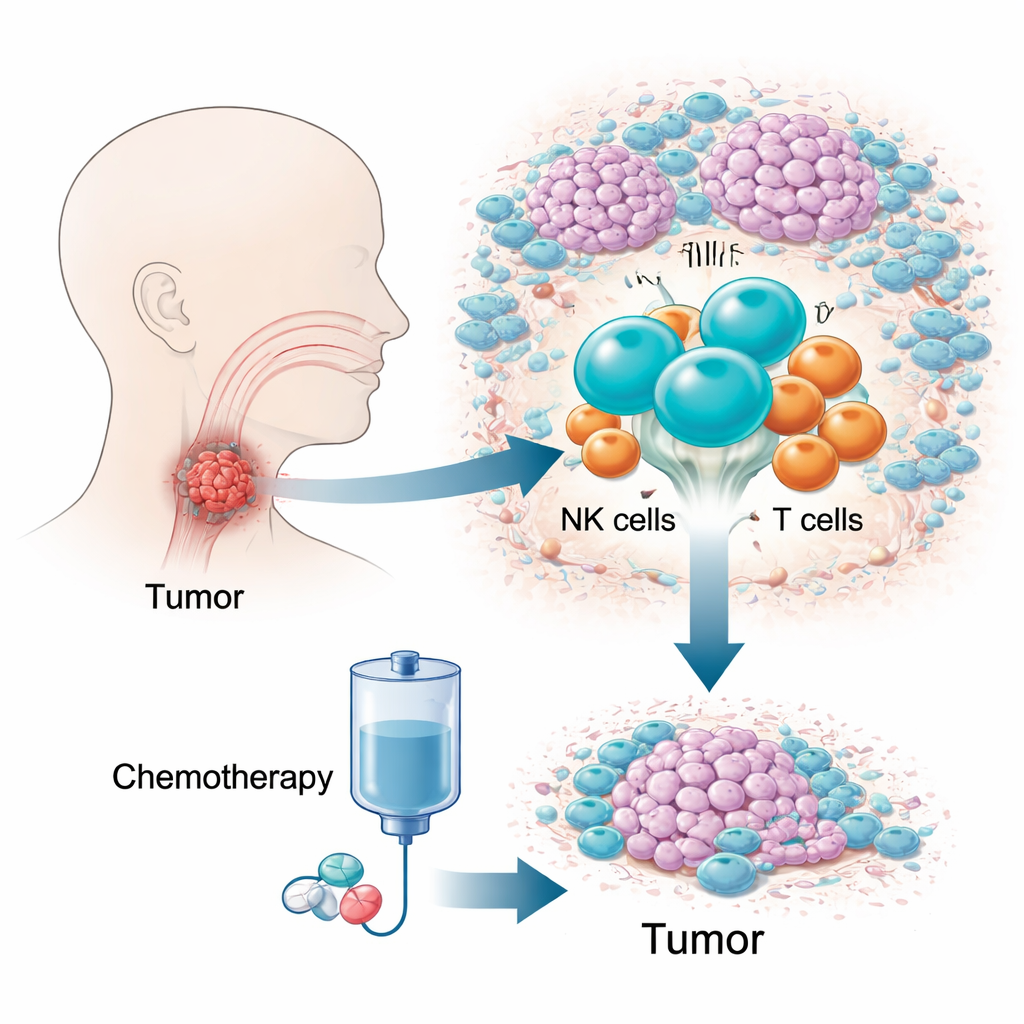
Die Herausforderung eines verborgenen, schwer zu behandelnden Krebses
Das hypopharyngeale Plattenepithelkarzinom zählt zu den tödlichsten Kopf-Hals-Tumoren, teilweise weil es in einem beengten, schwer zu untersuchenden Bereich wächst und in frühen Stadien wenige Symptome verursacht. Viele Patientinnen und Patienten werden spät diagnostiziert, wenn die Optionen begrenzt sind und die Fünf-Jahres-Überlebensraten niedrig sind. Eine Wirkstoffkombination, bekannt als TPF-Chemotherapie, wird weit verbreitet eingesetzt, weil sie die Erkrankung kontrollieren kann und die Stimmlippen oft erhält. Dennoch sprechen 10–20 Prozent der Patientinnen und Patienten kaum oder gar nicht an und verlieren so wertvolle Zeit. Traditionelle genetische Tests, die Signale über Millionen von Zellen mitteln, konnten diesen Unterschied nur schwer erklären; die Autoren richteten ihren Blick daher auf das lebende Ökosystem der Immunzellen im Tumor.
Die immunologische Landschaft des Tumors Zelle für Zelle lesen
Die Forschenden begleiteten 12 Patientinnen und Patienten über die Zeit, entnahmen Tumorproben vor und nach zwei Zyklen der TPF-Chemotherapie und analysierten mehr als 150.000 Immunzellen auf Einzelzellniveau. Zusätzlich wurden 41 weitere Patientinnen und Patienten untersucht, um zentrale Befunde mittels Bildgebung und Durchflusszytometrie zu bestätigen. Durch Kartierung der Genaktivität und Zelltypen entstand ein detailliertes Atlas des Tumormikromilieus: T-Zellen, B-Zellen, Makrophagen, dendritische Zellen, Mastzellen, Neutrophile und natürliche Killerzellen (NK-Zellen). Unter all diesen Akteuren fiel ein Muster besonders auf. Vor der Behandlung wiesen die Tumoren, die später schrumpften, deutlich mehr NK-Zellen auf als die therapieresistenten Tumoren — und je höher der Anteil an NK-Zellen, desto stärker die spätere Tumorverkleinerung.
Eine spezielle NK-Zell-Untergruppe bereitet T-Zellen auf den Erfolg vor
Bei genauerer Betrachtung teilte das Team die NK-Zellen anhand molekularer Merkmale in drei Gruppen. Nur eine davon, gekennzeichnet durch den Transkriptionsfaktor ZNF683 und überwiegend im Gewebe um Tumornester lokalisiert, korrelierte stark mit gutem Chemotherapieansprechen. Patientinnen und Patienten, deren Tumoren zu Beginn mehr dieser ZNF683+ NK-Zellen enthielten, profitierten deutlich häufiger von TPF. In Mausexperimenten machte die Entfernung von NK-Zellen den Nutzen der Chemotherapie nahezu komplett zunichte, was bestätigt, dass NK-Aktivität nicht nur ein Marker, sondern eine Voraussetzung für wirksame Behandlung ist. Auffällig war, dass diese NK-Zellen nicht einfach als direkte Krebs-Killer agierten; vielmehr waren ihre Genprogramme angereichert für Aktivitäten, die T-Zellen anleiten und aktivieren.
Wie NK-Zellen potente tumorzerstörende T‑Zellen ermöglichen
Um zu verstehen, welche T‑Zellen am wichtigsten waren, verfolgten die Wissenschaftler einzelne T‑Zell-Rezeptor-Klone vor und nach der Behandlung. Sie fanden, dass bei den Ansprechern eine spezifische Gruppe von CD8‑„Effektor‑Memory“-T‑Zellen, die reich an dem Molekül GZMK ist, nach der Chemotherapie dramatisch expandierte. Diese T‑Zellen produzierten hohe Mengen der toxischen Zytokine TNF und Interferon‑gamma, ohne tiefere Erschöpfungszeichen zu zeigen, und waren dadurch kraftvolle, langlebige Effektorzellen. Räumliche Bildgebung zeigte, dass sich diese GZMK+ CD8‑T‑Zellen nach der Behandlung in Tumoren der Ansprechenden stark zusammenlagerten, nicht jedoch in denen der Nichtansprechenden. In Labor-Co-Kultur-Experimenten mit menschlichen Zellen förderte direkter Kontakt mit ZNF683+ NK-Zellen das Wachstum dieser GZMK+ CD8‑Untergruppe — ein Effekt, der verschwand, wenn die Zellen durch eine Barriere getrennt wurden.
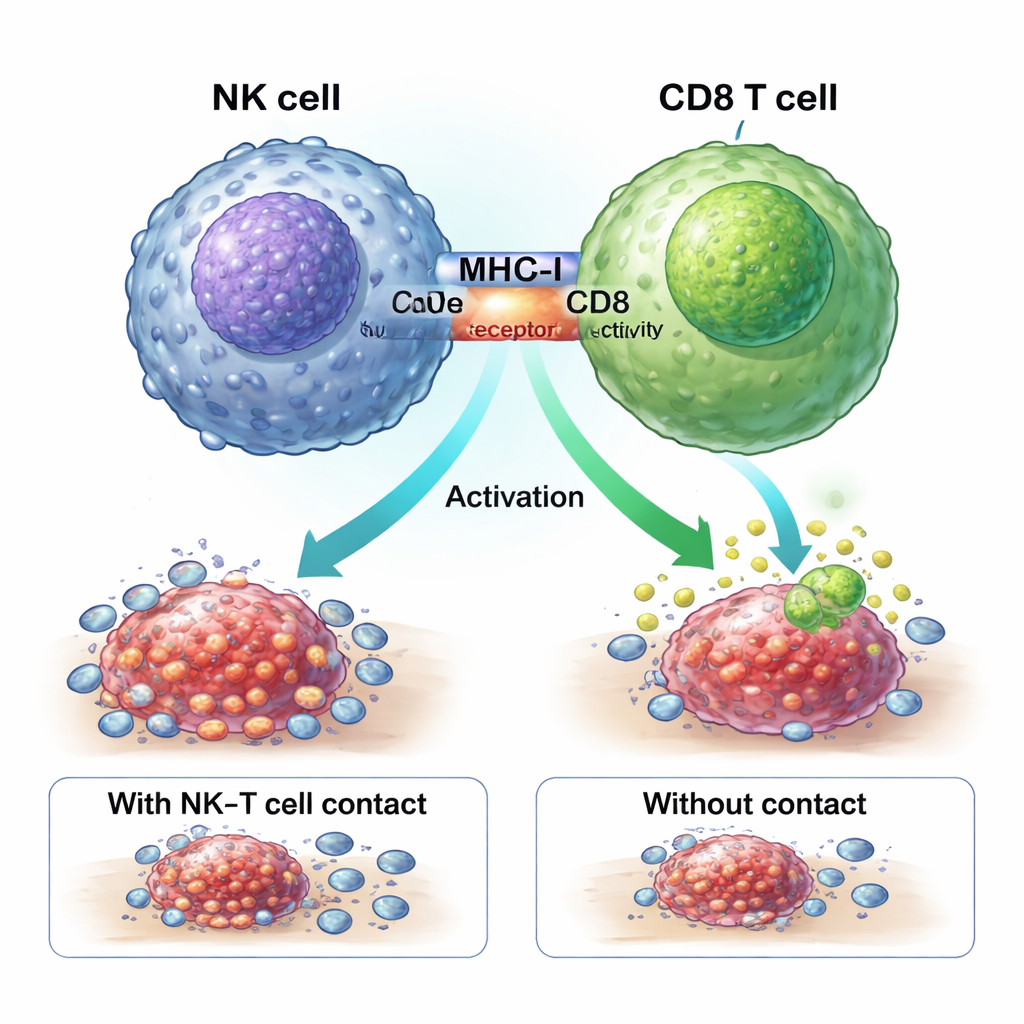
Ein physischer Händedruck, der Tumorfighter einschaltet
Die Studie zeigt, dass ZNF683+ NK‑Zellen die Chemotherapieantwort über einen physischen „Händedruck“ mit CD8‑T‑Zellen verstärken. Moleküle namens MHC‑I an der NK‑Zelloberfläche binden an CD8‑Rezeptoren auf T‑Zellen in einer engen Kontaktzone, der Immun‑Synapse. Das Blockieren von MHC‑I verhinderte, dass NK‑Zellen die potenten GZMK+ CD8‑T‑Zellen erzeugten. In speziell konstruierten Mäusen, denen ZNF683 nur in NK‑Zellen fehlte, exprimierten diese NK‑Zellen weniger MHC‑I und waren deutlich schlechter darin, CD8‑T‑Zellen zu aktivieren — ein Befund, der die Vorstellung stützt, dass ZNF683 NK‑Zellen darauf programmiert, effektive Trainer für T‑Zell‑Kämpfer zu sein, statt einfache Vollstrecker.
Was das für Patientinnen und Patienten bedeutet
Für nichtfachliche Leser ist die Kernbotschaft: Nicht alle Immunzellen im Tumor sind gleichwertig. Diese Arbeit identifiziert eine bestimmte NK‑Zell‑Untergruppe als Vorhut, die das Schlachtfeld vor Beginn der Chemotherapie vorbereitet. Tumoren, die reich an diesen Zellen sind, sind bereit, nach Wirkstoffgabe Wellen starker CD8‑T‑Zellen freizusetzen, was zu deutlich besserer Tumorverkleinerung führt. Die Messung der Häufigkeit dieser NK–T‑Zell‑Achse vor der Behandlung könnte Ärzten helfen vorherzusagen, wer von TPF profitiert und wer alternative oder zusätzliche Therapien benötigen könnte. In Zukunft könnten Therapien, die diese ZNF683+ NK‑Zellen stärken oder nachahmen, resistente Hypopharynxkarzinome empfindlicher für Standardchemotherapie machen.
Zitation: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Schlüsselwörter: Hypopharynxkarzinom, Chemotherapie-Resistenz, Natürliche Killerzellen, tumorimmunes Mikromilieu, CD8-T-Zellen