Clear Sky Science · de
Photoinitiierte selektive N–N-Bindungsbildung durch Nutzung von Nitrenfreisetzung und -transfer
Ein neuer Weg, Stickstoffatome zu verbinden, erhellt
Stickstoffatome stehen im Zentrum vieler Arzneimittel, Pflanzenschutzmittel und moderner Materialien. Chemiker sind sehr gut darin, Stickstoff an Kohlenstoff zu binden, doch das direkte Verbinden zweier Stickstoffatome ist deutlich schwieriger. Diese Studie stellt eine lichtgetriebene, metallfreie Methode vor, um Stickstoffatome kontrolliert miteinander zu verknüpfen und damit einen einfacheren Zugang zu einer breiten Palette nützlicher Moleküle zu eröffnen.
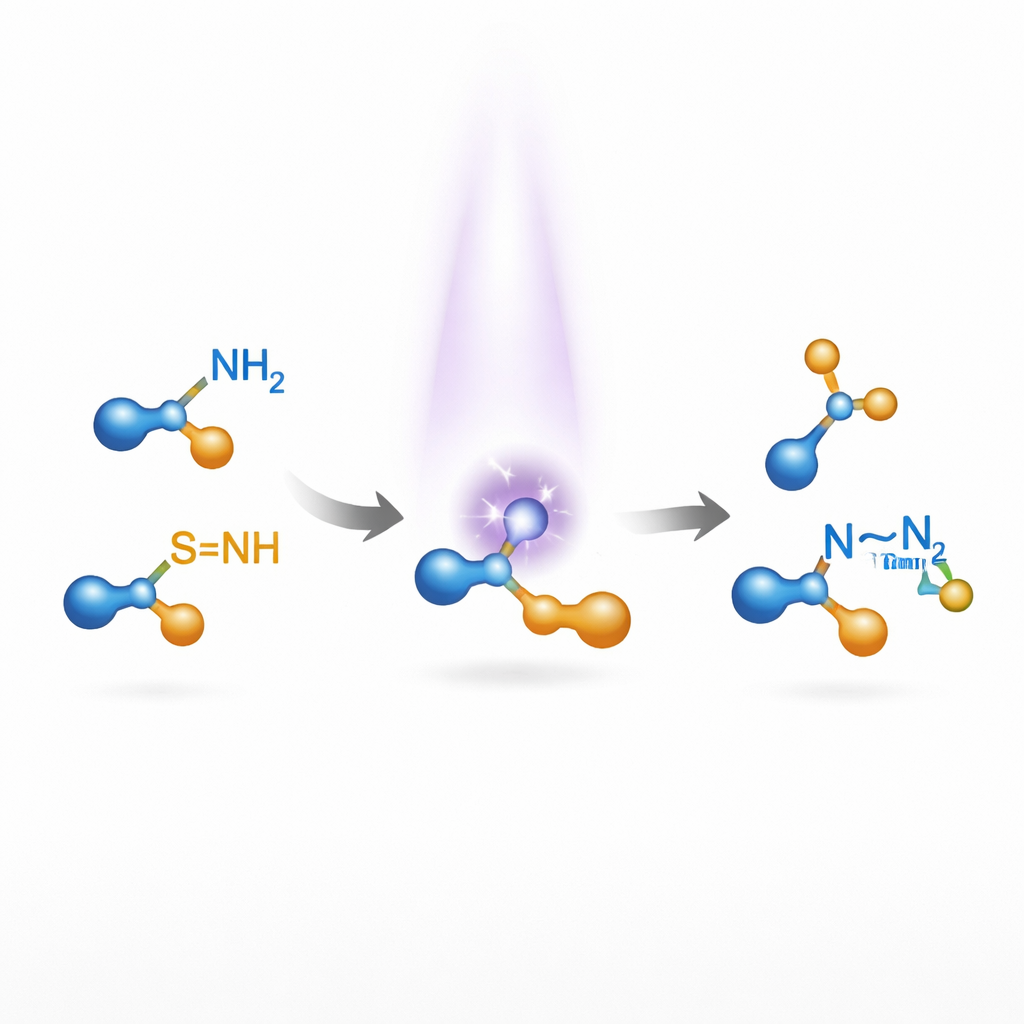
Warum es schwer ist, Stickstoff mit Stickstoff zu verbinden
Viele Naturstoffe und Arzneistoffe enthalten Stickstoffpaare, die miteinander gebunden sind — ein Muster, das das Verhalten eines Moleküls im Körper oder in Materialien beeinflussen kann. Bestehende Methoden zum Aufbau solcher N–N-Einheiten beginnen meist mit vorgefertigten Stickstoff–Stickstoff-Fragmenten wie Hydrazinen oder Diazoverbindungen und werden dann Schritt für Schritt modifiziert. Die direkte Schmiedung der N–N-Bindung aus einfachen Aminen ist verlockend, aber schwierig: Stickstoff ist relativ elektronegativ, weshalb zwei Stickstoffatome nicht natürlich eine stabile, unpolare Bindung bilden. Frühere Erfolge beruhten stark auf Übergangsmetallkatalysatoren und funktionierten oft nur für enge Molekülfamilien, wodurch ihre Nützlichkeit für die Entdeckungschemie begrenzt war.
Mit Licht einen reaktiven Zwischenzustand zähmen
Die Autoren wandten sich Nitrenen zu — hochreaktiven, kurzlebigen Stickstoffspezies, die prinzipiell in andere Bindungen inserieren können. Traditionelle Nitrenchemie benötigt typischerweise Metallkatalysatoren und leidet oft unter Nebenreaktionen, weil Nitrene sehr energiereich sind. Das Team fragte, ob sich Nitrene mit Licht auf schonendere, kontrolliertere Weise und ohne Metalle erzeugen und dann nutzen lassen, um einfache Amine zu N–N-enthaltenden Produkten zu verknüpfen. Ihr wichtiger Einfall war, Sulfilimine zu verwenden — eine Molekülklasse, die sich leicht anpassen lässt und im UV- bis nahsichtbaren Bereich Licht absorbiert. Unter Bestrahlung können diese Sulfilimine so gespalten werden, dass ein Nitrenfragment freigesetzt wird, während ein unproblematisches schwefelhaltiges Nebenprodukt zurückbleibt.
Ein breites, metallfreies Rezept für Stickstoffpaare
Nach systematischen Tests identifizierten die Forscher ein bestimmtes Sulfilimin, das unter 365-Nanometer-Licht in Chloroform effizient mit vielen Aminen zu Hydrazidprodukten reagiert — Molekülen, die eine frisch gebildete N–N-Bindung neben einer Carbonylgruppe tragen. Sie optimierten Faktoren wie die Sulfiliminstruktur, das Lösungsmittel und die Lichtintensität, um das gewünschte Produkt gegenüber häufigen Nebenprodukten wie Harnstoffen zu bevorzugen. Unter diesen milden Bedingungen koppelte eine große Vielfalt von Aminen — aromatisch wie aliphatisch sowie cyclische Varianten — erfolgreich. Außerdem zeigten sie, dass viele unterschiedliche Sulfilimine mit aromatischen und aliphatischen Acyl- sowie Sulfonylgruppen gut reagieren und dutzende verschiedene N–N-haltige Produkte liefern. Wichtig ist, dass die Methode auch spät in einer Synthese anwendbar ist, um komplexe, biologisch aktive Moleküle wie gängige entzündungshemmende Wirkstoffe und chirale Bausteine zu modifizieren, was ihre Praxistauglichkeit für Wirkstoff- und Materialchemie demonstriert.
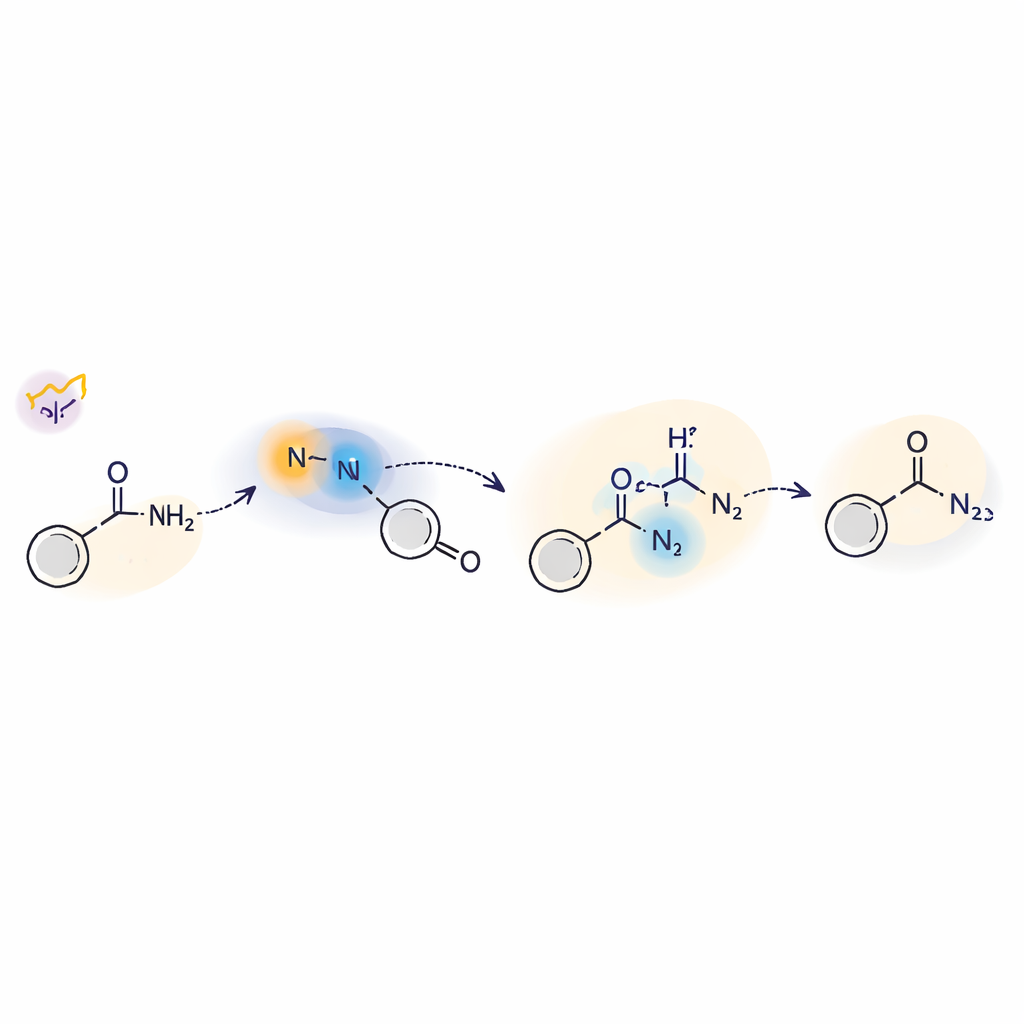
Ein Blick unter die Haube des lichtgesteuerten Schritts
Um zu verstehen, wie diese lichtgetriggerte Chemie funktioniert, kombinierten die Forscher Experimente und Theorie. Sie verwendeten Radikalfänger, Isotopenmarkierung und Elektronenspinresonanz, um zu zeigen, dass während der Reaktion freie Nitrenzwischenstufen und stickstoffzentrierte Radikale auftreten. Zeitaufgelöste Laserspektroskopie offenbarte zwei wichtige Formen des Nitrens: einen kurzlebigen Triplettzustand und einen länger lebenden Singulettzustand. Die Singulettform reagiert direkt mit Aminen durch eine Art nukleophilen Angriff, während das Triplett an Wasserstoff-Atom-Transfer-Schritten teilnehmen kann. Rechnerische Berechnungen stützten einen Mechanismus, bei dem Licht das Sulfilimin anregt, die Schwefel–Stickstoff-Bindung gespalten wird und das entstehende Nitren dann das Amin über sowohl Singulett- als auch Triplettwege angreift, bevor es zur finalen Hydrazidstruktur umgeformt wird.
Was das für zukünftige Moleküle bedeutet
Diese Arbeit zeigt, dass sorgfältig konstruierte Sulfilimine als „Nitrenreservoirs“ dienen können, die reaktive Stickstoffeinheiten bei Bedarf unter Lichteinfluss und ohne Metalle freisetzen. Indem man sowohl die Singulett- als auch die Triplettpersönlichkeiten der Nitrene nutzt und gleichzeitig ihre Konzentration niedrig hält, erzielt die Methode eine selektive Bildung von N–N-Bindungen über eine breite Palette von Bausteinen. Für Nichtfachleute lautet die Erkenntnis, dass Chemiker nun einen einfacheren, saubereren und flexibleren Weg haben, Stickstoffatome miteinander zu verbinden — ein Ansatz, der die Entstehung neuer Medikamente, Agrochemikalien und stickstoffreicher Materialien beschleunigen könnte.
Zitation: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Schlüsselwörter: Nitrenchemie, photoinitiierte Reaktionen, N–N-Bindungsbildung, Sulfilimine, Hydrazide