Clear Sky Science · de
Ausnutzung von PV‑Oxiren zur modularen Synthese von α‑Oxy‑Carbonylverbindungen
Warum winzige chemische Verbindungsstücke wichtig sind
Viele moderne Arzneimittel, Pflanzenschutzmittel und Hochleistungswerkstoffe beruhen auf kleinen molekularen „Verbindern“, die größere Einheiten zusammenhalten und deren Eigenschaften fein abstimmen. Eine solche Familie von Verbindern, die α‑oxy Carbonylverbindungen, kann die Stabilität eines Medikaments, die Faltung eines Peptids oder die Eigenschaften eines Kunststoffs verändern. Dennoch waren diese vielversprechenden Linker überraschend schwer auf flexible, „mix‑and‑match“‑Weise herzustellen. Dieser Artikel beschreibt eine neue, milde Methode, mit der Chemiker schnell viele verschiedene α‑oxy Carbonylverbindungen aus einfachen Startmaterialien aufbauen können — und damit neue Möglichkeiten in der Wirkstoffentwicklung, chemischen Biologie und Materialwissenschaft eröffnen.
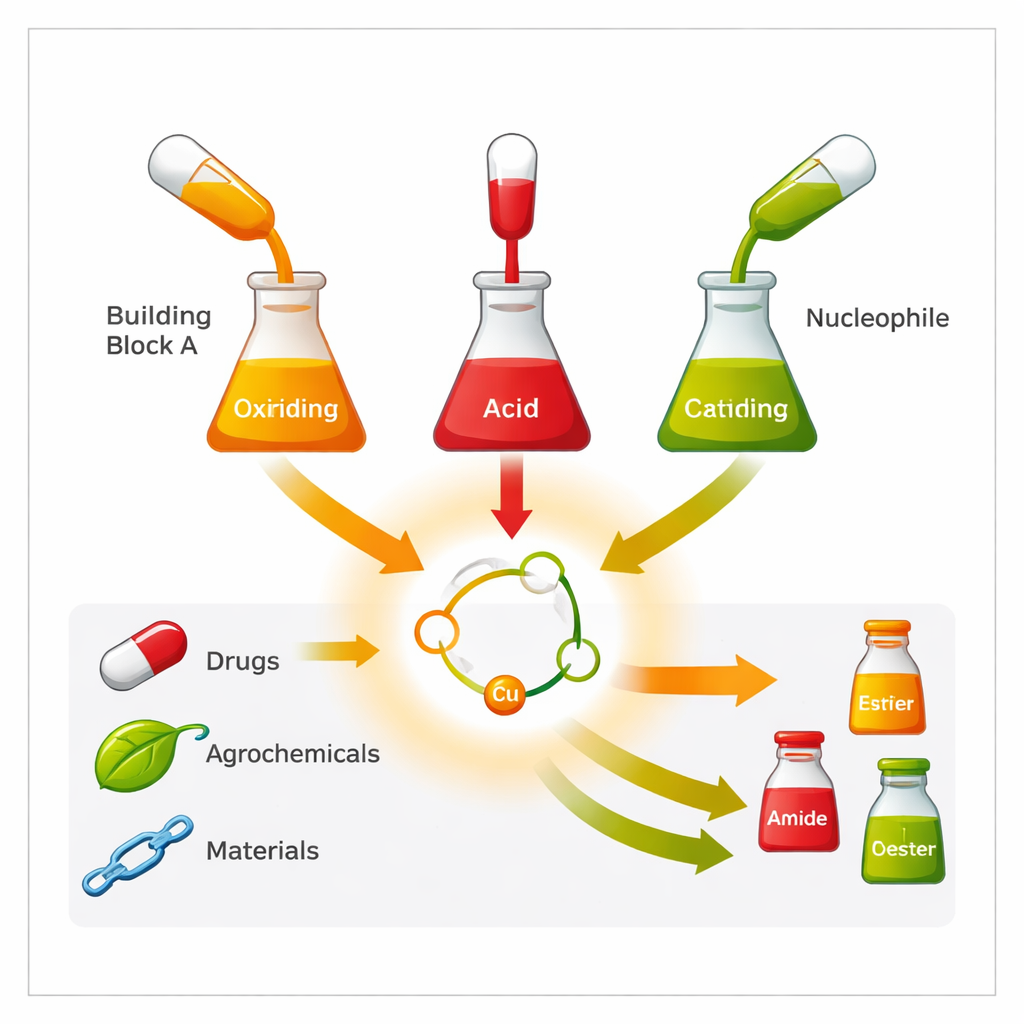
Ein besseres chemisches Werkzeug bauen
α‑Oxy Carbonylverbindungen kommen sowohl in der Natur als auch in der Technik vor — von Krebsmedikamenten und Antibiotika bis hin zu biologisch abbaubaren Polymeren und Herbiziden. Eine eng verwandte Gruppe, die α‑Hydroxysäuren, lässt sich sogar in proteinähnliche Ketten einbauen, um deren Faltungs‑ und Interaktionsverhalten fein zu justieren, was wiederum beeinflusst, wie sie biologische Ziele erkennen. Bestehende Zugänge zu diesen Linkern beruhen oft auf mehrstufigen Sequenzen, harten Reagenzien oder einem engen Satz an Bausteinen. Diese Einschränkungen erschweren es Chemikern, schnell neue Strukturen zu erkunden oder komplexe Wirkstoffmoleküle spät in der Entwicklung zu modifizieren.
Eine neue Dreiteil‑Montagelinie
Die Forschenden stellen eine kupferbasierte Reaktion vor, die drei einfache Bausteine in einem Ansatz zusammenfügt: ein speziell entwickeltes „Ylid“‑Reagenz, eine gewöhnliche Carbonsäure (eine Gruppe, die in zahllosen Naturstoffen und Arzneistoffen vorkommt) und einen dritten Partner, der Stickstoff, Sauerstoff, Schwefel, Selen oder Wasser einbringt. Unter milden Bedingungen und ohne Edelmetalle werden diese drei Teile zu α‑oxy Carbonylprodukten wie Estern, Amiden, Thioestern und verwandten Strukturen verbunden. Die Reaktion toleriert viele weitere empfindliche Funktionen — Doppelbindungen, Nitrile, Sulfide und komplexe Ringsysteme — und eignet sich damit direkt für komplizierte, wirkstoffähnliche Moleküle.
Eine flüchtige Ringstruktur für Kontrolle nutzen
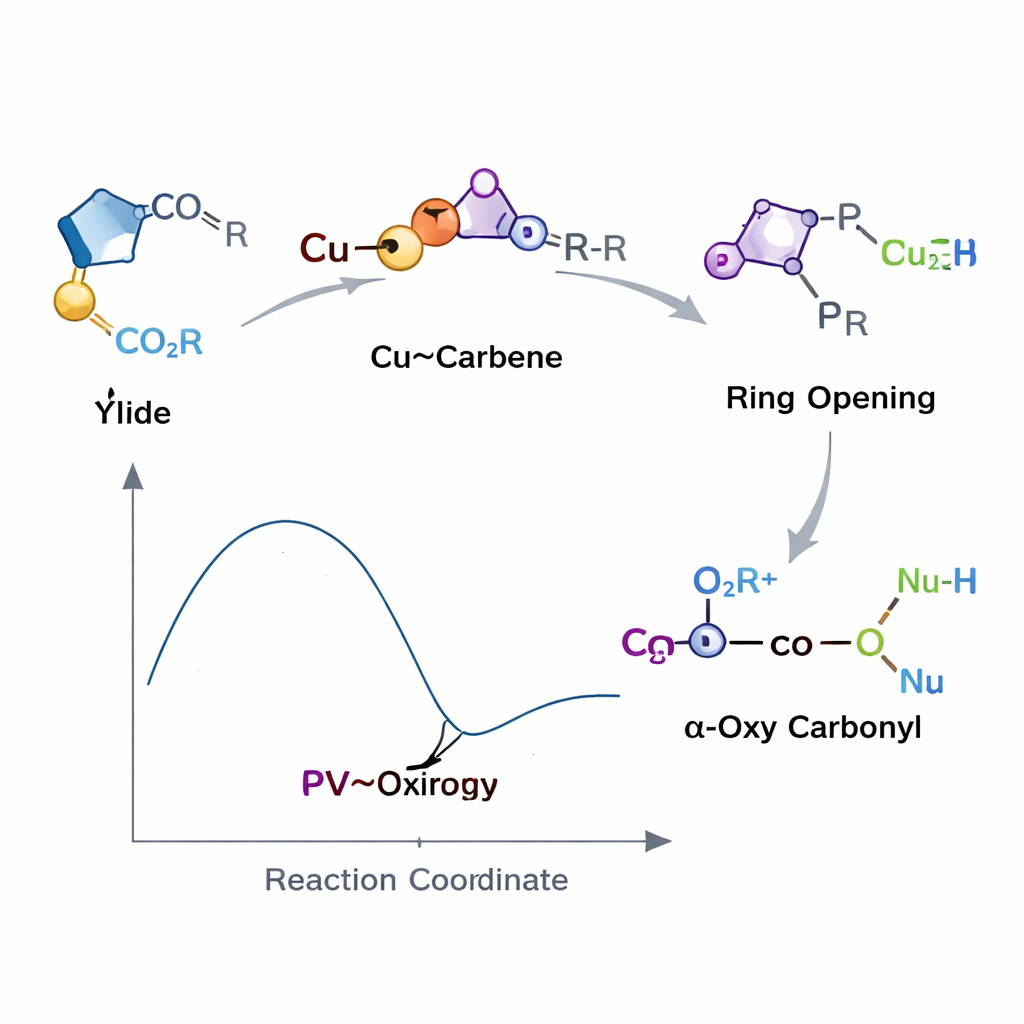
Hinter dieser neuen Methode steht ein ungewöhnlicher, stark verzerrter Ring, das Oxiren, das lange als kurzlebige Kuriosität statt als praktisches Werkzeug galt. Indem die Gruppe ein phosphorhaltiges Fragment in den Ring einbettet und das Oxiren kurzzeitig mit Hilfe von Kupfer erzeugt, verwandelt das Team diese reaktive Struktur in eine steuerbare Zwischenstufe. Die Carbonsäure wird zunächst zu einem geladenen Partner, der das Oxiren an einer bevorzugten Position angreift und die Reaktion so lenkt, dass ein Hauptprodukt entsteht statt eines unübersichtlichen Gemisches. Das entstandene Zwischenprodukt überträgt dann seinen Acyl‑Teil auf das dritte Nukleophil und liefert das finale α‑oxy Carbonyl in einem Schritt, der an einen sorgfältig choreografierten Staffelstabwechsel erinnert.
Von Peptiden bis zu Herbiziden und darüber hinaus
Um das Potenzial dieser Chemie zu demonstrieren, stellen die Autorinnen und Autoren kurze, peptidähnliche Ketten her, in denen normale Verbindungen durch Esterbindungen aus α‑Hydroxysäuren ersetzt sind. Solche „Depsipeptide“ sind wertvolle Werkzeuge, um zu untersuchen, wie kleine Änderungen im Rückgrat die biologische Funktion beeinflussen, sind aber meist schwer zugänglich. Dieselbe Strategie liefert außerdem das kommerzielle Herbizid Lactofen in einem einzigen Schritt aus einem bekannten Vorläufer und erzeugt rasch neue Analoga, die über ältere Methoden umständlich herzustellen wären. Darüber hinaus zeigen die Forschenden, dass sich durch Kombination der neuen Reaktion mit wenigen einfachen Schritten Carbonsäuren um ein Kohlenstoffatom verlängern lassen, während gleichzeitig eine α‑Hydroxygruppe eingeführt wird — eine Umwandlung, die in der Wirkstoffchemie sehr geschätzt wird.
Was das für die Zukunft bedeutet
In praktischer Hinsicht bietet diese Arbeit Chemikern ein vielseitiges, benutzerfreundliches Werkzeug zum Einbau von α‑oxy Carbonyl‑Verbindern fast überall dort, wo eine Carbonsäure und ein Nukleophil vorhanden sind — selbst in komplexen, bioaktiven Molekülen. Auf einer tieferen Ebene zeigt sie, dass ein einst esoterisches Zwischenprodukt, das Oxiren, gezähmt und in der alltäglichen Synthese nutzbar gemacht werden kann. Indem ein flüchtiger Ring zu einem kontrollierbaren Schritt in einer Montagelinie wird, erweitert die Methode das Angebot an molekularen Verbindern für die Wirkstoffgestaltung, die Untersuchung biologischer Systeme und die Entwicklung neuer Materialien.
Zitation: Huang, S., Duan, D., Luo, J. et al. Harnessing PV-oxirene for the modular synthesis of α-Oxy carbonyls. Nat Commun 17, 1918 (2026). https://doi.org/10.1038/s41467-026-68671-2
Schlüsselwörter: alpha‑oxy Carbonylverbindungen, modulare Synthese, Kupferkatalyse, Depsipeptide, Carbonsäure‑Funktionalisierung